DE ROL VAN
18
F-FDG PET/CT IN DE
UITWERKING
VAN
ASEPTISCHE
INFLAMMATIE
Diane Pavlenko
Stamnummer: 01509900Promotor: Prof. dr. Ingeborg Goethals
Masterproef voorgelegd in het kader tot het behalen van de graad Master of Medicine in de Geneeskunde
Deze pagina is niet beschikbaar omdat ze persoonsgegevens bevat.
Universiteitsbibliotheek Gent, 2021.
This page is not available because it contains personal information.
Ghent University, Library, 2021.
Voorwoord
Deze masterproef is het resultaat van anderhalf jaar intensief werk. Het was een leerrijk proces waarbij ik hulp heb gekregen en gesteund werd door een aantal personen. Ik zou graag gebruik willen maken van deze gelegenheid om jullie te bedanken.
Allereerst wil ik mijn promotor Prof. Dr. Ingeborg Goethals bedanken voor het geduld, de begeleiding, opbouwende kritiek en de grondige verbeteringen van mijn thesis. Ik kreeg de nodige vrijheid om dit werk zelfstandig tot een goed einde te brengen, maar werd telkens bijgestuurd wanneer dit noodzakelijk was. Ondanks de drukke agenda nam ze telkens opnieuw de tijd om deze masterproef in goede banen te leiden.
Ten tweede wil ik de stafleden van de dienst nucleaire geneeskunde bedanken: Dr. B. Van den Broeck, Dr. K. De Man en Dr. V. Schelfhout. Oprechte dank voor jullie sympathie, interesse in dit werk en de motiverende woorden telkens wanneer jullie mij zagen.
Vervolgens nog een dankwoord aan Johan Keppens en Sam Donche. Ik mocht altijd rekenen op jullie hulp en uitleg over de technische aspecten van deze masterproef.
Als laatste wil ik mijn gezin bedanken. Van het begin af aan hebben jullie mij altijd geleerd om het beste van mezelf te geven, en dit van toepassing op elk gebied in het leven. Jullie geven me altijd moed om te blijven doorzetten, hoe moeilijk het soms ook is.
Inhoudsopgave
1. Abstract ... 1
2. Inleiding ... 2
2.1. Positron emissie tomografie ... 2
2.1.1. Radionucliden en radioactief verval ... 2
2.1.2. Fluorine-18 fluorodeoxyglucose (18F-FDG) ... 4
2.2. Computertomografie (CT) ... 6
2.3. 18F-FDG hybride PET/CT-beeldvorming ... 7
2.4. Koorts/inflammatie van onbekende oorsprong ... 8
2.4.1. Definitie ... 8
2.4.2. Klinische benadering ... 9
2.4.3. Plaats van 18F-FDG PET/CT-beeldvorming volgens de SNMMI/EANM richtlijnen ... 10
2.5 Verschillende entiteiten van aseptische inflammatie ... 10
2.5.1. Grote bloedvaten vasculitis ... 10
2.5.2. Systeemlijden ... 13 2.5.2.1. Inflammatoir gewrichtslijden ... 13 2.5.2.1.1. Reumatoïde artritis ... 13 2.5.2.1.2. Spondyloartritis ... 16 2.5.2.1.3. Polymyalgia reumatica ... 19 2.5.2.2. Polychondritis recidivans ... 22 2.5.2.3. Inflammatoir darmlijden ... 23 2.5.2.4. Longen ... 25 2.5.2.4.1. Interstitieel longlijden ... 25 2.5.2.4.2. Sarcoïdose ... 27 2.5.3. Tumorkoorts ... 30 2.6. Vraagstelling ... 32 3. Methodologie ... 33 3.1. Patiëntengroep ... 33 3.2. 18F-FDG PET/CT-beoordeling ... 34 3.3. Finale diagnose ... 34
3.4. Vergelijking van het 18F-FDG PET/CT-resultaat versus de finale diagnose ... 35
3.5. Bijdrage van 18F-FDG PET/CT-beeldvorming in de diagnostische uitwerking ... 35
3.6. Statistische analyse ... 37
4. Resultaten ... 38
4.1. Patiënt karakteristieken ... 38
4.2. Finale diagnose ... 39
5. Discussie ... 44
5.1. Bijdrage van 18F-FDG PET/CT-beeldvorming in de diagnostische uitwering ... 44
5.2. Richtlijnen ... 45
5.3. Sterktes en beperkingen van de studie ... 46
5.4. Conclusie ... 46
1. Abstract
Inleiding: koorts/inflammatie van onbekende oorsprong/origine vormt een majeure uitdaging in de klinische praktijk met meer dan 200 mogelijke differentiaaldiagnoses. De rol hierin van 18F-FDG
PET/CT-beeldvorming is echter nog onduidelijk.
Doelstelling: de rol bepalen van 18F-FDG PET/CT in de diagnostische uitwerking van patiënten
met koorts/inflammatie van onbekende oorsprong.
Methodologie: er werd een prospectief monocentrisch onderzoek uitgevoerd in UZ Gent. Alle patiënten die voldeden aan de definitie van koorts/inflammatie van onbekende oorsprong (volgens Durack en Street / Vanderschueren) en die in het kader hiervan tussen 06/09/2018 en 31/06/2019 een 18F-FDG PET/CT-onderzoek ondergingen werden geïncludeerd in de studie.
De bevindingen van het 18F-FDG PET/CT-onderzoek werden getoetst aan de bevindingen bij het
klinisch onderzoek, de resultaten van de biochemie en follow-up (≥ 3 maand). Er zijn 3 belangrijke oorzaken van FUO, met name niet-infectieuze inflammatoire aandoeningen (NIIA), infecties en maligniteiten.
Resultaten: er werden 66 patiënten geïncludeerd in de studie (33 mannen, 33 vrouwen). In totaal kon bij 35/66 (53.0%) patiënten een finale diagnose gesteld worden. 17 (25.8%), 11 (16.7%) en 4 (6.1%) patiënten hadden respectievelijk een NIIA, infectie of maligniteit als oorzaak van de koorts/inflammatie. De resterende 3 patiënten (4.5%) waren niet onder te brengen in 1 van deze categorieën. Het 18F-FDG PET/CT-onderzoek was in 59/66 behulpzaam in de diagnostische
uitwerking van koorts/inflammatie van onbekende oorsprong.
De sensitiviteit, specificiteit en diagnostische accuraatheid van 18F-FDG PET/CT-beeldvorming
was respectievelijk 94.3%, 83.9% en 89.4%.
Conclusie en toekomstperspectieven: 18F-FDG PET/CT heeft een hoge specificiteit, sensitiviteit
en diagnostische accuraatheid voor de uitwerking van koorts/inflammatie van onbekende oorsprong. Deze studie ondersteunt aldus het advies van experten om 18F-FDG PET/CT op een
vroeg tijdstip in de diagnostische uitwerking te includeren. Onderzoek naar de impact op hospitalisatieduur en totale hospitalisatiekost lijkt bijzonder interessant/is aangewezen.
2. Inleiding
2.1. Positron emissie tomografie
2.1.1. Radionucliden en radioactief verval
Positron emissie tomografie (PET) is een diagnostische nucleaire beeldvormingstechniek waarmee biochemische processen niet-invasief in beeld gebracht worden aan de hand van radiofarmaca. Een radiofarmacon bestaat uit twee elementen: een radionuclide en een carrier molecule (1, 2). Een radionuclide is een onstabiele nucleaire variant van een chemisch element. Stabiele elementen hebben een gelijk aantal protonen en neutronen in de kern, bij een radionuclide daarentegen is het !"#$#%&%
%&'$"#%&% ratio verschillend. Dit zorgt ervoor dat de nucleaire configuratie
onstabiel is. Aangezien elk element streeft naar een toestand van minimale energie, proberen radionucliden op basis van radioactieve vervalprocessen een grotere nucleaire stabiliteit te verkrijgen. Om dit te bekomen vindt in de kern een desintegratie plaats waarbij protonen- en neutronenaantallen worden gewijzigd, waardoor de massa afneemt. Gebaseerd op de fysische formule E = m.c2 neemt zo ook de energie van de kern af, die vrijkomt onder de vorm van
ioniserende straling (1, 2).
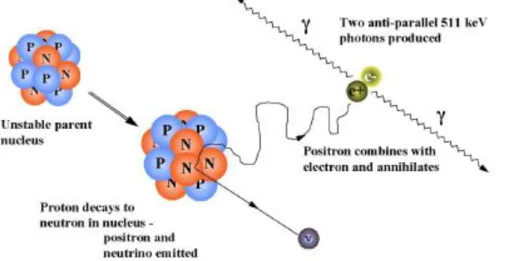
Er zijn verschillende manieren waarop radioactief verval kan plaatsvinden, maar de werking van PET-beeldvorming baseert zich op het b+-verval van een radionuclide (figuur 1).
Figuur 1: voorstelling van b+-verval van een radionuclide (3).
De overmaat aan protonen in de kern zorgt voor een onstabiele nucleaire configuratie. Hierdoor wordt een proton omgezet in een neutron. Dit resulteert in de uitzending van een positron (b+ deeltje) en een neutrino. Een neutrino is een ongeladen partikel zonder massa en interageert na
zijn uitzending niet met het omringend weefsel. Een positron daarentegen bezit dezelfde massa als een elektron, maar heeft een positieve lading. Na zijn uitzending verplaatst het positron zich over een korte afstand doorheen het medium en verliest hierbij geleidelijk kinetische energie. Wanneer het deeltje uiteindelijk tot stilstand komt, bindt het een vrij elektron van het weefsel en ondergaat een annihilatieproces (4). De 2 gebonden deeltjes verdwijnen samen en de massa van beiden komt vrij als kinetische energie. Deze energie bestaat uit de uitzending van 2 fotonen in tegengestelde richting (±180°) met elk een energie van 511 keV en wordt annihilatiestraling genoemd (1, 2). Het zijn deze annihilatiefotonen die geregistreerd worden door PET-detectoren (4).
De PET-detectoren omringen de patiënt 360° en bestaan uit honderden aangrenzende scintillatiekristallen. Indien 2 detectoren die zich tegenover elkaar bevinden binnen een bepaald tijdsvenster (gebruikelijk 3-15 nanoseconden) beiden een foton vaststellen met een energievenster rond 511 keV, wordt dit een coïncidentie genoemd (figuur 2) (4). Het fotonpaar wordt dan beschouwd als ontstaan uit hetzelfde annihilatieproces gelegen ergens op de verbindingslijn tussen de 2 detectoren. Na interactie van het foton met het scintillatiekristal ontstaat een lichtflits. Deze wordt waargenomen door de fotomultiplier buis welke rechtstreeks in verbinding staat met het scintillatiekristal en het finale beeld reconstrueert (1). Een registratie van miljoenen coïncidenties is noodzakelijk om een beeld te vormen van de radiofarmacon distributie in het lichaam (4).
2.1.2. Fluorine-18 fluorodeoxyglucose (18F-FDG)
Om biochemische processen in beeld te brengen moet de radionuclide gekoppeld worden aan een carriermolecule. Deze past op specifieke receptoren in het lichaam. De combinatie van een radionuclide en een carriermolecule noemt men een radiofarmacon. Er bestaan verscheidene radiofarmaca, maar één van de meest gebruikte voor PET-beeldvorming is een combinatie van de radionuclide fluorine-18 (18F) en de carriermolecule fluorodeoxyglucose (FDG) (1).
FDG is een glucose analoog waarbij de hydroxylgroep (-OH) in de moleculaire structuur gesubstitueerd is door een fluorine atoom (5). Het mechanisme van 18F-FDG signaal amplificatie
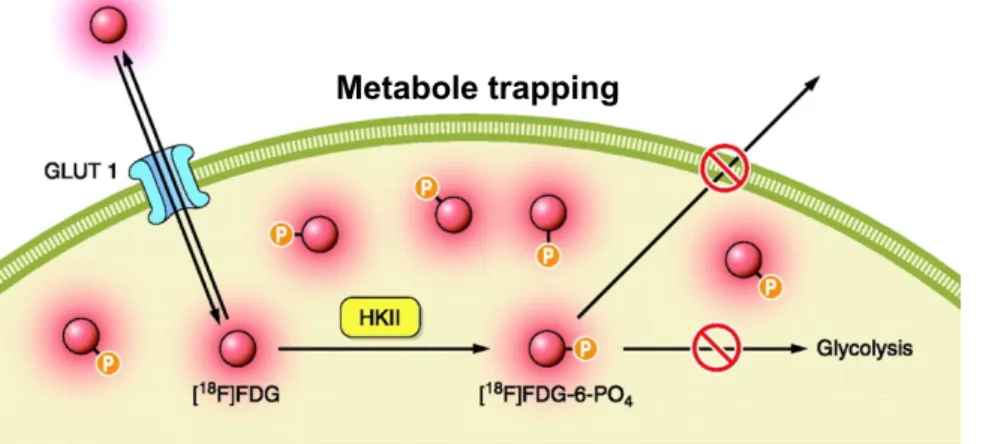
wordt weergegeven in figuur 3.
Figuur 3: mechanisme van 18F-FDG PET-signaal amplificatie (5).
18F-FDG wordt net zoals glucose opgenomen in de cel doorheen glucose transporters (GluT) in de cellulaire
membraan. Intracellulair wordt deze zoals glucose gefosforyleerd door het enzym hexokinase, waardoor 18
F-FDG-6-PO4gevormd wordt. Glucose ondergaat verder de glycolyse, maar 18F-FDG-6-PO4 is geen substraat
van deze enzymen. Hierdoor blijft het na de eerste metabolisatiestap gefixeerd in de cel. Dit fenomeen wordt metabole trapping genoemd en vormt de basis voor 18F-FDG PET-beeldvorming.
De graad van 18F-FDG opname in een cel komt overeen met de cellulaire metabole activiteit en het
aantal GluT’s in de cellulaire membraan. Weefsel met een verhoogd glucosemetabolisme, zoals tumorcellen en inflammatoire cellen, vertoont een verhoogde 18F-FDG opname en dus ook een
verhoogde metabole trapping van het 18F-FDG-6-PO4intracellulair (6).In multipele weefsels in het lichaam die voor hun energievoorziening afhangen van glucose is er fysiologische 18F-FDG
opname. Deze normale biodistributie moet herkend worden voor een correcte interpretatie / lezing van de 18F-FDG PET-beelden en wordt weergegeven in figuur 4 (7).
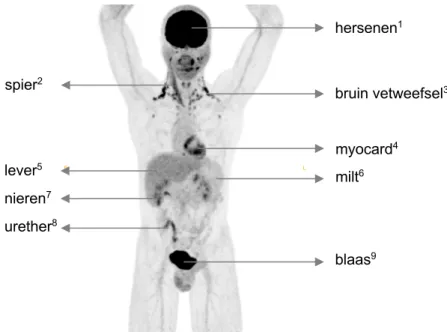
Figuur 4: totaal lichaam 18F-FDG PET-beeld van de normale 18F-FDG biodistributie. Verklaring voor de 18
F-FDG opname in deze weefsels volgt hieronder (7).
1 predominant glucosemetabolisme 2 spiertonus
3 thermogenese
4 mate van 18F-FDG opname afhankelijk van de voorkeur voor glucose of vrije vetzuren voor energielevering 5 glycogenese
6 hematopoëse
7,8,9 urinaire tractus: urinaire excretie van gefosforyleerd 18F-FDG dat ontsnapt aan metabole trapping
Vooraleer een 18F-FDG PET-onderzoek wordt uitgevoerd, dienen bij elke patiënt maatregelen
getroffen te worden om de fysiologische 18F-FDG opname zo beperkt mogelijk te houden (tabel 1)
(1, 4, 7, 8). Op deze manier wordt de gevoeligheid van 18F-FDG opname voor targetweefsel
behouden (4).
Tabel 1: patiëntvoorbereiding voor 18F-FDG PET-beeldvorming.
Maatregel Verklaring
Minstens 4-6u voor het onderzoek nuchter zijn Minimale competitie tussen endogeen glucose en 18F-FDG voor cellulaire GluT’s
Blaas ledigen voor het onderzoek Visuele beoordeling van het bekken mogelijk maken
Temperatuur van de wachtruimte rond
20-22°C Beperken van de thermogenese in bruin vetweefsel Vermijden van zware fysieke inspanning tot 24
uur voor het onderzoek Beperken van de fysiologische
18F-FDG opname in spierweefsel
Geen insulinetoediening voor het onderzoek bij diabeten
Beperken van de 18F-FDG opname doorheen insulinedependente GluT’s in dwarsgestreepte spieren hersenen1 bruin vetweefsel3 myocard4 milt6 lever5 blaas9 urether8 nieren7 spier2
Om het belang van de patiëntvoorbereiding te verduidelijken wordt in onderstaand figuur (figuur 5) een 18F-FDG PET-beeld weergegeven waarbij deze niet nageleefd werd.
Figuur 5: 18F-FDG PET-beeld van een diabetespatiënt die wegens hyperglycemie insulinetoediening kreeg
voor het onderzoek. 18F-FDG werd hierdoor snel en massaal opgenomen in de dwarsgestreepte spieren
doorheen de insulinedependente GluT-4 transporters. Hierdoor bleef te weinig 18F-FDG over om
pathologische processen in beeld te brengen. Het beeld van de hersenen benadrukt deze bevinding. Hoewel de hersenen voor hun energielevering volledig afhangen van glucose, is er nagenoeg geen 18F-FDG opname
waar te nemen (rode cirkel) (7).
2.2. Computertomografie (CT)
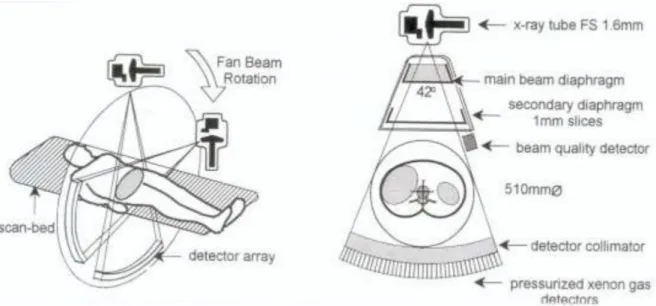
CT-beeldvorming weergeeft morfologische structuren. Het berust op de differentiële attenuatie van röntgenstraling (X-stralen) door verschillende weefsels. Attenuatie omvat het principe van een gradueel verlies aan intensiteit van een X-stralenbundel bij doorgang van weefsel. Elk type weefsel heeft een specifieke attenuatiecoëfficiënt (µ). Hoe groter de weefseldensiteit, hoe groter µ (2, 9). Het basisprincipe van een CT-scanner wordt weergegeven in figuur 6. De patiënt ligt op een computergestuurde tafel die geschoven wordt door een opening in een grote ring. Hierin bevinden zich de X-stralenbuis en het detectorsysteem (9). Er worden opeenvolgende axiale scans gemaakt waarbij de roterende X-stralenbuis met een hoge snelheid 360° rond de patiënt beweegt en een smalle bundel X-stralen uitzendt. De hoeveelheid straling die door de patiënt geraakt en dus niet geabsorbeerd wordt door het weefsel, valt op het detectorsysteem dat zich in een boogvorm aan de tegenoverliggende zijde van de X-stralenbuis bevindt. Deze informatie wordt verwerkt voor de finale beeldreconstructie (2, 9).
Figuur 6: basisprincipe van een CT-scanner (2).
2.3. 18F-FDG hybride PET/CT-beeldvorming
Het grootste nadeel van PET-beeldvorming is een beperkte anatomische detailweergave. Dit kan overwonnen worden door integratie van een PET- en een CT-beeldvormingsonderzoek in één geheel en wordt hybride PET/CT-beeldvorming genoemd. De beelden van beide onderzoeken worden met behulp van hardware gefuseerd en gecoregistreerd (4).
De ontwikkeling hiervan brengt de volgende voordelen met zich mee: nauwkeurige anatomische lokalisatie van 18F-FDG opname en all-in-one principe, waardoor de patiënt slechts één keer
aanwezig dient te zijn voor het onderzoek (4).
Voor het onderzoek krijgt de patiënt intraveneus iodine contrastmiddel en een intraveneuze 18
F-FDG injectie. De patiënt dient hierna 45-60 minuten in rust door te brengen in een voorbereidingsruimte. Zodoende wordt een adequate 18F-FDG biodistributie bereikt (1). De tafel
waar de patiënt op ligt gedurende het onderzoek schuift door een grote opening in een ring waarin zowel de PET- als de CT-component in tandem geïncorporeerd zijn (8). De CT-scan wordt uitgevoerd net voor de PET-scan en beide scans strekken zich uit van het hoofd tot het midden van de dijen van de patiënt (4, 8). Aangezien de scans opeenvolgend uitgevoerd worden, moeten positionele veranderingen van de patiënt zo miniem mogelijk gehouden te worden (6).
Het gebruik van 18F-FDG hybride PET-beeldvorming ter opsporing van inflammatie berust op het
feit dat ook geactiveerde leukocyten een verhoogd glucosemetabolisme vertonen met upregulatie van glucosetransporters in de cellulaire membraan (voornamelijk GluT-1 en GluT-3) (10).
De distributie van 18F-FDG op een hybride PET/CT-onderzoek wordt visueel beoordeeld.
Desgewenst maakt men ook gebruik van semikwantificatie (8).
2.4. Koorts/inflammatie van onbekende oorsprong 2.4.1. Definitie
Het begrip ‘koorts van onbekende oorsprong’ werd gedefinieerd door Petersdorf en Beeson in 1961, waarbij voldaan werd aan 3 criteria (tabel 2) (11, 12). De intentie van deze definitie was om zelflimiterende infecties en habituele hyperthermie te elimineren als oorzaak van koorts, alsook voldoende tijd te rekenen voor de diagnostische uitwerking (12).
In 1991 werd deze definitie aangepast door Durack en Street (tabel 2) (11). De eerste verandering was de classificatie van koorts in 4 categorieën: klassieke koorts (zoals oorspronkelijk beschreven door Peetersdorf en Beeson), nosocomiale koorts, neutropene koorts (neutrofielen <500/µl) en HIV-geassocieerde koorts (12). De immunogecompromitteerde patiënten werden door deze indeling geclasseerd in aparte groepen. Elk van deze groepen heeft specifieke kwetsbaarheden en vereist een andere diagnostische benadering (13).
Ten tweede werd het laatste criterium aangepast. De diagnostische periode werd hierbij verkort naar 3 dagen, en dit zowel voor gehospitaliseerde patiënten als voor de uitwerking in de ambulante zorg (12). In de huidige literatuur over koorts van onbekende oorsprong worden nog altijd beide definities gehanteerd.
Tabel 2: beide definities van koorts van onbekende oorsprong.
Petersdorf en Beeson (1961) Durack en Street (1991)
1. lichaamstemperatuur >38.3°C op minstens 3 metingen
1. lichaamstemperatuur >38.3°C op minstens 3 metingen
2. koorts is reeds ≥3 weken aanwezig 2. koorts is reeds ≥3 weken aanwezig 3. geen oorzaak gevonden na diagnostische
uitwerking gedurende minstens één week hospitalisatie
3. geen oorzaak gevonden na diagnostische uitwerking gedurende minstens 3 dagen hospitalisatie of na 3 consultaties
Voor wat betreft inflammatie van onbekende oorsprong is de literatuur schaars en is er nog geen eenduidige definitie. Een voorstel werd gedaan door Vanderschueren S. et al (11):
1) temperatuur is niet hoger dan 38,3°C op 3 verschillende metingen
2) verhoogde inflammatoire markers (CRP of bloedbezinkingssnelheid (BSE)) op minstens 3 metingen en dit gedurende ≥3 weken
3) oorzaak van de inflammatie is niet gekend onlangs diagnostische uitwerking gedurende minstens 3 dagen hospitalisatie / 3 consultaties
De klinische termen koorts en inflammatie van onbekende oorsprong worden in de praktijk door elkaar gebruikt. Het zijn majeure diagnostische uitdagingen met meer dan 200 mogelijke diagnoses (14). Gemiddeld wordt 1.5-3% van alle gehospitaliseerde patiënten hiervoor behandeld, waarvan 12-35% sterft aan de onderliggende aandoening. De mortaliteit hangt af van de aard van de aandoening en de prognose is slechter naarmate de tijd tot diagnosetelling langer wordt. Bovendien zijn er geen evidence-based richtlijnen en blijft 40% van de patiënten ongediagnosticeerd. Men verdeelt de mogelijke oorzaken in 4 grote categorieën (12):
1) Infecties
2) Niet-infectieuze inflammatoire aandoeningen (NIIA) 3) Maligniteit
4) Andere
Infecties vormen een groot aandeel van de oorzaken. Enkele voorbeelden zijn abcessen, endocarditis, tuberculose en gecompliceerde urineweginfecties (12). De groep van de NIIA’s vertoont eerder een verzameling van zeldzame aandoeningen met een leeftijdsafhankelijke verdeling. Hiertoe behoren de vasculitiden, granulomateuze aandoeningen en de reumatische aandoeningen (15). Deze entiteiten worden in 2.5. uitvoerig toegelicht. In de groep van de maligniteiten kan koorts/inflammatie gerelateerd zijn aan de maligniteit zelf (1/3de van de gevallen,
frequent in geval van lymfoom), maar kan het ook het gevolg zijn van surinfecties (2/3de van de
gevallen) (12).
De etiologie is deels ook afhankelijk van geografische factoren, economische ontwikkeling en de beschikbare diagnostische onderzoeken. Zo vormen in ontwikkelingslanden infecties de grootste groep van de oorzaken, terwijl in westerse landen NIIA’s en maligniteiten meer op de voorgrond staan (15).
2.4.2. Klinische benadering
Verscheidene studies hebben een poging gedaan om een diagnostisch protocol op te stellen voor de uitwerking van koorts/inflammatie van onbekende oorsprong (13, 15-17). Gezien de uitgebreide differentiaaldiagnostiek is dit geen evidente opdracht. Er is tot nu toe dan ook geen evidence-based protocol (13). Het is niet zinvol om een grote scala aan onderzoeken toe te passen op elke patiënt, dus een individuele benadering is van groot belang. Een algemeen aanvaarde uitwerking is anamnese en klinisch onderzoek, gevolgd door biochemie. Wanneer dit geen diagnostische aanwijzingen opbrengt, wordt overgegaan tot beeldvorming (15).
Een empirische behandeling wordt niet aanbevolen. Dit kan de diagnose camoufleren waardoor de tijd tot diagnosestelling verlengt. Er zijn slechts een aantal uitzonderingen waarbij therapie direct gestart dient te worden bij een primair diagnostisch vermoeden: antibiotica bij vermoeden van een cultuur negatieve endocarditis, tuberculostatica bij vermoeden van een actieve tuberculose en glucocorticoïden bij vermoeden van reuscelarteritis met visusverlies (8).
2.4.3. Plaats van 18F-FDG PET/CT-beeldvorming volgens de SNMMI/EANM richtlijnen
De Society of Nuclear Medicine and Molecular Imaging (SNMMI) en de European Association of Nuclear Medicine (EANM) staan beide in voor de uitwerking van richtlijnen binnen de nucleaire beeldvorming. De laatst gepubliceerde richtlijnen voor het gebruik van 18F-FDG
PET/CT-beeldvorming in de uitwerking van koorts/inflammatie van onbekende oorsprong dateren reeds van 2012. Hierin werd beschreven dat er onvoldoende evidentie is voor de implementatie van 18F-FDG
PET/CT-beeldvorming als standaard diagnostisch onderzoek in de uitwerking. Wel werd benadrukt dat op basis van de cumulatief gerapporteerde accuraatheid in de literatuur (>85%) en expertopinies kan aangenomen worden dat dit onderzoek vroeg in de uitwerking kan uitgevoerd worden, specifiek voor de volgende indicaties: koorts van onbekende oorsprong volgens de criteria van Durack en Street, postoperatieve koorts met recurrente sepsis, immunodeficiëntie-gerelateerde koorts, neutropene koorts en inflammatie van onbekende oorsprong (persistente stijging van CRP en/of BSE) (8).
2.5 Verschillende entiteiten van aseptische inflammatie 2.5.1. Grote bloedvaten vasculitis
Definitie
Vasculitiden vormen een heterogene verzameling aan inflammatoire aandoeningen van de bloedvatwanden. Er zijn een aantal manieren om het grote aantal te groeperen in categorieën, bijvoorbeeld aan de hand van etiologie, pathogenese, type van aangetaste bloedvaten, orgaandistributie… In deze masterproef wordt dit gedaan aan de hand van de 2012 Revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Hierbij worden vasculitiden gegroepeerd op basis van het caliber van de betrokken bloedvaten: grote, middelgrote en kleine bloedvaten vasculitis (figuur 7) (18). Enkel de categorie van grote bloedvaten vasculitis wordt verder besproken, vermits 18F-FDG PET/CT-beeldvorming hierin een rol speelt.
Figuur 7: (7A) indeling van vasculitiden op basis van het caliber van de betrokken bloedvaten; (7B) weergave van de grote bloedvaten in het lichaam (18).
Aantasting van de aorta en de grote aftakkingen staat op de voorgrond bij grote bloedvaten vasculitis. De 2 meest voorkomende ziektebeelden zijn Takayasu arteritis (TA) en reuscelarteritis. Deze vertonen anatomische, epidemiologische en klinische verschillen maar hebben ook overlap (19). De voornaamste kenmerken van beiden worden opgesomd in tabel 3 (18, 20, 21).
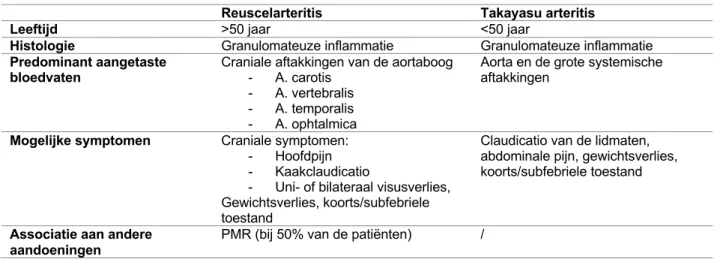
Tabel 3: voornaamste kenmerken van reuscelarteritis en Takayasu arteritis.
Reuscelarteritis Takayasu arteritis
Leeftijd >50 jaar <50 jaar
Histologie Granulomateuze inflammatie Granulomateuze inflammatie
Predominant aangetaste
bloedvaten Craniale aftakkingen van de aortaboog - A. carotis
- A. vertebralis - A. temporalis - A. ophtalmica
Aorta en de grote systemische aftakkingen
Mogelijke symptomen Craniale symptomen:
- Hoofdpijn - Kaakclaudicatio
- Uni- of bilateraal visusverlies, Gewichtsverlies, koorts/subfebriele toestand
Claudicatio van de lidmaten, abdominale pijn, gewichtsverlies, koorts/subfebriele toestand
Associatie aan andere aandoeningen
PMR (bij 50% van de patiënten) /
Een snelle bevestiging van de diagnose en behandeling van grote bloedvaten vasculitis is noodzakelijk om het risico op complicaties zoals blindheid, aorta aneurysmata en vasculaire stenoses te verminderen. De behandeling bestaat uit corticosteroïden (22).
Beeldvorming
Beeldvorming is essentieel voor de diagnose van grote bloedvaten vasculitis (23).
Reuscelarteritis met craniale symptomen wordt bevestigd aan de hand van echografie van de A. temporalis. Een niet-comprimeerbaar ‘halo teken’ is de meest suggestieve bevinding voor de ziekte. Dit houdt een homogene hypoechogene wandverdikking in, zowel zichtbaar in het longitudinale als het transversale vlak. Indien echografie niet conclusief is, is hoge resolutie MRI van de oppervlakkige craniale bloedvaten tweede keuze om de inflammatie te beoordelen. De extracraniale inflammatie kan beoordeeld worden aan de hand van MRI of 18F-FDG
PET/CT-beeldvorming (23). Grote bloedvaten vasculitis op 18F-FDG PET-beeldvorming kenmerkt zich door
hypermetabole activiteit in de betrokken bloedvatwanden. Morfologische kenmerken op CT-beeldvorming met contrast zijn bloedvatwandverdikking (≥2-3 mm) en contrastcaptatie in het adventitium en peri-adventitium. Complicaties zoals vasculaire stenoses of aneurysmata kunnen hierop ook beoordeeld worden. Vermits morfologische kenmerken worden voorafgegaan door metabole veranderingen, is 18F-FDG PET-beeldvorming geschikt voor de vroege diagnostiek van
grote bloedvaten vasculitis (24).
Indien na beeldvorming de diagnose nog altijd in vraag gesteld wordt, zijn bijkomende investigaties zoals een A. temporalis biopsie voor reuscelarteritis en/of additioneel beeldvormingsonderzoek vereist. 18F-FDG PET-beeldvorming kan niet enkel gebruikt worden voor de diagnosestelling, maar
Voorbeeld uit eigen studie
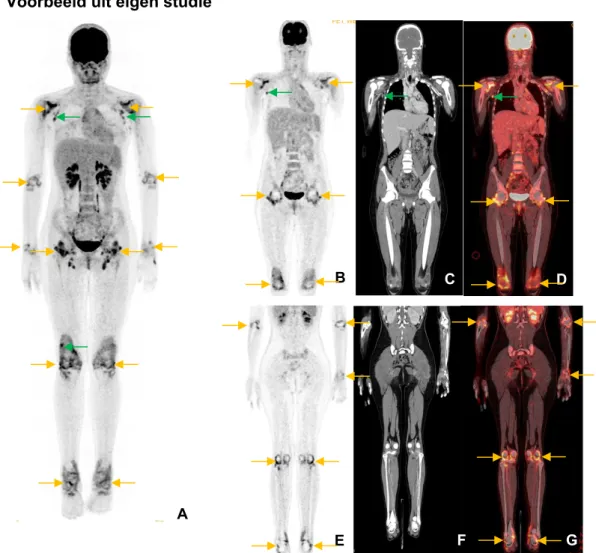
Figuur 8: grote bloedvaten vasculitis op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in profielopname: matig verhoogde 18F-FDG opname over het verloop
van de aorta thoracalis descendens. (Lever als referentieorgaan)
(B) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: mild verhoogde 18F-FDG opname over
het verloop van de aorta thoracalis ascendens, aortaboog en de aorta thoracalis descendens.
(C) en (E) thoracale axiale PET-beeld en PET/CT-fusiebeeld: matig verhoogde 18F-FDG opname over het
verloop van de aorta thoracalis ascendens (rode pijl) en aorta thoracalis descendens (oranje pijl).
(D) thoracale axiale CT-beeld in weke delen venster: geen CT-grafische afwijkingen over het verloop of in de wand van de aorta.
(F) en (H) axiale hersen PET-beeld en PET/CT-fusiebeeld: mild en (matig) intens verhoogde 18F-FDG
opname respectievelijk rechts en links over het verloop van de A. temporalis.
(G) axiale hersen CT-beeld in weke delen venster bevestigt dat de 18F-FDG opname zich situeert in de A.
temporalis.
2.5.2. Systeemlijden
2.5.2.1. Inflammatoir gewrichtslijden 2.5.2.1.1. Reumatoïde artritis
Definitie
Reumatoïde artritis (RA) is een chronische inflammatoire gewrichtsaandoening. Een auto-immuun gemedieerde inflammatie van het synovium (membraan dat de binnenzijde van een gewrichtskapsel bekleedt) leidt hierbij tot een verstoring van de gewrichtstructuur, boterosie en verlies aan functionaliteit (figuur 9). Reumafactor (RF) en anticitrulline antistoffen (anti-CCP)
A B C D E F G H
worden hierbij frequent vastgesteld op bloedonderzoek. Volgens de 2010 ACR/EULAR criteria kenmerkt RA zich klinisch door zwelling, pijn en gevoeligheid van gewrichten die langer aanhouden dan 6 weken. Hoe groter het aantal aangetaste gewrichten, hoe groter de probabiliteit dat het gaat om RA (figuur 9) (25).
De klassieke behandeling van RA bestaat uit disease-modifying antirheumatic drugs (DMARDs), in het bijzonder methotrexaat (MTX) (26).
Figuur 9: (9A) mogelijk aangetaste gewrichten door reumatoïde artritis en relatieve frequentie van aantasting (27); (9B) voorstelling van gewrichtsaantasting door reumatoïde artritis (28).
Beeldvorming
De klinische bevindingen kunnen bevestigd worden aan de hand van beeldvorming. Echografie wordt het meest gebruikt om de synovitis aan te tonen (25).
18F-FDG PET-beeldvorming representeert de metabole activiteit van de synovitis in de aangetaste
gewrichten. Regionale lymfeklieren kunnen ook een verhoogde 18F-FDG opname vertonen als
reactie op de gewrichtsontsteking. Frequent zijn dit de supratrochleaire, axillaire, inguïnale en popliteale lymfeklieren. De CT-component vertoont morfologische veranderingen zoals hydrops en boterosie (29).
Voorbeeld uit eigen studie
Figuur 10: (juveniele) reumatoïde artritis op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: matig verhoogde 18F-FDG opname in
de schouder-, heup-, knie- en enkelgewrichten. Mild verhoogde 18F-FDG opname in de elleboog- en
polsgewrichten. Matig verhoogde 18F-FDG opname bilateraal in de okselklieren en in klier boven de
rechterknie (groene pijlen). (Lever als referentieorgaan)
(B) en (D) coronale PET-beeld en PET/CT-fusiebeeld: matig tot matig intens verhoogde 18F-FDG opname
bilateraal in de schouder-, heup- en kniegewrichten. Matig verhoogde 18F-FDG opname in rechter okselklier
(groene pijl).
(C) coronale CT-beeld in weke delen venster: geen CT-grafische afwijkingen van de gewrichten. Vergrote rechter okselklier (groene pijl).
(E) en (G) coronale PET-beeld en PET/CT-fusiebeeld: mild tot matig verhoogde 18F-FDG opname in de
elleboog-, knie- en enkelgewrichten. Mild verhoogde 18F-FDG opname in het linker polsgewricht.
(F) coronale CT-beeld in weke delen venster: geen CT-grafische afwijkingen. A
B C D
F G
2.5.2.1.2. Spondyloartritis Definitie
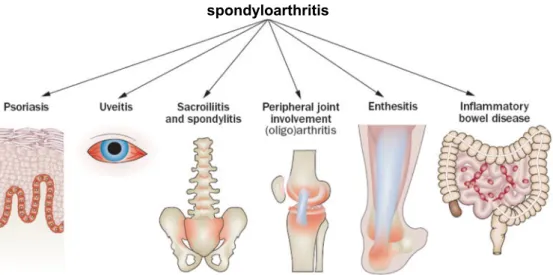
Spondyloartritis (SpA) is een heterogene groep reumatische aandoeningen met gemeenschappelijke klinische kenmerken, maar uiteenlopende fenotypes. Het gaat over de volgende aandoeningen: spondylitis ankylosans (SA), psoriatische artritis (PsA), reactieve artritis (ReA), artritis bij inflammatoir darmlijden en een subgroep van de juveniele idiopathische artritis. Mogelijke klinische manifestaties worden weergegeven in figuur 11 (30).
Figuur 11: mogelijke klinische manifestaties van spondyloartritis (31).
Patiënten met SpA kunnen op basis van hun klinische presentatie in 2 grote categorieën ingedeeld worden: SpA met overwegend axiale aantasting en SpA met overwegend perifere aantasting. De grootste genetische risicofactor om SpA te ontwikkelen is HLA-B27, een MHC-klasse 1 molecule. Gezien de fenotypische diversiteit wordt aangenomen dat ook andere genetische en omgevingsfactoren een bijdrage hebben in deze ziekte (30).
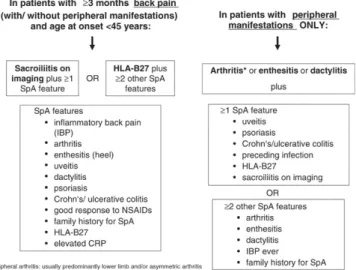
De huidig gebruikte richtlijnen voor de diagnosestelling van SpA zijn de Assessment of SpondyloArthritis international Society (ASAS) criteria. Deze worden weergegeven in figuur 12 (32).
Symptomatisch wordt SpA behandeld met NSAID’s. Indien de therapie continu wordt doorgegeven wordt een vertraging van axiale aantasting bekomen, maar gezien de mogelijke bijwerkingen worden TNF-blokkers eerder als basisbehandeling beschouwd. Deze werken zowel in op de axiale als de perifere aantasting (30).
Figuur 12: gecombineerde weergave van de Assessment of SpondyloArthritis international Society (ASAS)-criteria voor axiale en perifere spondyloartritis (32).
Beeldvorming
Sacroiliitis wordt beschouwd als een specifieke bevinding voor SpA op beeldvorming. Een Rx van het bekken wordt beschouwd als eerste keuze om structurele veranderingen in het gewricht vast te stellen. Indien deze negatief is, kan een sacroiliitis niet uitgesloten worden vermits Rx geen inflammatie kan weergeven. In dit geval wordt een MRI van het bekken uitgevoerd. Deze weergeeft synovitis en subchondraal oedeem van het sacroiliacaal gewricht vooraleer structurele veranderingen optreden (30).
18F-FDG PET/CT-beeldvorming kan niet enkel de metabole en structurele veranderingen van
sacroiliitis aantonen, maar ook hypermetabole activiteit in het tuberositas ischiadicum, trochanter major en processi spinosi. Deze wijzen op enthesitis. Verder kan ook de inflammatie in de wervellichamen beoordeeld worden (33).
Voorbeeld uit eigen studie
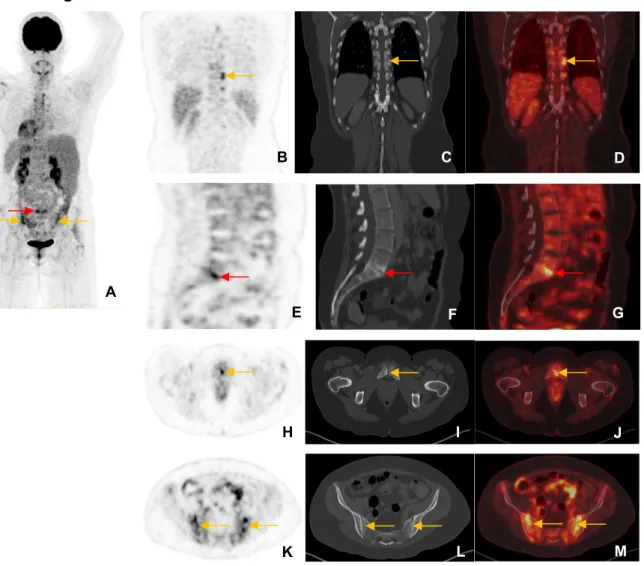
Figuur 13: axiale spondylartropathie op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in postero-anterieure opname: matig verhoogde 18F-FDG opname in
de sacro-iliacale gewrichten (gele pijlen) en tussen L5 en S1 (rode pijl). (Lever als referentieorgaan)
(B) en (D) coronale PET-beeld en PET/CT-fusiebeeld doorheen de costovertebrale gewrichten: matig intens verhoogde 18F-FDG opname ter hoogte van linker costovertebrale gewricht.
(C) coronale CT-beeld doorheen de costovertebrale gewrichten in botvenster: verbening costovertebraal gewricht.
(E) en (G) sagittale PET- en PET/CT-fusiebeeld doorheen de lumbale wervels: matig intens verhoogde 18
F-FDG opname tussen L5 en S1.
(F) sagittale CT-beeld doorheen de lumbale wervels in botvenster: boterosie en verbening van de discus tussen L5 en S1.
(H) en (J) axiale PET-beeld en PET/CT-fusiebeeld doorheen symphisis pubis: matig verhoogde 18F-FDG
opname in de symphisis pubis.
(I) axiale CT-beeld doorheen symphisis pubis in botvenster: boterosie en subchondrale botsclerose.
(K) en (M) axiale PET-beeld en PET/CT-fusiebeeld doorheen bekken: matig intens verhoogde 18F-FDG
opname in sacro-iliacaal gewricht.
(L) axiale CT-beeld doorheen bekken in botvenster: onregelmatige corticale botaflijning van het sacro-iliacaal gewricht. K L M A B E H C D F G I J
2.5.2.1.3. Polymyalgia reumatica Definitie
Polymyalgia reumatica (PMR) is een auto-immuun syndroom dat vrijwel uitsluitend voorkomt boven de 50 jaar. Het wordt gekenmerkt door synovitis ter hoogte van de schouderregio en/of heupgordel. Volgens de 2012 European League Against Rheumatism (EULAR) / American College of Rheumatology (ACR) criteria kan de diagnose PMR gesteld worden bij patiënten ouder dan 50 jaar die zich presenteren met bilaterale schouderpijn die niet verklaard kan worden door een andere oorzaak, met ochtendstijfheid die minstens 45 minuten aanhoudt, verhoogde inflammatoire parameters (CRP en/of BSE) en nieuw ontstane pijn in de heupgordel (34).
Tot maximaal 50% van de patiënten met PMR vertoont ook meer distaal gelegen manifestaties zoals perifere artritis (voornamelijk polsen en knieën) en carpaaltunnelsyndroom (34).
In 5-15% gaat PMR gepaard met reuscelarteritis. Het kan zowel vanaf het begin aanwezig zijn als ontwikkelen tijdens het beloop van PMR. De precieze relatie tussen de twee ziektes is niet gekend. Ook maligniteiten (vooral hematologisch) kunnen schuilgaan achter de klachten die aanvankelijk als PMR beschouwd worden. De kans op een onderliggende maligniteit is groter wanneer PMR zich atypisch manifesteert (<50 jaar, normale BSE, asymmetrische klachten en enkel pijn in arm of been) (20).
De behandeling van PMR bestaat uit orale corticosteroïden (34). Beeldvorming
18F-FDG PET-beeldvorming speelt een belangrijke rol in de diagnosestelling van PMR. De
volgende bevindingen zijn volgens de EANM/SNMMI richtlijnen kenmerkend voor PMR: verhoogde metabole activiteit in peri-articulaire en extra-articulaire synoviale structuren gelegen in schouder- en heupgordel (glenohumeraal synovium, bursa subacromialis en subdeltoïdea, supraspinatus tendinitis en biceps synovitis), kapsels en bursae gelegen rond de kniegewrichten, cervicale en lumbale interspineuze bursae, ischiale bursae en bursae trochanterica. 18F-FDG
PET-beeldvorming kan niet enkel gebruikt voor diagnostiek van PMR, maar ook voor de opvolging van therapierespons (24).
Voorbeeld 1 uit eigen studie
Figuur 14: PMR met grote bloedvaten vasculitis op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: matig verhoogde 18F-FDG opname
bilateraal over het verloop van de A. subclavia, de truncus brachiocephalicus en de A. carotis communis links (rode pijlen). Mild verhoogde 18F-FDG opname in het rechter schoudergewricht en rond de trochanter
major beiderzijds (gele pijlen). (Lever als referentieorgaan)
(B) en (D) sagittale PET-beeld en PET/CT-fusiebeeld doorheen wervelzuil: matig intens verhoogde 18
F-FDG opname rond de lumbale processi spinosi.
(C) sagittale CT-beeld doorheen wervelzuil in weke delen venster: geen CT-grafische afwijkingen.
(E) en (G) axiale PET-beeld en PET/CT-fusiebeeld op schouderniveau: matig verhoogde 18F-FDG opname
in schoudergewrichten.
(F) axiale CT-beeld op schouderniveau in weke delen venster: geen CT-grafische afwijkingen.
(H) en (J) axiale PET-beeld en PET/CT-fusiebeeld op bekken niveau: matig tot matig intens verhoogde 18
F-FDG opname rond de trochanter major beiderzijds.
(I) axiale CT-beeld op bekken niveau in weke delen venster: geen CT-grafische afwijkingen.
(K) en (M) axiale PET-beeld en PET/CT-fusiebeeld op bekken niveau: matig intens verhoogde 18F-FDG
opname rond tuber ischiadicum beiderzijds.
(L) axiale CT-beeld op bekken niveau in weke delen venster: geen CT-grafische afwijkingen.
A B E H K
C
D F G I J L MVoorbeeld 2 uit eigen studie
Figuur 15: PMR met maligniteit en aantasting van perifere gewrichten op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: matig verhoogde 18F-FDG opname ter
hoogte van de schouder-, pols- en heupgewrichten. Intens verhoogde focale 18F-FDG opname ter hoogte
van de linkerborst (rode pijl). (Lever als referentieorgaan)
(B) en (D) coronale PET-beeld en PET/CT-fusiebeeld: mild verhoogde18F-FDG opname ter hoogte van de
schouder- en heupgewrichten.
(C) coronale CT-beeld in weke delen venster: geen CT-grafische afwijkingen.
(E) en (G) axiale thoracale PET-beeld en PET/CT-fusiebeeld: focale matig intens verhoogde 18F-FDG
opname in de linkerborst.
(F) axiale thoracale CT-beeld in weke delen venster bevestigt nodule in linkerborstweefsel.
(H) en (J) axiale PET-beeld en PET/CT-fusiebeeld op schouderniveau: mild verhoogde 18F-FDG opname in
schoudergewricht.
(I) axiale CT-beeld op schouderniveau in weke delen venster: geen CT-grafische afwijkingen.
(K) coronale PET-beeld: mild verhoogde 18F-FDG opname in elleboog- en polsgewrichten, alsook in
handwortelbeenderen rechts. A B E H K C D F G I J
2.5.2.2. Polychondritis recidivans Definitie
Polychondritis recidivans (PR) is een zeldzame aandoening met aantasting van kraakbeen en proteoglycaanrijke structuren (35). Vooral het kraakbeen van de oren, neus, perifere gewrichten en larynx/trachea/bronchiaalboom wordt beschadigd. De proteoglycaanrijke structuren in het oog, binnenoor, bloedvaten en de nieren kunnen ook aangetast worden (29). Mechanische stimuli zoals trauma’s en piercings alsook zwangerschap zijn gekende uitlokkende factoren van PR (35). Het klinisch spectrum kan variëren van intermittente inflammatoire episodes met morfologische vervormingen tot levensbedreigende cardiopulmonale manifestaties zoals valvulaire regurgitatie en luchtwegcollaps. De aandoening is frequent geassocieerd aan andere reumatische en hematologische aandoeningen (35). Het is een traag progressieve ziekte met episodes van opflakkering en remissie, met als gevolg vervorming en vernietiging van kraakbeen (29).
De diagnose wordt meestal gesteld op basis van klinische bevindingen. Respiratoire symptomen zoals hoesten, heesheid en pijn in de proximale trachea en larynx karakteriseren frequent het begin van PR (35).
Op biopsie is er geen enkel pathognomonisch kenmerk voor PR. Wel kan granulatieweefsel en beschadiging van de kraakbeenarchitectuur vastgesteld worden (36).
Milde manifestaties worden behandeld met NSAID’s / dapsone / colchicine. In geval van ernstige manifestaties bestaat de behandeling uit corticosteroïden (35).
Beeldvorming
18F-FDG PET-beeldvorming representeert actieve chondritis en kan bijdragen tot een vroege
diagnosestelling van de ziekte. Het unieke patroon van 18F-FDG opname in de kraakbeenstructuren
Voorbeeld uit eigen studie
Figuur 16: polychondritis recidivans op 18F-FDG PET/CT-beeldvorming.
(A) en (B) 18F-FDG totaal lichaam PET-beeld in anteroposterieure en
profielopname: matig tot matig intens verhoogde 18F-FDG opname over
het verloop van de trachea (gele pijl) en het ribkraakbeen van verschillende ribben beiderzijds (blauwe pijl). (Lever als referentieorgaan) (C) en (E) coronale PET-beeld en PET/CT-fusiebeeld op niveau van het sternum en ribben: mild tot matig intens verhoogde 18F-FDG opname over
het verloop van het ribkraakbeen van verschillende ribben beiderzijds. (D) coronale CT-beeld op niveau van het sternum en ribben in weke delen venster: geen CT-grafische afwijkingen van ribkraakbeen.
(F) en (H) coronale PET-beeld en PET/CT-fusiebeeld doorheen trachea: matig intens verhoogde 18F-FDG opname rond de trachea.
(G) coronale CT-beeld doorheen trachea in weke delen venster: indruk van tracheale wandverdikking.
2.5.2.3. Inflammatoir darmlijden Definitie
Inflammatoir darmlijden (IBD) is gedefinieerd als een chronische intestinale inflammatie ten gevolge van een gestoorde gastheer-microbiële interactie. Zowel de dunne als de dikke darm kunnen hierbij aangetast worden. De 2 grote subtypes van IBD zijn de ziekte van Crohn (ZC) en colitis ulcerosa (CU); kenmerken hiervan worden opgesomd in tabel 4. Beide ziektes hebben een vergelijkbare beginleeftijd met een piekincidentie tussen de 20 en 40 jaar. De exacte etiologie van IBD is niet gekend, maar er wordt aangenomen dat een combinatie van de volgende elementen het ontstaan kan triggeren: genetische predispositie (meer dan 150 susceptibele genloci zijn
A B C F D E G H J
ondertussen gekend), een gedysreguleerd immuunrespons op een verandering van het darm microbioom en omgevingsfactoren (bijvoorbeeld stress en roken) (37). De diagnose wordt gesteld op basis van de kliniek, biochemie, stoelgangstaal, ileocoloscopie, histologie en beeldvorming (38). Hoewel beide ziektes op dezelfde manier gediagnosticeerd worden, vereisen ze elk een aparte en individuele therapie (tabel 4). Slechts wanneer de medicamenteuze behandeling faalt, kan eventueel overgegaan worden tot een chirurgische ingreep (37-39).
Tabel 4: kenmerken van de ziekte van Crohn en colitis ulcerosa (CU).
Ziekte van Crohn Colitis ulcerosa
Localisatie van aantasting Gehele digestieve tractus Voornamelijk colon (meestal rectum het ergst aangetast) Meest voorkomende
symptomen Pijn laag in rechterabdomen, zwelling van de buik Pijn laag in het linker abdomen, diarree, gewichtsverlies, bloed in stoelgang
Endoscopische bevindingen
Discontinue laesies, lineaire ulceraties
Continue laesies, crypten, verdikking van de mucosa Aantasting op
microscopisch niveau Transmurale inflammatie met aanwezigheid van granulomen en een abnormale
cryptarchitectuur
Mucosale en submucosale inflammatie met aggregatie van granulocyten
Behandeling Milde tot matige ziekte activiteit: orale glucocorticoïden
Ernstige ziekte activiteit: immunosuppressiva en biologicals
Milde tot matige ziekte activiteit: 5-aminosalicylaten
Ernstige ziekte activiteit: orale glucocorticoïden
Indien refractair aan reeds opgenoemde behandeling: anti-TNF
Beeldvorming
De 2018 European Crohn’s and Colitis Organisation (ECCO) en European Society of Gastrointestinal and Abdominal Radiology (ESGAR) richtlijnen stellen dat beeldvorming dient uitgevoerd te worden bij alle nieuw gediagnosticeerde patiënten met IBD. Echografie, CT en MRI worden het meest gebruikt om de uitgebreidheid en ziekte activiteit in de darm te beoordelen. Morfologische kenmerken zijn wandverdikking en een verhoogde contrastcaptatie in de darmwand (38). 18F-FDG PET-beeldvorming is een alternatief onderzoek waarop de uitgebreidheid en ernst
van de inflammatie alsook de therapierespons kunnen beoordeeld worden. 18F-FDG opname is
parallel met de infiltratie van immunologische cellen in de darmwand. De CT-component staat in voor de morfologische beoordeling van de darm (40, 41).
Voorbeeld uit eigen studie
Figuur 17: ziekte van Crohn op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: intens verhoogde 18F-FDG opname over
het verloop van het distaal ileum (rode pijl). Intens verhoogde multifocale fysiologische 18F-FDG opname in
bruin vetweefsel bilateraal in de hals, mediastinaal en axillair (blauwe pijl). (Lever als referentieorgaan) (B) en (D) coronale PET-beeld en PET/CT-fusiebeeld: intens verhoogde 18F-FDG opname over het verloop
van het distaal ileum (rode pijl). Matig intens tot intens verhoogde fysiologische 18F-FDG opname in het bruin
vetweefsel in de hals (blauwe pijl).
(C) coronale CT-beeld in weke delen venster: wandverdikking van het distaal ileum (rode pijl). Beeld bevestigt dat 18F-FDG opname zich situeert in het bruin vetweefsel in de hals (blauwe pijl).
2.5.2.4. Longen
2.5.2.4.1. Interstitieel longlijden Definitie
Interstitiële longaandoeningen zijn een groepering van meer dan 200 diffuse parenchymale longziekten die inflammatie en irreversibele verlittekening veroorzaken van het longparenchym, longfibrose genoemd (42). De verschillende subtypes zijn onderverdeeld in enkele categorieën, weergegeven in figuur 18. De symptomen en het ziekteverloop variëren van persoon tot persoon, maar inflammatie is een gemeenschappelijk begin van al deze aandoeningen. De meest voorkomende symptomen zijn: hoest, wheezing, haemoptoe, dyspnoe (zeker bij inspanning), anorexie en gewichtsverlies (43).
Figuur 18: overzicht van de categorieën van interstitiële longaandoeningen (42).
AIP, acute interstitial pneumonia; COP, cryptogenic organizing pneumonia; CTD, connective tissue disease; DAH, diffuse alveolar hemorrhage; DIP, desquamative interstitial pneumonia; IPF, idiopathic pulmonary fibrosis; NSIP, nonspecific interstitial pneumonia; PM/DM, polymyositis/dermatomyositis; RA, rheumatoid arthritis; RB-ILD, respiratory bronchiolitis-associated interstitial lung disease.
De diagnose wordt gesteld op basis van klinische bevindingen, longfunctiemetingen en beeldvorming (Rx en HRCT). Indien hierna de diagnose niet duidelijk is, kan overgegaan worden tot broncho-alveolaire lavage en transbronchiale longbiopsie (43).
De behandeling is individueel te bepalen en is afhankelijk van het onderliggende subtype van interstitieel longlijden. Er wordt een rookstop geadviseerd aan alle rokende patiënten. Wanneer de longaantasting te uitgebreid wordt, is een longtransplantatie noodzakelijk (43).
Beeldvorming
Rx en HRCT worden gebruikt voor de diagnosestelling van interstitieel longlijden (43). 18F-FDG
PET-beeldvorming weergeeft de inflammatoire zones van het longparenchym. Vermits de inflammatie voorafgaat aan fibrosevorming, kan verergering van de ziekte activiteit waargenomen worden op 18F-FDG PET-beeldvorming vooraleer morfologische veranderingen te zien zijn op
Voorbeeld uit eigen studie
Figuur 19: respiratoire bronchiolitis - interstitiële longaandoening op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: matig tot matig intens verhoogde focale 18F-FDG opname in beide longen (rode pijl). Mild tot matig verhoogde fysiologische 18F-FDG opname over
het verloop van de tussenribspieren beiderzijds (blauwe pijlen).
(B) en (D) axiale thoracale PET-beeld en PET/CT-fusiebeeld: matig intens verhoogde focale 18F-FDG
opname in beide longen (rode pijl).
(C) axiale thoracale CT-beeld in longvenster bevestigt dat 18F-FDG opname overeenkomt met
matglasverdichtingen in beide longen.
(E) en (G) axiale thoracale PET-beeld en PET/CT-fusiebeeld: mild tot matig verhoogde 18F-FDG opname in
beide longen.
(F) axiale thoracale CT-beeld in longvenster bevestigt dat 18F-FDG opname zich nodulair bevindt in beide
longen.
2.5.2.4.2. Sarcoïdose Definitie
Sarcoïdose is een systemische aandoening gekenmerkt door vorming van immuungemedieerde granulomen in verscheidene organen. De longen en de lymfeklieren worden het meest aangetast, maar in 30-50% zijn ook andere organen betrokken. Enkele voorbeelden zijn het hart, de huid, de ogen, de lever en milt (figuur 20). De precieze oorzaak van de aandoening is niet gekend. Studies tonen aan dat het mogelijk een overdreven granulomateuze reactie is op blootstelling aan niet-geïdentificeerde antigenen (45). A B E C D F G
Figuur 20: symptomen en ziektetekenen van sarcoïdose (46).
De diagnose wordt gesteld aan de hand van de kliniek, bevindingen op beeldvorming en een histologische bevestiging van granulomen. De piekincidentie is tussen de 25 en 45 jaar en bij vrouwen ouder dan 50 jaar. In meer dan de helft van de gevallen verdwijnt de ziekte spontaan binnen de 5 jaar. De behandeling van sarcoïdose bestaat uit corticosteroïden (45).
Beeldvorming
Op beeldvorming kenmerkt sarcoïdose zich meest frequent door bilaterale hilaire lymfadenopathieën of diffuse micronodulaire infiltraties in de longen. 18F-FDG PET-beeldvorming
weergeeft de inflammatoire activiteit. In tegenstelling tot de conventionele radiografie van de longen kan hier ook de extrapulmonale manifestatie van de ziekte beoordeeld worden. Dit onderzoek wordt zowel gebruikt voor de diagnosestelling als voor de opvolging van therapierespons. Indien een koolhydraatarm dieet wordt gevolgd als voorbereiding op 18F-FDG
Voorbeeld uit eigen studie
Figuur 21: sarcoïdose op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: mild tot matig verhoogde focale 18
F-FDG opname in beide longen (gele pijl). (Matig) intens verhoogde focale 18F-FDG opname in beide longhili
(groene pijlen), milt (blauwe pijl) en net onder de lever (paarse pijl). (Lever als referentieorgaan)
(B) en (D) axiale thoracale PET-beeld en PET/CT-fusiebeeld: matig verhoogde multifocale 18F-FDG opname
in beide longen.
(C) axiale thoracale CT-beeld in longvenster bevestigt dat 18F-FDG opname overeenkomt met diffuus
verspreide polylobulaire tot spiculair begrensde longnoduli.
(E) en (G) axiale thoracale PET-beeld en PET/CT-fusiebeeld: matig intens verhoogde 18F-FDG opname ter
hoogte van beide longhili.
(F) axiale thoracale CT-beeld in weke delen venster bevestigt dat 18F-FDG opname zich situeert in vergrote
lymfeklieren.
(H) en (J) axiale abdominale PET-beeld en PET/CT-fusiebeeld: (matig) intens verhoogde focale 18F-FDG
opname in de milt.
(I) axiale abdominale CT-beeld in weke delen venster bevestigt dat 18F-FDG opname zich bevindt in een
hypodens letsel in de milt.
(K) en (M) axiale abdominale PET-beeld en PET/CT-fusiebeeld: (matig) intens verhoogde 18F-FDG opname
tussen pancreaskop en het duodenum.
(L) axiale abdominale CT-beeld in weke delen venster bevestigt dat de 18F-FDG opname zich situeert in een
vergrote klier tussen de pancreaskop en het duodenum. A B E H K C D F G I J L M
2.5.3. Tumorkoorts Definitie
Neoplastische koorts, ook gekend als tumorkoorts is een paraneoplastisch verschijnsel veroorzaakt door de kanker zelf. Het komt vaak voor bij Hodgkin en niet-Hodgkin lymfomen, sarcomen, acute/chronische leukemieën en renaalcelcarcinomen, maar kan feitelijk bij elke kanker voorkomen (47).
Voorbeeld 1 uit eigen studie
Figuur 22: gemetastaseerd melanoom op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: mild verhoogde focale 18F-FDG opname
in de rechterlong (paarse pijl). Matig intens tot intens verhoogde focale 18F-FDG opname in rib links (rode
pijl), lever (blauwe pijl), multipele klieren (groene pijl) en in de proximale femur rechts en links (gele pijl). (B) 18F-FDG totaal lichaam PET-beeld in postero-anterieure opname vertoont bijkomend intens verhoogde 18F-FDG opname in multipele wervels (gele pijl).
(C) en (E) axiale thoracale PET-beeld en PET/CT-fusiebeeld: mild verhoogde focale 18F-FDG opname in de
rechterlong (paarse pijl). Matig intens verhoogde 18F-FDG opname in de linkerscapula (bruine pijl). Intens
verhoogde 18F-FDG opname in wervelcorpus (gele pijl).
(D) axiale thoracale CT-beeld in longvenster: bevestigt dat 18F-FDG opname zich situeert in nodule in
rechterlong. Beeld vertoont werveldestructie (gele pijl). A B C F I L D E G H J K M N
(F) en (H) axiale abdominale PET-beeld en PET/CT-fusiebeeld: matig tot intens verhoogde focale 18F-FDG
opname in de lever.
(G) axiale abdominale CT-beeld in weke delen venster: multipele hypodense leverletsels (discrepantie tussen het aantal visualiseerbare leverletsels op PET en CT).
(I) en (K) axiale abdominale PET-beeld en PET/CT-fusiebeeld: intens verhoogde focale 18F-FDG opname
aan leverhilus.
(J) axiale abdominale CT-beeld in weke delen venster bevestigt dat 18F-FDG opname zich situeert in een
vergrote lymfeklier aan leverhilus.
(L) en (N) coronale PET-beeld en PET/CT-fusiebeeld doorheen proximale femur: intens verhoogde 18F-FDG
opname in de rechter proximale femur.
(M) coronale CT-beeld doorheen proximale femur in botvenster: bevestigt dat 18F-FDG opname zich situeert
ter hoogte van een lytische botmetastase in de rechter proximale femur.
Voorbeeld 2 uit eigen studie
Figuur 23: Hodgkin lymfoom op 18F-FDG PET/CT-beeldvorming.
(A) 18F-FDG totaal lichaam PET-beeld in anteroposterieure opname: (matig) intens verhoogde 18F-FDG
opname in mediastinale (groene pijl), parasternale (gele pijl), hilaire en abdominale klieren. Algemeen matig verhoogd 18F-FDG metabolisme in milt met multipele foci van matig intens verhoogde 18F-FDG opname (rode
pijl).
(B) en (D) axiale thoracale PET-beeld en PET/CT-fusiebeeld: intens verhoogde focale 18F-FDG opname
intertracheocavaal (groene pijl) en parasternaal (gele pijl).
(C) thoracale axiale CT-beeld in weke delen venster: bevestigt dat 18F-FDG opname zich bevindt in vergrote
lymfeklieren intertracheocavaal (groene pijl) en ter hoogte van de A. mammaria interna (gele pijl).
(E) en (G) abdominale axiale PET-beeld en PET/CT-fusiebeeld: intens verhoogde 18F-FDG opname in de
milt (rode pijl). (Matig) intens verhoogde 18F-FDG opname in multipele foci abdominaal (blauwe pijl) en
retroperitoneaal rechts van wervelcorpus (groene pijl).
(F) abdominale axiale CT-beeld in weke delen venster bevestigt dat 18F-FDG opname abdominaal en
retroperitoneaal zich situeert in lymfeklieren (respectievelijk blauwe en groene pijl). Geen CT-grafische afwijkingen in de milt. A B E C D F G
2.6. Vraagstelling
Het doel van de scriptie is exploratief van aard voor wat de meerwaarde van 18F-FDG hybride
PET/CT-beeldvorming betreft bij patiënten met koorts/inflammatie van onbekende oorsprong. Zo wordt onderzocht welke diagnostische bijdrage dit onderzoek levert in een studiepopulatie op het UZ Gent. Er wordt ook gekeken hoe deze resultaten zich verhouden ten opzichte van de literatuur. Verder zal dieper ingegaan worden op de verschillende entiteiten van aseptische inflammatie.
3. Methodologie
3.1. Patiëntengroep
Deze scriptie is een monocentrisch prospectief onderzoek uitgevoerd in het Universitair Ziekenhuis Gent en goedgekeurd door de Commissie voor Medische Ethiek. De dataverzameling omvat alle patiënten die tussen 06/09/2018 en 31/06/2019 verwezen werden voor 18F-FDG hybride
PET/CT-beeldvorming op de dienst nucleaire geneeskunde in het kader van koorts/inflammatie van onbekende oorsprong.
Volgende patiënten werden opgenomen in de studie:
- patiënt heeft een 18F-FDG PET/CT-onderzoek ondergaan met als verwijzingsreden
infectie/inflammatie
- patiënt heeft een akkoordverklaring ondertekend waarbij de student toestemming krijgt om het medisch dossier en het 18F-FDG PET/CT-onderzoek in te kijken
De volgende exclusiecriteria werden gehanteerd:
- definitie van klassieke koorts (volgens Durack en Street) / inflammatie van onbekende oorsprong (volgens Vanderschueren) is niet voldaan
- nosocomiale koorts, neutropene koorts, HIV-geassocieerde koorts - te weinig data gerapporteerd in het EPD
- lost to follow-up
Het medisch dossier van elke geïncludeerde patiënt werd nagekeken en volgende elementen werden weerhouden:
- Medische voorgeschiedenis, anamnese, maligniteit (max. 6 maanden voor het 18F-FDG
PET/CT-onderzoek), chirurgie of invasieve procedures (max. 3 maanden voor het 18F-FDG
PET/CT-onderzoek), inflammatoire markers (C-reactief proteïne (CRP),
bloedbezinkingssnelheid van erythrocyten (BSE)), hemoglobine, leukocyten, bloedplaatjes, maximumwaarde van de koorts (hoger of lager dan 38.3°C), duur van de koorts/inflammatie, reeds uitgevoerde onderzoeken, bevestigend onderzoek voor de diagnosestelling en de finale diagnose.
De labowaarden met het kleinste tijdsinterval voor het 18F-FDG PET/CT-onderzoek werden
gebruikt.
Om te voldoen aan de definitie van inflammatie van onbekende oorsprong, moest minstens 1 inflammatoire marker verhoogd zijn. Hiervoor werd gekeken naar de referentiewaarden die gehanteerd worden in het UZ Gent.
Afwijkende waarden zijn:
- CRP >5 mg/L
- Bloedbezinkingssnelheid:
Man jonger dan 50 jaar: >15 mm/u Man ouder dan 50 jaar: >20 mm/u Vrouw jonger dan 50 jaar: >20 mm/u Vrouw ouder dan 50 jaar: >30 mm/u
3.2. 18F-FDG PET/CT-beoordeling
De 18F-FDG PET/CT-onderzoek vond plaats op de dienst nucleaire geneeskunde in het UZ Gent.
Er was geen vast tijdstip in de uitwerking van koorts/inflammatie van onbekende oorsprong waarop de patiënten verwezen werden voor 18F-FDG PET/CT-beeldvorming.
De gebruikte hybride PET/CT-toestellen waren samengesteld uit een TOF-PET en een spiraal CT. De 18F-FDG PET-beelden werden visueel beoordeeld door een nucleair geneeskundige. De
opname van 18F-FDG werd als afwijkend beschouwd indien deze ter hoogte van de afwijking
heterogeen én groter of gelijk was aan de 18F-FDG opname in het referentieorgaan (lever of
mediastinum). Er werd geen semikwantitatieve analyse toegepast. De CT-beelden werden geanalyseerd door een radioloog.
Hierna volgde telkens een stafvergadering waarbij de bevindingen overlegd werden door beide partijen en waarbij de beelden gecoregistreerd geanalyseerd werden.
3.3. Finale diagnose
Voor deze studie werd de informatie betreffende de finale diagnose bekomen uit het EPD van de patiënt. De diagnose was telkens gebaseerd op de resultaten van het klinisch onderzoek, biochemie, beeldvorming en bevestigende onderzoeken (biopsie / exploratieve ingreep / klinische follow-up (≥3 maand) / respons op tentatieve behandeling…). Enkel diagnoses die maximaal 4 maanden na de 18F-FDG PET/CT-beeldvorming bekomen waren, werden opgenomen in de studie.
De finale diagnose werd ingedeeld in 1 van de volgende diagnostische groepen: - Niet-infectieuze inflammatoire aandoening (NIIA)
- Infectie - Maligniteit
3.4. Vergelijking van het 18F-FDG PET/CT-resultaat versus de finale diagnose
Het 18F-FDG PET/CT-onderzoek werd telkens ingedeeld in 1 van de 4 volgende categorieën, naar
analogie met recente literatuur (48-56).
- Terecht positief (TP): de afwijkende bevindingen werden door verdere diagnostische onderzoeken / klinische follow-up / respons op behandeling bevestigd als oorzaak van de koorts/inflammatie.
- Vals positief (VP): de afwijkende bevindingen waren niet gecorreleerd met de koorts/inflammatie.
- Terecht negatief (TN): er waren geen afwijkende bevindingen en verdere diagnostische onderzoeken / klinische follow-up (≥3 maand) brachten geen onderliggende aandoening aan het licht.
- Vals negatief (VN): er waren geen afwijkende bevindingen, maar de etiologie van de koorts/inflammatie werd uiteindelijk bevestigd aan de hand van andere diagnostische onderzoeken / klinische follow-up / respons op behandeling.
3.5. Bijdrage van 18F-FDG PET/CT-beeldvorming in de diagnostische uitwerking
Om de bijdrage van 18F-FDG PET/CT-beeldvorming in de diagnostische uitwerking van
koorts/inflammatie van onbekende oorsprong weer te geven werd de sensitiviteit, specificiteit en de diagnostische accuraatheid berekend. Deze werd vergeleken met resultaten uit de recente literatuur (voor volledig overzicht zie tabel 5).
Tabel 5: recente literatuur over de bijdrage van 18F-FDG PET/CT-beeldvorming in de uitwerking van koorts/inflammatie van onbekende oorsprong.
Auteur Jaar a Studie design Inclusie
periode Aantal patiënten Land Koorts / inflammatie Definitie Sens b (%) Spec c (%) Diagnostische accuraatheid (%) Garcia-Vicente AM, et al.
2018 retrospectief 2007-2015 67 Spanje koorts en inflammatie
koorts: temp. >38.3°C gedurende >3 weken, oorzaak niet gekend na 1 week hospitalisatie inflammatie: alle criteria van koorts, maar temp. <38.3°C
84 31 61
Schönau
V, et al. 2018 prospectief 2007-2015 240 Duitsland koorts en inflammatie koorts: temp. >38.3°C gedurende >3 weken, oorzaak niet gekend na uitgebreide diagnostische uitwerking
inflammatie: temp. <38.3°C, CRP >7 mg/L en/of BSE d >leeftijd/2 bij mannen of >(leeftijd+10)/2 bij
vrouwen gedurende >3 weken; oorzaak niet gekend na diagnostische uitwerking
91 22 65
Hung
B.-T, et al. 2017 retrospectief 2013-2016 58 Taiwan koorts definitie volgens Durack en Street 79 56 72 Pereira
AM, et al
2016 retrospectief 2006-2012 76 Zwitserland koorts minstens 2 metingen met temp. >38.3°C; duur van ziekte is minstens 3 weken
77 31 60 Balink H, et al. 2015 retrospectief (patiëntendata van 3 reeds gepubliceerde studies gebruikt) studie 1: 2000-2010 studie 2: 2005-2012 studie 3: 2005-2008 498 Nederland koorts en inflammatie
studie 1: patiënten met grote bloedvaten vasculitis als klinische vraagstelling bij verwijzing naar 18
F-FDG PET/CT-onderzoek
studie 2 (inflammatie): CRP >20 mg/L en/of BSE >20 mm/u, temp. <38.3°C op verschillende metingen. Duur niet gespecifieerd. Geen oorzaak gekend na diagnostische uitwerking
studie 3 (koorts): langdurige koorts >38.3°C, duur niet gespecifieerd. Geen diagnose na hospitalisatie of ambulante uitwerking
89 89 89
Gafter-Gvili A, et al.
2015 retrospectief 2008-2012 112 Israël koorts definitie volgens Durack en Street 72 58 66
Buch-Olsen KM, et al.
2014 retrospectief 2010-2011 57 Denemarken koorts niet beschreven 95 29 75
Tokmak H, et al.
2014 retrospectief 2008-2012 21 Turkije koorts koorts: temp. >38°C gedurende >3 weken, oorzaak niet gekend na 1 week hospitalisatie of ambulante uitwerking
94 80 91
Manohar K, et al.
2013 retrospectief NR e 103 India koorts koorts: temp. >38.3°C gedurende >3 weken,
oorzaak niet gekend na 1 week hospitalisatie of ambulante uitwerking
90 97 83
3.6. Statistische analyse
De statistische analyse werd uitgevoerd aan de hand van SPSS-software (IBM SPSS Statistics 25 voor Windows).
Om de basiskarakteristieken van data weer te geven werd een descriptieve statistische analyse uitgevoerd op de numerieke variabelen en een frequentie analyse op de categorische variabelen. De waarden worden respectievelijk gerapporteerd als gemiddelde ± standaardafwijking (SD) en als frequenties met percentages.