DE VROEGTIJDIGE RESULTATEN VAN
HEROPERATIES AAN DE AORTAKLEP
Laurent De Backer
Stamnummer: 01408154Promotor: Prof. Dr. Katrien François
Masterproef voorgelegd in het kader tot het behalen van de graad Master of Medicine in de Geneeskunde
Inhoudsopgave
Abstract ... 1 Doel ... 1 Methode ... 1 Resultaten ... 1 Conclusie ... 1 Inleiding ... 3Anatomie en fysiologie van de aortaklep ... 3
Pathologie van de aortaklep ... 3
Aortaklepstenose ... 3
Aortaklepregurgitatie ... 4
Indicaties voor aortaklepvervanging ... 4
Aortaklepstenose ... 5
Aortaklepregurgitatie ... 6
Risicofactoren bij aortaklepvervanging ... 7
Prothesetypes bij aortaklepvervanging ... 8
Resultaten van primaire SAVR ... 8
Resultaten van primaire chirurgische operaties in de literatuur... 9
TAVR tegenover SAVR ... 9
Heroperatie aan de aortaklep ... 10
Reden voor heroperatie na SAVR/TAVR ... 10
Timing van heroperatie ... 11
Resultaten van chirurgische heroperaties in de literatuur ... 11
TAVR als heroperatie ... 15
Besluit ... 16
Doel van de studie ... 16
Methode en patiënten ... 17 Methode literatuurstudie ... 17 Studiepopulatie ... 17 Statistische analyse ... 17 Resultaten ... 19 Preoperatieve parameters ... 19 Preoperatieve patiëntkarakteristieken ... 19
Preoperatieve echocardiografische parameters ... 21
Parameters vorige operatie ... 22
Parameters heroperatie ... 23
Indicaties voor heroperatie ... 23
Interval tussen ingrepen ... 24
Operatieve en intra-procedurele parameters van de heroperatie ... 25
Vroeg postoperatieve parameters ... 28
Vroeg postoperatieve interventies en complicaties ... 28
Hospitalisatie en mortaliteit ... 30
Ontslag uit het ziekenhuis ... 30
2 maand tot 1 jaar postoperatief ... 31
Statistische analyses ... 32
Discussie ... 35
Patiëntkarakteristieken ... 35
Mortaliteit ... 35
Morbiditeit ... 39
Beperkingen van de studie ... 40
Conclusie ... 41
Referenties ... 42
Afkortingen en acroniemen ... 1
Appendix ... 3
Deze pagina is niet beschikbaar omdat ze persoonsgegevens bevat.
Universiteitsbibliotheek Gent, 2021.
This page is not available because it contains personal information.
Ghent University, Library, 2021.
Voorwoord
Na een intensief proces van ongeveer anderhalf jaar is het eindelijk zo ver. Ik leg de laatste hand aan mijn thesis.
Ik zou vooraf graag nog enkele personen willen bedanken die mij het afgelopen anderhalf jaar gesteund en geholpen hebben. In het bijzonder wil ik Prof. Dr. François, de promotor van deze thesis, bedanken. Zij stond steeds paraat om mijn vragen te beantwoorden en gaf constructieve feedback op mijn tussentijdse versies. Deze feedback motiveerde me om verder te gaan en het beste uit mezelf te halen. Het klinkt misschien cliché maar Prof. Dr. François is het soort arts waar ik naar opkijk: professioneel, gedreven en immer bereid om zowel collega’s als patiënten als studenten hulp en oplossingen te bieden.
Ook zou ik graag mijn familie, vriendin en vrienden willen bedanken om mij door dik en dun te steunen. Ik ben enorm dankbaar dat zij er voor mij zijn. In het bijzonder wil ik mijn vader, Yves, en mijn vriendin, Jana, bedanken om mij te helpen bij het overlezen van deze thesis. Ik hoop dan ook dat ik vooral hen trots maak.
Tijdens het schrijven van deze thesis heb ik ontzettend veel bijgeleerd, zowel op wetenschappelijk als op individueel vlak. Het onderwerp van deze thesis, namelijk chirurgie aan de aortaklep, sprak mij vanaf het begin aan. Ik keek er dan ook naar uit meer te weten te komen over deze complexe chirurgie.
Vanaf de start was ik bereid tot het uiterste te gaan en van plan deze thesis tot een goed, in mijn ogen zelfs tot het best mogelijke einde te brengen. Laat er geen twijfel over bestaan dat deze thesis mij op heel wat momenten deed twijfelen aan mijzelf, mijn capaciteiten, mijn kennis, mij irriteerde en mij zelfs tot slapeloze nachten dwong. Toch zie ik achteraf dat het vele werk het allemaal meer dan waard was en presenteer ik u, de lezer, met trots het afgewerkte resultaat.
Abstract
Doel
Deze studie zal de vroege postoperatieve resultaten van heroperaties aan de aortaklep, uitgevoerd binnen het UZ Gent, in beeld proberen brengen. Er zal voornamelijk gefocust worden op de vroeg postoperatieve mortaliteit en morbiditeit. Ook zal aan de hand van analyse gezocht worden naar risicofactoren die voorspellend zijn voor de vroeg postoperatieve mortaliteit en morbiditeit.
Methode
Honderdeenendertig patiënten die een heroperatie aan de aortaklep ondergingen binnen het UZ Gent werden in deze studie geïncludeerd. Patiënten ondergingen deze heroperatie in de periode van 01/01/2000 tot 10/06/2018. Univariabele en multivariabele analyses werden uitgevoerd om de risicofactoren voor vroege postoperatieve mortaliteit en morbiditeit in beeld te brengen.
Resultaten
Elf patiënten overleden vroeg postoperatief. De ziekenhuismortaliteit en dertigdagenmortaliteit waren beiden 8,4%. De voornaamste complicaties die optraden bij heroperatie aan de aortaklep waren: hartritmestoornissen bij 45 (34,4%) patiënten, voornamelijk VKF bij 34 (26,0%) patiënten, ANI bij 33 (25,2%) patiënten, pulmonale complicaties bij 21 (16,0%) patiënten en bloedingen eveneens bij 21 (16,0%) patiënten. De mediane hospitalisatieduur was 44 dagen voor endocarditis en 13 dagen voor andere indicaties (p < 0,05). Univariabele analyse toonde een associatie tussen een lagere preoperatieve creatinineklaring (p = 0,002), NYHA-klasse IV (p = 0,015), hogere EuroSCORE II (p = 0,006), een geassocieerde CABG (p = 0,025) en een hogere piekgradiënt over de aortaklep (p = 0,025) en de dertigdagenmoraliteit. Eveneens werd een associatie aangetoond tussen klependocarditis en langdurige postoperatieve beademing (p = 0,042).
Conclusie
De vroege postoperatieve mortaliteit binnen onze studie was vergelijkbaar met die terug te vinden in de literatuur, rekening houdende met de verschillen in inclusie- en exclusiecriteria bij andere studies in vergelijking met de onze. Risicofactoren beschreven in de literatuur kwamen terug. Lagere preoperatieve creatinineklaring, NYHA-klasse IV, geassocieerde CABG, hogere EuroSCORE II en hogere piekgradiënt over de aortaklep konden significant (p < 0,05) geassocieerd worden aan de dertigdagenmortaliteit.
Verder is er nog nood aan bijkomend multicentrisch prospectief onderzoek onder de vorm van studies die alle vormen van heroperatie aan de aortaklep includeren. Zo bekomt men studiepopulaties die dichter aansluiten bij de patiëntenpopulatie die zich in het ziekenhuis
presenteert voor heroperatie aan de aortaklep en kan men de real-life vroege postoperatieve moraliteit voor deze patiënten beter inschatten.
Inleiding
Anatomie van de aortaklep
Een goede kennis van de anatomie van de aortaklep is belangrijk bij zowel vervanging als herstel van de aortaklep. De anatomische kennis van de chirurg leidt immers tot een betere chirurgische uitvoering van de correcte positionering van een aortaklepprothese in de aortawortel met respect voor de omliggende structuren zoals de coronaire arteriën, de mitralisklep en het geleidingsweefsel van het hart. Zo kan men beschadiging van deze structuren, wat kan leiden tot postoperatieve complicaties, zoveel mogelijk vermijden. (1)
De aortaklep heeft normalerwijze een tricuspide morfologie. Dit wil zeggen dat de aortaklep uit drie klepblaadjes bestaat, die mooi op elkaar aansluiten en bijgevolg de doorgang vanuit het hart naar de aorta goed kunnen afsluiten. Een frequent voorkomende anatomische variant hierop is een aortaklep met bicuspide morfologie. Hierbij bestaat de aortaklep slechts uit 2 klepblaadjes, die meestal minder mooi op elkaar aansluiten. Hierdoor vormt een aortaklep met bicuspide morfologie een belangrijke risicofactor voor vroegtijdige aortaklepinsufficiëntie. (1)
Pathologie van de aortaklep
De voornaamste oorzaken van aortakleppathologie zijn aortaklepstenose, aortaklepregurgitatie en reumatisch hartkleplijden. Reumatisch hartkleplijden komt in Westerse landen bijna niet meer voor. Het komt wel nog endemisch voor in derdewereldlanden. (2)
Met een incidentie van ongeveer 1% in de Verenigde Staten symboliseert aortakleppathologie een belangrijke ziektelast, voornamelijk bij oudere personen. (3)
Aantonen van een valvulaire hartziekte (VHD) zoals een aandoening ter hoogte van de aortaklep, gebeurt het best met behulp van echocardiografie na een doelmatige klinische evaluatie. Met behulp van echocardiografie kan men immers de linkerventrikelfunctie en een eventuele klepcalcificatie inschatten. (2)
Op de echocardiografische criteria voor het vaststellen van ernstige klepstenose of klepregurgitatie zal in deze studie niet verder worden ingegaan, maar deze zijn terug te vinden in de European Society of Cardiology (ESC)/ European Association for Cardio-Thoracic Surgery (EACS) richtlijnen van 2017 voor de aanpak van VHD. (2)
Aortaklepstenose
Aortaklepstenose is in Europa en Noord-Amerika de voornaamste oorzaak van primair aortakleplijden. De prevalentie is de laatste jaren sterk toegenomen door de vergrijzing van de bevolking. (2)
In de American Heart Association (AHA)/ American College of Cardiology (ACC) richtlijnen van 2014 voor VHD (4) wordt aortaklepstenose onderverdeeld in 4 verschillende stadia. Deze stadia gaan van aortaklepstenose (stadium A), aortaklepstenose met hemodynamische obstructie (stadium B), ernstig asymptomatische aortaklepstenose (stadium C) tot symptomatische aortaklepstenose (stadium D). Elk van deze stadia geeft kenmerkende symptomen bij de patiënt en heeft een typische klepanatomie en klephemodynamica. De klepobstructie geeft bovendien ook specifieke complicaties ter hoogte van het linkerventrikel en ter hoogte van de aorta ascendens. (4)
Aortaklepregurgitatie
Aortaklepregurgitatie wordt veroorzaakt door primaire aandoeningen aan de aortaklepblaadjes en/of afwijkingen in de geometrie van de aortawortel en aorta ascendens. Volgens de Euro Heart Survey over VHD, kon ongeveer twee derde van de onderliggende etiologie bij aortaklepregurgitatie verklaard worden door degeneratieve factoren bij zowel tricuspide als bicuspide aortakleppen. Andere oorzaken van aortaklepregurgitatie zijn infectieuze en reumatische endocarditis van de aortaklep of aortadissectie. (2)
Aortaklepregurgitatie wordt meestal onderverdeeld in acute en chronische aortaklepregurgitatie. Acute Aortaklepregurgitatie wordt voornamelijk veroorzaakt door een infectieuze aortaklependocarditis en in mindere mate door een aortadissectie. (2)
In de AHA/ACC-richtlijnen voor VHD (4) wordt aortaklepregurgitatie dan weer op een andere manier onderverdeeld in stadia. De stadia gaan van risico op aortaklepregurgitatie (stadium A), progressieve matig tot milde aortaklepregurgitatie (stadium B), ernstig asymptomatische aortaklepregurgitatie (stadium C) tot symptomatische aortaklepregurgitatie (stadium D). (4)
Echocardiografie is het voornaamste onderzoek bij aortaklepregurgitatie. Het wordt gebruikt in de opsporing van klepmisvormingen, bij de kwantificatie van aortaklepregurgitatie en bij de evaluatie van het onderliggende mechanisme. Het wordt tevens gebruikt om de morfologie van de aortaklep in beeld te brengen en ter bepaling van de haalbaarheid van klepsparende aortaklepchirurgie of klepherstel. (2)
Indicaties voor aortaklepvervanging
In wat volgt zal dieper ingegaan worden op de indicaties voor klepvervangende chirurgie bij de verschillende aortaklepaandoeningen. Hierbij behoren aortaklepstenose en aortaklepregurgitatie tot de belangrijkste. (2) Indicaties voor chirurgie werden zowel beschreven in de Europese ESC/EACTS-richtlijnen van 2017 (2) als in de Amerikaanse AHA/ACC-richtlijnen van 2014 (4, 5).
Aortaklepstenose
Alle symptomatische patiënten vormen een indicatie voor operatie in geval van aortaklepstenose, omwille van de slechte prognose indien onbehandeld. Operaties worden wel afgeraden bij patiënten met ernstige comorbiditeit en patiënten met een oudere leeftijd, bij wie het twijfelachtig is dat een operatie zal leiden tot een betere levenskwaliteit en een verlengde levensverwachting. (2) Bij asymptomatische patiënten zijn er bijna geen indicaties voor chirurgie zolang de gemiddelde gradiënt over de aortaklep beneden de 40 mmHg blijft, ongeacht een eventuele lagere ejectiefractie van het linkerventrikel. (2)
Behandeling van asymptomatische patiënten met een lage gradiënt aortaklepstenose is moeilijk. Bij patiënten met een lage flow en lage gradiënt aortaklepstenose in combinatie met een gedaalde ejectiefractie die voornamelijk veroorzaakt wordt door een hoge afterload, verbetert de linkerventrikelfunctie doorgaans na operatie en is chirurgie aangewezen. Bij de keuze van het type chirurgie dienen bij deze groep patiënten zeker ook de klinische status en comorbiditeit, de graad van klepcalcificatie, de ernst van hart- en vaatziekten en de haalbaarheid van een adequate revascularisatie in rekening te worden gebracht. (2)
Bij asymptomatische patiënten met een lage flow, lage gradiënt aortaklepstenose en een normale ejectiefractie blijft operatie controversieel en enkel aan te raden indien er zeer significante klepobstructie aanwezig is. Patiënten met een normale flow, lage gradiënt aortaklepstenose en een normale ejectiefractie hebben geen voordeel bij operatie. Chirurgie is dus niet aan te raden in deze laatste groep. (2)
De behandeling van een asymptomatische aortaklepstenose blijft controversieel. In studies kan immers niet aangetoond worden dat vroege chirurgische aortaklepvervanging (SAVR) voordelen biedt, zelfs niet bij patiënten met een zeer ernstige asymptomatische aortaklepstenose. (2)
Samengevat is aortaklepvervanging ten gevolge van aortaklepstenose aan te raden bij:
Symptomatische patiënten met een ernstige aortaklepstenose (stadium D) en bij asymptomatische patiënten met een ernstige aortaklepstenose (stadium C) (pieksnelheid over de aortaklep 4,0 m/s of gemiddelde drukgradiënt over de aortaklep 40 mmHg), een linker ventriculaire ejectiefractie (LVEF) kleiner dan 50% en een vernauwde systolische opening van de aortaklep. (4)
Patiënten met een ernstige aortaklepstenose (stadium C en D) indien ze cardiale chirurgie dienen de ondergaan omwille van andere redenen en indien er een vernauwde systolische opening is (pieksnelheid over de aortaklep 4,0 m/s of gemiddelde drukgradiënt over de aortaklep 40 mmHg). (4)
Aortaklepvervanging kan in overweging genomen worden bij:
Asymptomatische patiënten met een zeer ernstige aortaklepstenose (stadium C) indien de systolische opening vernauwd is (pieksnelheid over de aortaklep 5,0 m/s of gemiddelde drukgradiënt over de aortaklep 60 mmHg) en het operatief risico laag is. (4)
Schijnbaar asymptomatische patiënten met een ernstige aortaklepstenose (stadium C) indien de aortaklep verkalkt is (pieksnelheid over de aortaklep van 4,0 tot 4,9 m/s of gemiddelde drukgradiënt over de aortaklep van 40 tot 59 mmHg) en een inspanningstest afwijkend is. (4)
Symptomatische patiënten met een ernstige aortaklepstenose met lage flow of lage gradiënt en een gedaalde LVEF (stadium D). (4)
Patiënten met een symptomatische aortaklepstenose met een lage flow of lage gradiënt (stadium D) indien klepobstructie de meest waarschijnlijke oorzaak is voor de symptomen van de patiënt en bij patiënten met een matige aortaklepstenose (stadium B) die reeds cardiale chirurgie dienen te ondergaan omwille van andere redenen (pieksnelheid over de aortaklep van 3,0 tot 3,9 m/s en gemiddelde drukgradiënt over de aortaklep van 20 tot 39 mmHg). (4)
Aortaklepregurgitatie
De behandeling van een aortaklepregurgitatie of aortaklepinsufficiëntie hangt af van de klinische presentatie. Acute aortaklepregurgitatie vereist steeds urgente chirurgie. (2)
Bij chronische aortaklepregurgitatie hangt een eventuele operatie af van de symptomen, de status van het linkerventrikel of de aanwezigheid van een aortadilatatie. Bij symptomatische patiënten met een chronische aortaklepregurgitatie is chirurgie steeds aan te raden, ongeacht de LVEF, indien de aortaklepregurgitatie ernstig is en het operatief risico aanvaardbaar is. (2) Asymptomatische patiënten met een ernstige aortaklepregurgitatie, een gedaalde linkerventrikelfunctie, een linker ventriculaire eind-diastolische diameter (LVEDD) groter dan 70 mm of een linker ventriculaire eind-systolische diameter (LVESD) meer dan 50 mm vormen een absolute indicatie voor chirurgie. (2)
Bij de overige asymptomatische patiënten met een chronische aortaklepregurgitatie dient de linkerventrikelfunctie regelmatig geschat te worden en dient de fysische conditie regelmatig opgevolgd te worden, aangezien deze cruciaal zijn om de ideale timing voor chirurgie te bepalen. Bij snel progressieve toename van de ventriculaire dimensies of snelle afname van de ventriculaire contractiliteit dient chirurgie sterk aangeraden te worden. (2)
Symptomatische patiënten met ernstige aortaklepregurgitatie, ongeacht de systolische linkerventrikelfunctie (stadium D). (4)
Asymptomatische patiënten met een chronisch ernstige aortaklepregurgitatie en een gedaalde systolische linkerventrikelfunctie (LVEF < 50%) in rust (stadium C) indien er geen andere oorzaak voor de systolische linkerventrikeldysfunctie gevonden kan worden. (4) Patiënten met ernstige aortaklepregurgitatie (stadium C en D) die cardiale chirurgie dienen
te ondergaan omwille van andere redenen. (4) Aortaklepchirurgie is aan te raden bij:
Patiënten met een ernstige aortaklepregurgitatie en een normale systolische linkerventrikelfunctie (LVEF 50%) maar met een ernstige linkerventrikeldilatatie (LVESD > 50 mm) (stadium C). (4)
Patiënten met een matige aortaklepregurgitatie (stadium B) die eveneens chirurgie dienen te ondergaan aan de aorta ascendens, een coronaire overbrugging (CABG) of een mitraalklepoperatie moeten ondergaan. (4)
Aortaklepchirurgie kan overwogen worden bij:
Patiënten met een ernstige aortaklepregurgitatie en een normale systolische linkerventrikelfunctie in rust (LVEF 50%) (stadium C) indien er een progressief ernstige linkerventrikeldilatatie (LVEDD > 65mm) is en het operatief risico laag is. (4)
Risicofactoren bij aortaklepvervanging
De EuroSCORE II en de Society of Thoracic Surgeons (STS) score zijn belangrijke hulpmiddelen voor preoperatieve risicostratificatie van patiënten die cardiale chirurgie ondergaan. Ze kunnen helpen een onderscheid te maken tussen patiënten met een laag en hoog operatief risico en zijn een goede voorspeller voor de postoperatieve uitkomst na cardiale chirurgie. Deze scores kennen echter ook hun beperkingen, aangezien belangrijke risicofactoren voor een slechte uitkomst zoals frailty, een porseleinaorta of voorgaande thoraxbestraling er niet bij in rekening worden gebracht. (2)
De EuroSCORE II is een goede voorspeller voor de 1-jaarsmortaliteit en wordt voornamelijk in studieverband vaak gebruikt. Het is echter belangrijk niet blind op deze scores te vertrouwen en steeds rekening te houden met de levensverwachting, de te verwachten levenskwaliteit na chirurgie en de voorkeuren van de patiënt. Dit aangezien de EuroSCORE II vooral het risico op coronair lijden postoperatief voorspelt en ze minder bruikbaar is bij klepchirurgie. (2, 3)
Er dient rekening gehouden te worden met het feit dat patiënten die een heroperatie aan de aortaklep ondergaan meestal een verhoogd risicoprofiel hebben. Het zijn immers vaak patiënten met een oudere leeftijd en met meer comorbiditeit. (2)
Prothesetypes bij aortaklepvervanging
Bij vervanging van de aortaklep kan gekozen worden tussen een biologische of een mechanische klepprothese. Uit voorafgaande gerandomiseerde studies blijkt dat de overleving tussen beide klepprothesen vergelijkbaar is en er geen significante verschillen zijn in het voorkomen van trombose of trombo-embolieën postoperatief. (2) Wel stelde men vaker bloedingen vast bij patiënten met een mechanische klepprothese en ondergaan patiënten met een biologische klepprothese vaker een heringreep. (2)
De keuze tussen een mechanische of een biologische klepprothese gebeurt door het afwegen en inschatten van allerhande risicofactoren. Bij een mechanische klepprothese dient rekening gehouden te worden met het risico op anticoagulantia gerelateerde bloedingen en trombo-embolieën. Bij een biologische klepprothese daarentegen mag men het risico op structurele klepdegeneratie (SVD) niet uit het oog verliezen. Algemeen dient men steeds rekening te houden met de leeftijd, de levensstijl en de klinische presentatie van de patiënt. (2)
Biologische klepprothesen worden aangeraden bij patiënten met een lagere levensverwachting dan de verwachte levensduur van de klepprothese, zeker indien er sprake is van comorbiditeit en indien er in de toekomst nog bijkomende chirurgische procedures noodzakelijk zullen zijn. Ook bij een verhoogd bloedingsrisico wordt best voor een biologische klepprothese gekozen. (2)
De recente tendens is dat als maar vaker gekozen wordt voor deze biologische klepprothesen. In de toekomst zullen hierdoor vermoedelijk ook meer en meer patiënten een heringreep aan de aortaklep dienen te ondergaan omwille van SVD inherent aan biologische klepprothesen. (3, 6)
Resultaten van primaire SAVR
In de behandeling van primaire aortaklepstenose is SAVR nog steeds de gouden standaard. (3, 7) De standaardchirurgie bij patiënten met een aortaklepregurgitatie was vroeger vervanging van de aortaklep. Recentelijk werden er ook meer technieken ontwikkeld om de klep te herstellen en dus een klepsparende operatie uit te voeren. Klepherstel en klepsparende operaties worden vooral uitgevoerd bij patiënten met een soepele, niet-verkalkte tricuspide of bicuspide aortaklep. Deze patiënten hebben tevens vaak een vergrote aortawortel met normaal beweeglijke klepblaadjes of prolaps van de klepblaadjes. (2)
Resultaten van primaire chirurgische operaties in de literatuur
Thourani et al. (8) onderzocht de uitkomsten na primaire SAVR bij patiënten met een laag, intermediair en hoog risico. In deze studie werden 141905 patiënten opgenomen. Deze patiënten ondergingen een geïsoleerde, primaire SAVR tussen 2002 en 2010. De meerderheid van de patiënten (80%) waren laagrisicopatiënten met een gemiddelde leeftijd van 65 jaar en de minderheid van de patiënten (6,2%) waren hoogrisicopatiënten met een gemiddelde leeftijd van 77 jaar. (8)
De voornaamste vroeg postoperatieve interventies en complicaties die optraden in deze studie waren voorkamerfibrillatie (VKF) (26,5%), verlengde ventilatie (10,3%) en nierfalen (4,2%). De hospitaalmortaliteit was gemiddeld 2,5%, meer bepaald 1,4% voor laagrisicopatiënten, 5,1% voor patiënten met een intermediair risico en 11,8% voor hoogrisicopatiënten. Voor de patiënten met een intermediair en een hoog risico werd ook een significant gedaalde (p < 0,002) vroeg postoperatieve mortaliteit vastgesteld bij de patiënten die de operatie recenter ondergingen. (8) Thourani et al. (9) onderzocht dan weer de korte en middellange termijn uitkomsten van hoogrisicopatiënten die een primaire SAVR ondergingen. Honderdnegenvijftig patiënten die een eerste, geïsoleerde AVR ondergingen werden in deze studie opgenomen. Deze patiënten ondergingen in de periode van januari 2002 tot december 2007 een operatie. Operaties gingen door in 4 verschillende academische centra in de Verenigde Staten. De gemiddelde leeftijd was 76,1 11,2 jaar en de meeste patiënten (57,9%) waren mannen. Belangrijke preoperatieve patiëntkarakteristieken waren: perifeer vaatlijden bij 33,3%, een doorgemaakte beroerte bij 23,3%, nierfalen bij 50,3% en New York Heart Association (NYHA) klasse III of IV bij 78,0% van de patiënten. Een voorgaande hartoperatie onder de vorm van een CABG werd reeds uitgevoerd bij 39,0% van de patiënten. (9)
De postoperatieve complicaties die optraden in deze studie waren: een beroerte bij 4,4%, een hartblok bij 5,0%, multiple orgaanfalen (MOF) bij 6,9%, een pneumonie bij 7,5% en een nieuwe dialyse bij 8,2% van de patiënten. (9)
Patiënten verbleven gemiddeld 12,6 11,0 dagen in het ziekenhuis. De ziekenhuismortaliteit in deze studie bedroeg 16,4%. De eenjaarsoverleving was 70,9% en de vijfjaarsoverleving 47,4%. (9)
TAVR tegenover SAVR
Nieuwere technieken zoals transcatheter aortic valve replacement (TAVR) of transcatheter aortic valve implantation (TAVI) winnen steeds meer aan belang, maar blijven voorlopig voornamelijk geïndiceerd bij patiënten met een hoog operatief risico. (3)
TAVI is niet bij iedereen mogelijk en voornamelijk geïndiceerd bij patiënten die een symptomatische aortaklepstenose hebben, in de afwezigheid van comorbiditeiten die de voordelen van deze techniek te niet doen en bij oudere patiënten met een hoog operatief risico. (2) Het is in die gevallen een veiliger alternatief voor SAVR. (3, 6)
Deze minimaal invasieve technieken vormen tegenwoordig dan ook een waardig alternatief voor SAVR met een klassieke sternotomie. (10)
Tamburino et al. (11) onderzocht de klinische uitkomsten van primaire AVR en maakte de vergelijking tussen SAVR en TAVR. Deze studie maakte deel uit van Italiaanse observationele studie naar de effectiviteit van SAVR/TAVI-procedures voor de behandeling van ernstige aortaklepstenose (OBSERVANT). Deze studie bestond uit 7618 patiënten, waarvan 5707 SAVR ondergingen en 1911 een transfemorale TAVR. (11)
De eenjaarsmortaliteit was vergelijkbaar (p = 0,936) tussen beide groepen. SAVR had een eenjaarsmortaliteit van 13,6% en TAVR 13,8%. Ook de incidentie van beroertes en van heropname omwille van cardiale redenen of hartfalen 1 jaar postoperatief waren vergelijkbaar tussen beide groepen. (11)
Reynolds et al. (12) vergeleek de gezondheid en kwaliteit van leven van patiënten die een TAVR of SAVR ondergingen omwille van aortaklepstenose en een hoog operatief risico hadden bij chirurgie. Deze studie kaderde in het Placement of Aortic Transcatheter Valve (PARTNER) onderzoek. Zeshonderdachtentwintig patiënten werden in deze studie opgenomen. De uitkomsten op vlak van morbiditeit na 1 jaar werden geëvalueerd aan de hand van de Kansas City Cardiomyopathy Questionnaire summary score en waren beter bij TAVR. (12)
Heroperatie aan de aortaklep
Reden voor heroperatie na SAVR/TAVR
Na een primaire chirurgische ingreep aan de aortaklep zijn er sommige patiënten die na verloop van tijd nood hebben aan een heroperatie. Het aantal heroperaties is de laatste jaren sterk toegenomen omwille van de toegenomen levensverwachting na klepchirurgie, de vergrijzing van de bevolking en de voorkeur voor biologische klepprothesen. Ouderen hebben immers vaak een verhoogd risicoprofiel door allerhande comorbiditeiten. (3, 13)
De belangrijkste oorzaken voor heroperaties aan de aortaklep zijn in volgorde van voorkomen: een SVD, een aortaklependocarditis, een paravalvulair lek (PVL), een recidief aortakleplijden na een voorgaand klepherstel, een mechanische klepdysfunctie of een heringreep na een Bentall procedure omwille van een aorta aneurysma. (3, 13)
Timing van heroperatie
De aanpak van kleppathologie is in het laatste decennium sterk veranderd. (14) Het doel van heringrepen aan de aortaklep is voornamelijk een slecht functionerende aortaklep of klepprothese te vervangen met aanvaardbare morbiditeit en mortaliteit. De indicaties voor heroperatie bij aortaklepstenose of -insufficiëntie zijn grotendeels dezelfde als die voor de primaire aortaklepprocedure, maar vaak wordt toch iets langer afgewacht vooraleer de heroperatie uit te voeren. Indien er echter gewacht wordt tot er reeds irreversibele schade aan het ventriculaire myocard is opgetreden, heeft dit een negatieve invloed op de late postoperatieve uitkomsten. (14)
Resultaten van chirurgische heroperaties in de literatuur
Kaneko et al. (6) onderzocht de uitkomsten van patiënten die die een electieve, geïsoleerde redo-aortaklepvervanging (redo-AVR) ondergingen en vergeleek deze met de uitkomsten van patiënten die een primaire aortaklepvervanging (AVR) ondergingen gedurende dezelfde periode. Deze studie baseerde zich op de STS Adult Cardiac Surgery database (ACSD), bijgehouden tussen juli 2011 en september 2013. In deze studie werden 3380 patiënten opgenomen die een aortaklep heroperatie ondergingen. Deze patiënten werden vergeleken met 54183 patiënten die een primaire aortaklepvervanging ondergingen. In deze studie werden enkel patiënten geïncludeerd die ouder waren dan 20 jaar. (6)
Patiënten die een heroperatie aan de aortaklep ondergingen waren in deze studie (6) gemiddeld jonger in vergelijking met patiënten die een primaire aortaklepvervanging ondergingen (66 tegenover 70 jaar, p < 0,001) en hadden gemiddeld ook meer comorbiditeit in vergelijking met patiënten die een primaire operatie aan de aortaklep ondergingen. Zo hadden patiënten die een heroperatie aan de aortaklep ondergingen gemiddeld meer ernstige, chronische longziekten (6,1% tegenover 4,2%, p < 0,0001), meer nieraandoeningen met nood aan dialyse (3,8% tegenover 2,3%, p < 0,0001), meer cerebrovasculaire ziekten en accidenten in de voorgeschiedenis (20,0% tegenover 12,5%, p < 0,0001), meer perifeer vasculair lijden (11,5% VS 8,6%, p < 0,0001), meer voorgaande myocardinfarcten (14,9% tegenover 8,9%, p < 0,0001) en meer aritmie (32,8% tegenover 19,4%, p < 0,0001). De groep die een heroperatie aan de aortaklep onderging presenteerde zich ook vaker in cardiogene shock (2,0% tegenover 0,6%, p < 0,0001), met congestief hartfalen (53,9% tegenover 38,8%, p < 0,0001), had vaker perioperatief intra-aortische ballonpomp (IABP) ondersteuning nodig (0,5% tegenover 0,3%, p < 0,0001) en coronaire ziekte van de linker hoofdtak (2,3% tegenover 0,3%, p < 0,0001) in vergelijking met patiënten die een eerste operatie aan de aortaklep ondergingen. In deze studie werd ook een verschil in etiologie tussen heroperaties aan de aortaklep en primaire operaties aan de aortaklep aangetoond.
Patiënten die een heroperatie aan de aortaklep ondergingen hadden minder vaak aortaklepstenose (62,4% tegenover 88,1%, p < 0,0001), vaker ernstige aortaklepinsufficiëntie (37,5% tegenover 16,5%, p < 0,0001) en vaker actieve infectieuze endocarditis (13,1% tegenover 3,0%, p < 0,0001) in vergelijking met primaire operaties aan de aortaklep. Heroperaties aan de aortaklep waren ook vaker urgent (38,8% tegenover 19,9%, p < 0,0001) en vaker zeer dringend (2,4% tegenover 0,7%, p < 0,0001) in vergelijking met primaire operaties aan de aortaklep. Operatieve variabelen verschilden ook tussen primaire- en heroperaties aan de aortaklep. Bij heroperaties aan de aortaklep was de duur van de aortaklem (XCT) (93 minuten tegenover 73 minuten, p < 0,0001) en de duur van de cardiopulmonaire bypass (CBP) (131 minuten tegenover 97 minuten, p < 0,0001) gemiddeld langer. Bij heroperaties aan de aortaklep was er vaker nood aan intra-operatieve bloedtransfusie (65,5% tegenover 38,0%, p < 0,0001). Op het moment van heroperatie werd tevens vaker gekozen voor mechanische klepprotheses (23,4% tegenover 11,6%, p < 0,0001) of een homograft (3,1% tegenover 0,2%, p < 0,0001) in vergelijking met primaire operaties aan de aortaklep. (6)
Heroperaties aan de aortaklep waren in deze studie (6) ook, vergeleken met primaire aortaklepoperaties, geassocieerd aan een hogere operatieve mortaliteit (4,6% tegenover 2,2%, p < 0,0001) en een hoge samengestelde operatieve mortaliteit-morbiditeit (21,6% tegenover 11,8%, p < 0,0001). Ook stelde het onderzoeksteam meer gevallen van postoperatieve beroertes (1,9% tegenover 1,4%, p = 0,02), nierfalen (4,2% tegenover 2,5%, p < 0,0001), revisie ten gevolge van bloeding of tamponade (3,9% tegenover 3,2%, p = 0,028) en vaker noodzaak aan een pacemaker (PM) (11,0% tegenover 4,3%, p < 0,0001) en vasculaire complicaties (0,06% tegenover 0,04%, p = 0,04) vast. De postoperatieve opnameduur voor heroperaties aan de aortaklep was gemiddeld ook langer voor heroperaties aan de aortaklep in vergelijking met primaire operaties aan de aortaklep (7 dagen tegenover 6 dagen, p < 0,0001). (6)
Leontyev et al. (13) onderzocht de korte- en langetermijnuitkomsten voor redo-AVR. In deze studie ondergingen 155 patiënten een geïsoleerde redo-AVR, waarvan 86 patiënten zonder aortawortelvervanging en 69 patiënten met aortawortelvervanging. Alle patiënten ondergingen de heroperatie aan de aortaklep binnen hetzelfde hartcentrum te Leipzig. Deze patiënten ondergingen een heroperatie aan de aortaklep in de periode van november 1994 tot april 2008. De opvolging van deze patiënten was 100% en duurde gemiddeld 2,7 2.8 jaar. (13)
De gemiddelde patiëntenleeftijd was 58,1 16,3 jaar. Van deze patiënten was 23,2% vrouw. Indicaties voor de heroperatie waren een infectieuze endocarditis (27,1%), een structurele
aorta aneurysma (7,1%). De intra-operatieve patiënten parameters in deze studie waren als volgt: XCT-duur was 86 38 minuten en CPB-duur was 134 75 minuten. (13)
Een vroege mortaliteit van 4,5% voor alle patiënten die een heroperatie aan de aortaklep ondergingen, werd in deze studie (13) met een jongere patiëntenpopulatie beschreven. Meer specifiek was de mortaliteit 3,5% voor aortaklepheroperaties zonder aortawortelvervanging en 5,8% voor aortaklepheroperaties met aortawortelvervanging (p = 0.05). Met een multivariate analyse kon in deze studie aangetoond worden dat een LVEF lager dan 0,30 (odds ratio (OR) 9,2; 95% betrouwbaarheidsinterval (BI) 1,1 – 80,3) en preoperatieve neurologische disfunctie (OR 22,1; 95% BI 2,3 – 197,4) onafhankelijke voorspellers waren voor de ziekenhuismortaliteit. De meest frequente complicatie in deze studie (13) was een supraventriculaire aritmie. Een aritmie die medicatie of cardioversie vereiste trad op bij 40,6% van de patiënten. Overige complicaties en interventies waren low cardiac output syndroom (LCOS) (9,0%), PM-implantatie (22,6%), pneumonie (7,1%), revisie ten gevolge van bloeding (9,7%), beroerte (5,8%), nierfalen (7,1%), gastro-intestinale bloedingen (1,3%) en gastro-intestinale ischemie (3,9%). (13)
Deze studie (13) beschreef een vijfjaarsoverleving van 66% 5% en een achtjaarsoverleving van 61% 6% voor alle patiënten, zonder significant verschil tussen patiënten die een aortaklepheroperatie ondergingen met of zonder aortawortelvervanging. In een Cox-regressieanalyse werden volgende onafhankelijke variabelen als voorspellers voor de langetermijnoverleving geïdentificeerd: preoperatieve NYHA-klasse IV (HR 2,2; 95% BI 1,5 – 3,2; p < 0,01) en een infectieuze endocarditis (HR 2,2; 95% BI 1,4 – 3,1; p < 0,01). (13)
Joshi et al. (3) onderzocht de uitkomsten van meerdere heroperaties aan de aortaklep. De focus werd in deze studie gelegd op de operatieve mortaliteit en langetermijnuitkomsten. Patiënten ondergingen in deze studie een open redo-AVR in de periode januari 2007 tot december 2016 in één centrum, het George Pompidou Europees Ziekenhuis te Parijs. 316 patiënten werden in deze studie opgenomen, waarvan 263 patiënten een eerste heroperatie ondergingen, 42 patiënten een tweede heroperatie en 11 patiënten een derde heroperatie of meer. Alle patiënten in deze studie ondergingen een aortaklepvervanging, waarvan 60,8% één of meerdere gecombineerde ingrepen zoals een tricuspidklepvervanging (TVR) of -herstel (TVP) (9,3%), een mitraalklepvervanging (MVR) (12,3%), een vervanging van de aorta ascendens (12,0%), een redo-Bentall procedure (15,5%) of een geassocieerde CABG (5,7%). (3)
De mediane leeftijd in deze studie was 58 (Q1 – Q3: 46 – 70) jaar. De voornaamste indicaties voor heroperatie waren SVD van de biologische klepprothese (44%), aortaklependocarditis (18%) en prothetische klepdehiscentie (13%). (3)
Deze studie stelde een ziekenhuismortaliteit van 7,3% vast. Deze ziekenhuismortaliteit bedroeg 7,2% voor patiënten die een eerste heroperatie aan de aortaklep ondergingen, 4,76% voor patiënten die een tweede heroperatie ondergingen en 18,2% voor patiënten die drie of meer heroperaties ondergingen (p = 0,233). De ziekenhuismortaliteit voor een heringreep ten gevolge van SVD bedroeg 3,7% terwijl deze voor een heringreep naar aanleiding van een endocarditis tot 14,0% steeg. In deze studie toonde men aan dat hoge preoperatieve NYHA-klasse (III of IV) (OR 15,9; P = 0,011), een re-entry trauma (OR 16,9; p = 0,015), een endocarditis (OR 3,7; p = 0,038) en een gelijktijdige MVR (OR 5,6; p = 0,006) onafhankelijke voorspellende factoren waren van de ziekenhuismortaliteit. In deze studie diende bij 7,3% van de patiënten een revisie uitgevoerd te worden omwille van excessieve bloeding. (3)
De achtjaarsoverleving in deze studie bedroeg 79,0 3,0% voor alle heroperaties en 88,4 3,2% voor heroperaties aan de aortaklep na SVD. Ook werd gekeken naar de recidiefkans op een volgende aortaklepoperatie na een eerste redo-AVR. De kans op een tweede heroperatie was 86,7% 3.4% na 8 jaar. (3)
Leontyev et al. (15) onderzocht de invloed van een prothetische klependocarditis op de uitkomsten bij heroperaties aan de aortaklep. Driehonderddertien patiënten ondergingen in deze studie een redo-AVR, waarvan 152 (48,6%) een prothetische klependocarditis hadden. De heroperaties hadden plaats tussen december 1994 en april 2008. (15)
In deze studie (15) waren patiënten met een prothetische klependocarditis gemiddeld ouder (65,8 14,7 jaar tegenover 57,6 16,2 jaar; p < 0,01) en hadden een hoger risicoprofiel. Patiënten die een heroperatie aan de aortaklep ondergingen omwille van prothetische klependocarditis hadden immers significant (p < 0,05) vaker nood aan urgente of zeer dringende chirurgie en vaker preoperatieve neurologische dysfunctie, trombo-embolie, nierfalen, diabetes en hartfalen. De hospitaalmortaliteit bedroeg gemiddeld 15,3%, meer specifiek 24,3% voor de endocarditis groep en 6,8% voor de niet-endocarditis groep. Een sepsis (OR 6,5; p < 0,001), een gedaalde ejectiefractie minder dan 30% (OR 5,8; p = 0,02), een geassocieerde CABG (OR 3,3; p = 0,03) en een aortawortel abces (OR 2,7; p = 0,02) werden bij prothetische klependocarditis beschreven als onafhankelijke voorspellers van de vroeg postoperatieve mortaliteit. Bij de niet-endocarditis groep werd dan weer gezien dat een geassocieerde CABG (OR 8,1; p < 0,01) of MVR (OR 4,8; p = 0,02) de vroeg postoperatieve mortaliteit goed konden voorspellen. (15)
Patiënten werden in deze studie gemiddeld lang opgevolgd, namelijk 6,5 0,4 jaar. Deze opvolging was tevens 97,4 % compleet. De één-, drie-, vijf- en tienjaarsoverleving voor patiënten met een
52% 4% tegenover 82% 3%, 43% 5% tegenover 73% 4%, 37% 5% tegenover 63% 5% en 31% 7% tegenover 56% 8% (logrank < 0,001). (15)
Een sepsis (OR 3,1; p < 0,01) en een slechte preoperatieve klinische status (OR 1,8; p = 0,04) waren voorspellers voor de mortaliteit op lange termijn voor patiënten die een heroperatie aan de aortaklep ondergingen omwille van prothetische klependocarditis. Bij de niet-endocarditis patiënten werd enkel NYHA-klasse IV (OR 2,5; p < 0,01) gezien als voorspeller van de mortaliteit op lange termijn. (15)
De afwezigheid van endocarditis gedurende vijf jaar postoperatief was 80% 0,3% voor prothetische klependocarditis tegenover 95% 0,6% voor de niet-endocarditis patiënten (p = 0,002). (15)
Naji et al. (16) onderzocht de karakteristieken en de uitkomsten van patiënten die een heroperatie aan de aortaklep dienden te ondergaan omwille van een ernstige stenose van de biologische aortaklepprothese. Tweehonderdzesenzeventig patiënten met ernstige prothetische aortaklepstenose (PAS) werden bestudeerd, waarvan 58% mannen. Ernstige PAS werd in deze studie gedefinieerd als een aortaklepoppervlak < 0,8 cm2, een gemiddelde aortaklepgradiënt 40
mmHg. Al deze patiënten ondergingen redo-AVR tussen 2000 en 2012. (16)
Deze studie (16) zag een patiënten leeftijd van gemiddeld 64 16 jaar. De gemiddelde STS-score bedroeg 8 8 en de gemiddelde aortaklepgradiënt 53 17 mmHg. 28% van de studiepatiënten had een aortaklepregurgitatie groter dan graad 2. 39% onderging een geïsoleerde redo-AVR. De overige patiënten ondergingen gecombineerde chirurgie, bestaande uit CABG en/of chirurgie aan de aorta. (16)
Een dertigdagenmortaliteit van 2,3% werd beschreven voor patiënten met ernstige PAS die een heroperatie aan de aortaklep ondergingen. (16)
Drieëntwintig procent van de patiënten haalden het vooraf bepaalde eindpunt van opvolging. Op dat punt waren 48 patiënten gestorven en 19 patiënten waren opgenomen voor congestief hartfalen. Een hogere STS-score (HR 1,35), een hogere graad van aortaklepregurgitatie (HR 1,29) en een hogere rechter ventriculaire systolische druk (HR 1,3) werden in deze studie via een multivariabele Cox-overlevingsanalyse gelinkt aan een slechtere langetermijnuitkomsten (p < 0,01). (16)
TAVR als heroperatie
Bij degeneratieve biologische klepprotheses kan valve-in-valve TAVR een waardig alternatief zijn voor een open heroperatie aan de aortaklep in zeer geselecteerde gevallen. (3, 6)
Erlebach et al. (17) toonde in een retrospectieve studie binnen één centrum aan dat er geen significant verschil is in dertigdagenmortaliteit tussen patiënten die een valve-in-valve TAVI ondergingen na een voorgaande open SAVR in vergelijking met patiënten die een traditionele redo-AVR ondergingen (4% tegenover 0%, p = 0,121). In deze studie echter, kon men wel aantonen dat de 1-jaarsoverleving voor patiënten die een valve-in-valve TAVI ondergingen na een voorgaande open SAVR significant minder was in vergelijking met patiënten die een traditionele redo-AVR ondergingen (83% tegenover 96%, p < 0,001). (3, 17)
Besluit
De vroege postoperatieve mortaliteit voor heroperatie aan de aortaklep schommelt gemiddeld dus ergens tussen de 2,3 (16) en 7,3% (3) en is onder andere afhankelijk van de indicatie voor heroperatie en eventuele geassocieerde ingrepen. De mortaliteit voor SVD is lager dan voor endocarditis. (3)
Patiënten die een heroperatie aan de aortaklep ondergaan presenteren zich ook vaker met deze ernstige pathologie. Ze hebben vaker een infectieuze endocarditis en ernstige aortaklepinsufficiëntie. Daarenboven presenteren ze zich minder vaak met minder ernstige pathologie zoals een aortaklepstenose.De vroege postoperatieve mortaliteit is dan ook hoger in vergelijking met primaire operaties. Bij heroperaties aan de aortaklep treden gemiddeld vaker complicaties op. (6)
In voorgaande studies werd een relatie gevonden tussen de LVEF (6), NYHA-klasse III of IV, endocarditis, een gelijktijdige MVR (3) en een geassocieerde CABG (15) en de vroeg postoperatieve mortaliteit, weergegeven aan de hand van de ziekenhuismortaliteit .
Doel van de studie
Deze studie zal de vroegtijdige resultaten voor heroperaties aan de aortaklep binnen het Universitair ziekenhuis (UZ) Gent in beeld brengen en zal deze vergelijken met de verschenen literatuur over heroperaties aan de aortaklep. Voornamelijk zal gekeken worden naar vroeg postoperatieve mortaliteit en morbiditeit. Vervolgens zal op zoek gegaan worden naar risicofactoren die de vroeg postoperatieve mortaliteit en morbiditeit voor heroperaties aan de aortaklep binnen het UZ Gent kunnen voorspellen. Deze zullen eveneens besproken worden en vergeleken worden met de risicofactoren beschreven in de literatuur.
Methode en patiënten
Methode literatuurstudie
De introductie van deze thesis werd geschreven aan de hand van de reeds verschenen literatuur omtrent heroperaties aan de aortaklep, operaties aan de aortaklep in het algemeen en de anatomie van de aortaklep. Bij het beschrijven van de pathologie van de aortaklep en de indicaties voor aortaklepchirurgie werd, op aanraden van de promotor van deze thesis, Prof. Dr. François, gebruik gemaakt van de Europese ESC/EACTS-richtlijnen van 2017 (2) en van de Amerikaanse AHA/ACC-richtlijnen van 2014 (4, 5). Deze artikels werden teruggevonden door de overeenkomstige titel in te geven via PubMed. De anatomie van de aortaklep werden beschreven op basis van een artikel (1) opgezocht via Google Scholar met de zoekterm ‘aortic valve anatomy’ . De studies (3, 6, 13, 15, 16) waarop de beschrijving van reeds gekende informatie omtrent chirurgische heroperaties aan de aortaklep gebaseerd werd, werden eveneens gevonden via Google Scholar en PubMed door afwisselend de zoektermen ‘redo aortic valve operations’, ‘redo aortic valve surgery’ en ‘redo aortic valve replacement’ in te geven. Artikels werden geselecteerd volgens titel, impact factor en abstract. Aanvullende literatuur omtrent TAVR/TAVI (10-12), primaire SAVR (7-9) en de timing van heroperaties aan de aortaklep (14) werd opgezocht door de zoektermen ‘TAVR’ en ‘TAVI’, ‘SAVR’ en ‘timing aortic valve replacement’ in te geven in Google Scholar.
Studiepopulatie
Deze retrospectieve studie includeerde 131 consecutieve patiënten die in het UZ Gent een heroperatie aan de aortaklep in de periode van 01/01/2000 tot 10/06/2018 ondergingen. Enkel patiënten ouder dan 16 jaar die reeds een voorafgaande procedure aan de aortaklep hadden ondergaan kwamen in aanmerking om in deze studie opgenomen te worden.
De gepseudonimiseerde database waarop deze retrospectieve analyse uitgevoerd is, werd aangeboden door de promotor van deze thesis, Prof. Dr. François, en verder statistisch verwerkt. Op 21/06/2018 werd de goedkeuring door het Ethisch Comité verleend om deze studie uit te voeren. Schriftelijke geïnformeerde toestemming werd niet nodig geacht door het ethisch comité aangezien het de verzameling betrof van reeds bestaande patiëntengegevens. Alle variabelen die werden bijgehouden in deze database, werden weergegeven in Appendix.
Statistische analyse
Aan de hand van de Shapiro-Wilk normaliteitstest werd bepaald of de variabelen al dan niet parametrisch verdeeld waren. Op basis van deze gegevens werd de weergave van de onderstaande resultaten bepaald. Parametrisch verdeelde variabelen werden beschreven met
behulp van het gemiddelde en de standaarddeviatie. Niet-parametrisch verdeelde variabelen werden beschreven met behulp van mediaan en range (minimum – maximum). De meeste variabelen waren niet parametrisch verdeeld. Met behulp van een binaire logistische regressieanalyse werden univariabele analyses uitgevoerd om associatie tussen bepaalde risicofactoren en mortaliteit of morbiditeit te achterhalen. Er werd gekozen voor een binaire logistische regressieanalyse in plaats van Chi-kwadraat testen omdat deze ook een kansverhouding weergeven. Vervolgens werd met behulp van een meervoudige logistische regressieanalyse een multivariabele analyse uitgevoerd om een beter voorspellend model te vormen. De modelkwaliteit werd weergegeven aan de hand van de Nagelkerke R2 die de variantie
in de uitkomstvariabele aangeeft. De statistische analyses werden verwerkt via SPSS 25. Alle statistische hypothesen werden tweezijdig getest en een p-waarde 0,05 werd statistisch significant geacht. Om de significantie te bepalen tussen bepaalde groepen binnen de variabelen, werd omwille van de niet-parametrische verdeling, een Mann-Whitney U-test.
Figuren en tabellen weergegeven in deze thesis werden eveneens gemaakt met behulp van SPSS 25.
Resultaten
Preoperatieve parameters
Preoperatieve patiëntkarakteristieken
De preoperatieve patiëntkarakteristieken voor heroperaties aan de aortaklep werden weergegeven in Tabel 1. Deze patiëntkarakteristieken bevatten onder andere de demografische gegevens van de geïncludeerde patiënten, de antropometrische gegevens, comorbiditeiten, de nierfunctie, eventuele ritmestoornissen en de berekende EuroSCORE II van deze patiënten.
Honderd eenendertig patiënten werden in deze retrospectieve cohorte studie opgenomen, waarvan 43 (32,8%) van het vrouwelijke en 88 (67,2%) van het mannelijke geslacht.
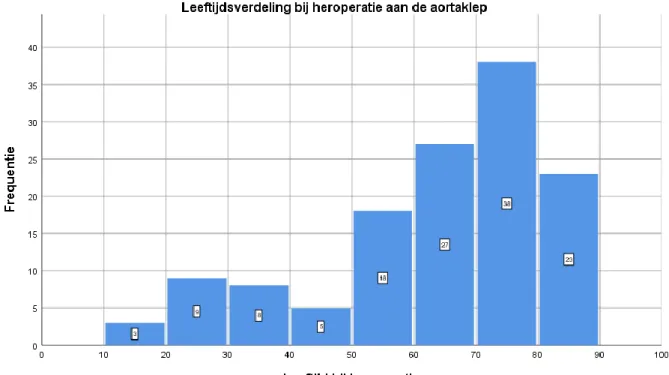
De mediane leeftijd van deze patiënten was 66 jaar met als minimum (min.) 17 jaar en als maximum (max.) 87 jaar. De leeftijdsverdeling van patiënten die een heroperatie aan de aortaklep ondergingen werd weergegeven in Figuur 1.
Figuur 1. Leeftijdsverdeling (in jaren) van patiënten bij heroperatie aan de aortaklep (leeftijdsinterval = 10 jaar). N = 131
De mediane body-mass index (BMI) bij opname van patiënten die een heroperatie aan de aortaklep ondergingen was 25,08 kg/m2 met een minimum van 15,24 kg/m2 en een maximum van 35,86
Ook comorbiditeit van patiënten werd bijgehouden. Twaalf patiënten (9,2%) hadden Chronisch obstructief longlijden (COPD), 16 (15,3%) patiënten hadden diabetes, 20 (15,3%) patiënten hadden perifeer vaatlijden, 42 (32,1%) patiënten hadden coronair lijden en 47 (35,9%) patiënten leden aan arteriële hypertensie. De nierfunctie werd preoperatief bepaald aan de hand van de creatinineklaring. De mediane preoperatieve creatinineklaring bedroeg 69 ml/min.
Preoperatief waren 98 (74,8%) patiënten in sinusritme (SR) en 29 (22,1%) patiënten maakten een VKF door. Twee (1,5%) patiënten hadden reeds een PM gekregen voor de heroperatie.
Logistische parameters zoals NYHA-klasse en de EuroSCORE II werden preoperatief aan de hand van een klinische evaluatie bepaald om zo de ernst van de klachten bij de patiënt en het risico op mortaliteit bij klepchirurgie in te schatten. Heel wat patiënten hadden een preoperatief beperkte inspanningstolerantie met 43 (32,8%) patiënten in NYHA-klasse III en 23 (17,6%) patiënten in NYHA-klasse IV. Vijfendertig (26,7%) patiënten waren preoperatief onbeperkt in hun fysieke activiteit en waren in NYHA-klasse I. Preoperatieve risicostratificatie van de patiënten stelde een mediane EuroSCORE II van 10,69%. De EuroSCORE II bevatte 41 ontbrekende waarden.
Demografische gegevens
Leeftijd (jaar), mediaan (min. – max.) 66 (17 – 87)
Geslacht, n (%)
Vrouw 43 (32,8)
Man 88 (67,2)
Antropometrische gegevens
Gewicht bij opname (kg), mediaan (min. – max.) 73 (43 – 112)
BMI bij opname (kg/m2), mediaan (min. – max.) 25,08 (15,24 – 35,86) Comorbiditeiten, n (%) COPD 12 (9,2) Diabetes 16 (15,3) Perifeer vaatlijden 20 (15,3) Coronair lijden 42 (32,1) Hypertensie 47 (35,9) Nierfunctie
Preoperatieve creatinineklaring (ml/min), mediaan
(min. – max.) 69 (13-91) Hartritme en ritmestoornissen, n (%) SR 98 (74,8) VKF 29 (22,1) VES 1 (0,8) AVBII 1 (0,8)
Logistische parameters NYHA-klasse, n (%) I 35 (26,7) II 30 (22,9) III 43 (32,8) IV 23 (17,6)
EuroSCORE II (%), mediaan (min. – max.) 10,69 (1,52 – 49,86)
Tabel 1. Preoperatieve patiëntkarakteristieken bij heroperatie aan de aortaklep. N = 131
Preoperatieve echocardiografische parameters
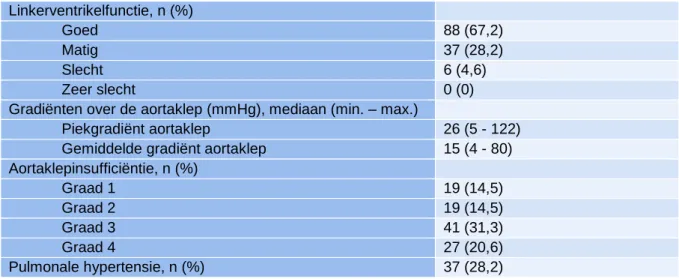
Preoperatieve echocardiografische parameters van de patiënten die een heroperatie aan de aortaklep ondergingen werden weergegeven in Tabel 2. Deze preoperatieve echocardiografische parameters bevatten onder andere de linkerventrikelfunctie, de gradiënten over de aortaklep, de graad van aortaklepinsufficiëntie en het voorkomen van pulmonale hypertensie, die in een preoperatieve consultatie bepaald werden. Linkerventrikelfunctie werd onderverdeeld in goed, matig, slecht en zeer slecht en was afhankelijk van de LVEF. Een goede linkerventrikelfunctie kwam overeen met een LVEF groter dan 50%, een matige linkerventrikelfunctie kwam overeen met een LVEF tussen 31 en 50%, een slechte linkerventrikelfunctie kwam overeen met een LVEF tussen 21% en 30% en zeer slecht met een LVEF van 20% of lager. Pulmonale hypertensie werd gedefinieerd als een longslagaderdruk (PAP) groter dan 55 mmHg.
Achtentachtig (67,2%) patiënten hadden een goede linkerventrikelfunctie. Bij 6 (4,6%) patiënten was de linkerventrikelfunctie ernstig beperkt, deze patiënten hadden een slechte linkerventrikelfunctie. Geen enkele patiënt had echter preoperatief een zeer slechte linkerventrikelfunctie.
Gradiënten over de aortaklep waren als volgt: de mediane piekgradiënt over de aortaklep bedroeg 26 mmHg (min. 5 – max. 122 mmHg) en de mediane gemiddelde gradiënt over de aortaklep bedroeg 15 mmHg (min. 4 – max. 80 mmHg).
Heel wat patiënten hadden een ernstige graad van aortaklepinsufficiëntie met een graad 4 aortaklepinsufficiëntie bij 27 (20,6%) patiënten en een graad 3 aortaklepinsufficiëntie bij 41 (31,3%) patiënten. Vijfentwintig patiënten (19,1%) hadden helemaal geen aortaklepinsufficiëntie.
Linkerventrikelfunctie, n (%)
Goed 88 (67,2)
Matig 37 (28,2)
Slecht 6 (4,6)
Zeer slecht 0 (0)
Gradiënten over de aortaklep (mmHg), mediaan (min. – max.)
Piekgradiënt aortaklep 26 (5 - 122) Gemiddelde gradiënt aortaklep 15 (4 - 80) Aortaklepinsufficiëntie, n (%) Graad 1 19 (14,5) Graad 2 19 (14,5) Graad 3 41 (31,3) Graad 4 27 (20,6) Pulmonale hypertensie, n (%) 37 (28,2)
Tabel 2. Preoperatieve echocardiografische parameters bij heroperatie aan de aortaklep. N = 131
Parameters vorige operatie
Patiëntkarakteristieken en operatieve factoren van de vorige operatie
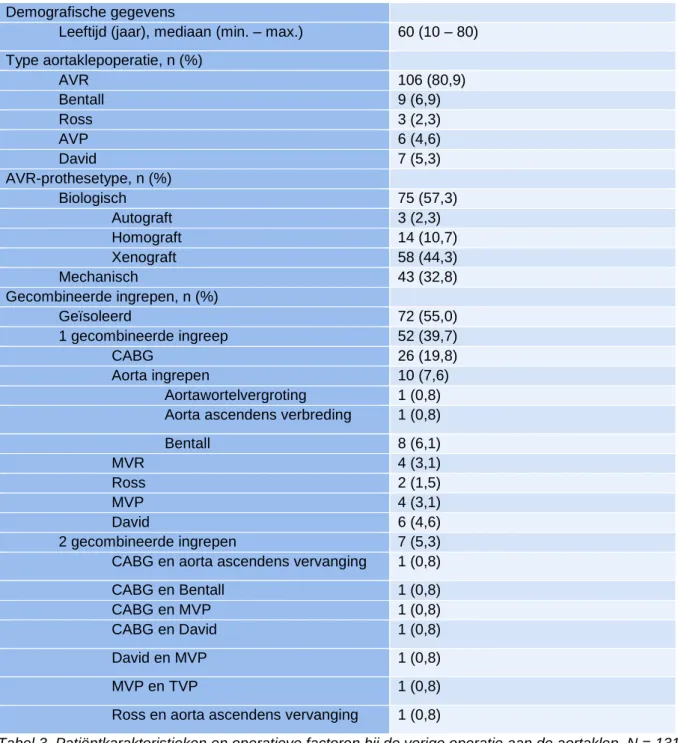
De patiëntkarakteristieken en operatieve factoren bij de vorige ingreep aan de aortaklep werden weergegeven in Tabel 3. Deze patiëntkarakteristieken bevatten de demografische gegevens van de patiënten. De operatieve factoren bestaan uit het type aortaklepoperatie, het gebruikte prothesetype en de gecombineerde ingrepen bij de vorige ingreep.
De mediane leeftijd bij de vorige operatie aan de aortaklep van patiënten die een heroperatie aan de aortaklepoperatie ondergingen was 60 jaar.
Honderdenzes (81%) patiënten ondergingen bij de vorige operatie een aortaklepvervanging, 9 (6,9%) patiënten een volledige aortawortelvervanging en 3 (2,3%) patiënten een Ross procedure met vervanging van de aortaklep door de eigen pulmonaalklep. Dertien (9,9%) patiënten ondergingen een klepsparende ingreep onder de vorm van aortaklepherstel (AVP) of een David procedure.
De prothesetypes, gebruikt bij de vorige operatie bij patiënten waren als volgt: 75 (57,3%) patiënten kregen een biologische klepprothese. Achtenvijftig (93,5%) van deze biologische klepprothesen waren xenografts. Drieënveertig (32,8%) patiënten kregen een mechanische klepprothese bij de vorige operatie.
Van de patiënten die een heroperatie aan de aortaklep ondergingen, ondergingen 72 (55,0%) patiënten bij de vorige operatie aan de aortaklep een geïsoleerde ingreep, 52 (39,7%) patiënten ondergingen 1 gecombineerde ingreep en 7 (5,3%) patiënten 2 gecombineerde ingrepen. Deze
Demografische gegevens
Leeftijd (jaar), mediaan (min. – max.) 60 (10 – 80) Type aortaklepoperatie, n (%) AVR 106 (80,9) Bentall 9 (6,9) Ross 3 (2,3) AVP 6 (4,6) David 7 (5,3) AVR-prothesetype, n (%) Biologisch 75 (57,3) Autograft 3 (2,3) Homograft 14 (10,7) Xenograft 58 (44,3) Mechanisch 43 (32,8) Gecombineerde ingrepen, n (%) Geïsoleerd 72 (55,0) 1 gecombineerde ingreep 52 (39,7) CABG 26 (19,8) Aorta ingrepen 10 (7,6) Aortawortelvergroting 1 (0,8) Aorta ascendens verbreding 1 (0,8)
Bentall 8 (6,1) MVR 4 (3,1) Ross 2 (1,5) MVP 4 (3,1) David 6 (4,6) 2 gecombineerde ingrepen 7 (5,3) CABG en aorta ascendens vervanging 1 (0,8)
CABG en Bentall 1 (0,8) CABG en MVP 1 (0,8) CABG en David 1 (0,8)
David en MVP 1 (0,8)
MVP en TVP 1 (0,8)
Ross en aorta ascendens vervanging 1 (0,8)
Tabel 3. Patiëntkarakteristieken en operatieve factoren bij de vorige operatie aan de aortaklep. N = 131
Parameters heroperatie
Indicaties voor heroperatie
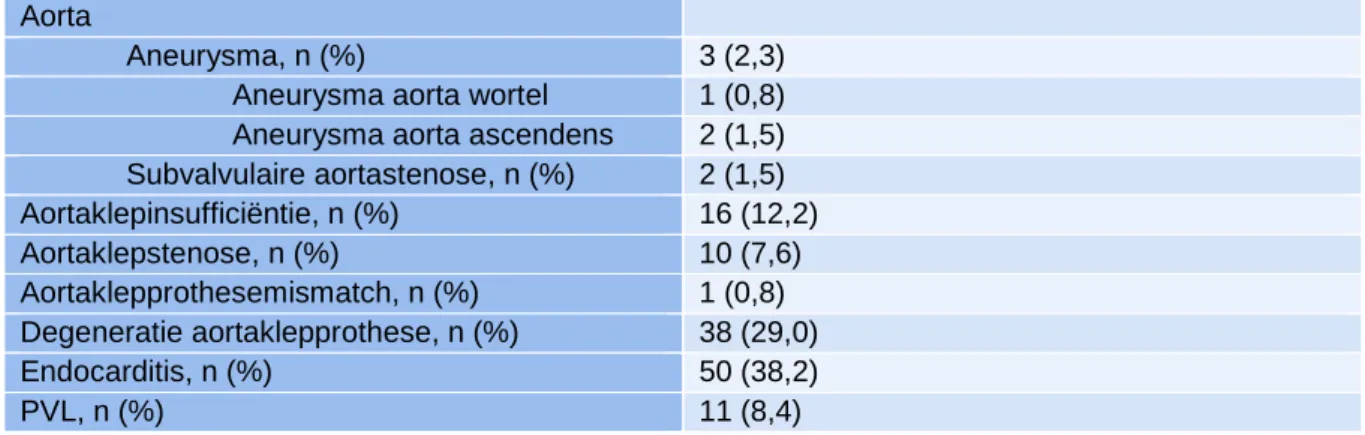
Indicaties voor heroperatie aan de aortaklep staan beschreven in Tabel 4. De voornaamste indicaties voor heroperatie aan de aortaklep waren aortaklependocarditis bij 50 (38,2%) patiënten,
patiënten (12,2%). Andere indicaties zoals aortaklepstenose traden op bij 10 (7,6%) patiënten. Drie (2,3%) patiënten hadden een aneurysma van de aorta.
Aorta
Aneurysma, n (%) 3 (2,3) Aneurysma aorta wortel 1 (0,8) Aneurysma aorta ascendens 2 (1,5) Subvalvulaire aortastenose, n (%) 2 (1,5) Aortaklepinsufficiëntie, n (%) 16 (12,2) Aortaklepstenose, n (%) 10 (7,6) Aortaklepprothesemismatch, n (%) 1 (0,8) Degeneratie aortaklepprothese, n (%) 38 (29,0) Endocarditis, n (%) 50 (38,2) PVL, n (%) 11 (8,4)
Tabel 4. Indicaties voor heroperatie aan de aortaklep. N = 131
Interval tussen ingrepen
Voor heroperaties aan de aortaklep was het mediane aantal dagen tussen de vorige operatie en de heroperatie aan de aortaklep gelijk aan 6,05 jaar met een minimum van 5 dagen en een maximum van 44,47 jaar tussen beide ingrepen. Een spreidingsgrafiek voor het interval tussen de vorige operatie aan de aortaklep en de heroperatie aan de aortaklep werd weergegeven in Figuur 2. Het langste interval was bij 2 patiënten. Eén patiënt onderging een AVR na AVP 44,47 jaar later omwille van een aortakleptrombose. De andere patiënt onderging ook een AVR na AVP 39 jaar later omwille van een subvalvulaire aortaklepstenose.
Operatieve en intra-procedurele parameters van de heroperatie
De operatieve en intra-procedurele parameters bij heroperatie aan de aortaklep staan weergegeven in Tabel 5. Deze operatieve en intra-procedurele parameters voor heroperatie bevatten onder andere het type aortaklepoperatie, om de hoeveelste heroperatie aan de aortaklep het precies gaat, de urgentie van de heroperatie, het gebruikte prothesetype, eventuele gecombineerde ingrepen en de intra-procedurele factoren.
Bij heroperatie aan de aortaklep ondergingen 75 (57,3%) patiënten een redo-AVR. Van de patiënten die een Bentall procedure ondergingen, ondergingen 8 (6,1%) patiënten een redo-Bentall procedure en 28 (21,4%) patiënten een Bentall procedure na een voorgaande AVR. Slechts 4 (3,1%) patiënten ondergingen een AVP bij heroperatie aan de aortaklep. Overige heroperatietypes werden weergegeven in Tabel 5.
Er werd tevens bijgehouden hoe vaak deze patiënten reeds een voorgaande operatie aan de aortaklep hadden ondergaan. Honderddertien (86,3%) patiënten ondergingen een eerste heroperatie aan de aortaklep, 17 (13,0%) patiënten een tweede en slechts 1 (0,8%) patiënt een derde.
Bij heroperatie dienden 6 patiënten (4,6%) de dag van opname nog geopereerd te worden, 92 patiënten vereisten (70,2%) urgente chirurgie en 33 patiënten (25,2%) werden electief geheropereerd.
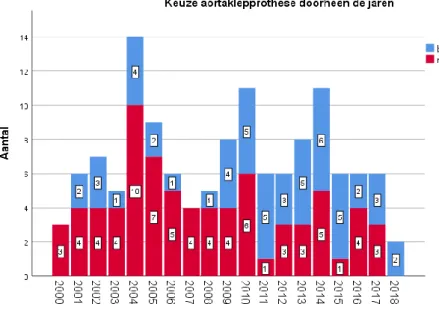
De prothesetypes gebruikt bij heroperaties aan de aortaklep die niet klepsparend werden uitgevoerd, waren de volgende: 54 patiënten (41,2%) kregen een biologische aortaklepprothese en 75 (57,3%) kregen een mechanische aortaklepprothese. Zevenenveertig (87,0%) van deze biologische klepprothesen waren xenografts. Figuur 3 geeft de keuze van de aortaklepprothese weer, gebruikt bij heroperaties aan de aortaklep, over de jaren heen.
Figuur 3. Keuze van het aortaklepprothesetype bij heroperatie aan de aortaklep doorheen de jaren. N = 131
Gecombineerde ingrepen toegepast bij heroperaties aan de aortaklep waren als volgt: 57 (43,5%) patiënten ondergingen een geïsoleerde ingreep, 57 (43,5%) patiënten ondergingen 1 gecombineerde ingreep, 15 (11,5%) patiënten ondergingen 2 gecombineerde ingrepen en 2 (1,5%) patiënten ondergingen zelfs 3 gecombineerde ingrepen. De voornaamste geassocieerde ingrepen bij patiënten die 1 gecombineerde ingreep ondergingen waren: een operatie aan de aorta bij 33 patiënten (25,2%), een CABG bij 8 (6,1%) patiënten, mitraalklepherstel (MVP) bij 8 (6,1%) patiënten en een MVR bij 4 (3,1%) patiënten. Deze gecombineerde ingrepen aan de aortawortel bestonden voornamelijk uit Bentall procedures. Negenentwintig (22,1%) patiënten ondergingen zo een Bentall procedure.
Bij de patiënten die meer dan 1 geassocieerde ingreep aan de aortaklep ondergingen, onderging de meerderheid, namelijk 6 (4,6%), van de patiënten een CABG samen met een Bentall procedure. Ook intra-procedurele factoren van de heroperatie aan de aortaklep, zoals CPB-duur en XCT-duur, werden bijgehouden. De mediane CPB-duur was 114 minuten voor geïsoleerde ingrepen en 154 minuten voor gecombineerde ingrepen. De mediane XCT-duur was dan weer 71 minuten voor geïsoleerde ingrepen en 107 min voor gecombineerde ingrepen. Voor zowel CPB-duur als XCT-duur werd er significant (p < 0,001) verschil gezien tussen geïsoleerde en gecombineerde ingrepen.
Type aortaklepoperatie, n (%) AVR Redo-AVR 75 (57,3) AVR na Bentall 1 (0,8) AVR na AVP 3 (2,3) AVR na David 8 (6,1) Bentall Redo-Bentall 8 (6,1) Bentall na AVR 28 (21,4) Bentall na Ross 2 (1,5) Bentall na AVP 1 (0,8) Ross Ross na AVP 1 (0,8) AVP AVP na AVR 3 (2,3) AVP na Ross 1 (0,8) Hoeveelste Heringreep, n (%) 1e heringreep 113 (86,3) 2e heringreep 17 (13,0) 3e heringreep 1 (0,8) Urgentie, n (%)
Operatie op dag zelf 6 (4,6)
Urgent 92 (70,2) Electief 33 (25,2) AVR-prothesetype, n (%) Biologisch 54 (41,2) Autograft 2 (1,5) Homograft 5 (3,8) Xenograft 47 (35,9) Mechanisch 75 (57,3) Gecombineerde ingrepen, n (%) Geïsoleerd 57 (43,5) 1 gecombineerde ingreep 57 (43,5) CABG 8 (6,1) Aorta ingrepen 33 (25,2) Aorta ascendens vervanging 1 (0,8) Arcus aortae vervanging 1 (0,8) Aortawortelvergroting 2 (1,5) Bentall 29 (22,1) MVR 4 (3,1) Ross 1 (0,8) MVP 8 (6,1) TVP 2 (1,5) Septale myectomie 1 (0,8) 2 gecombineerde ingrepen 15 (11,5) CABG en Bentall 6 (4,6) CABG en MVR 1 (0,8) Bentall en PVR 1 (0,8)
Bentall en MVP 2 (1,5) MVR en TVP 2 (1,5) MVP en TVP 2 (1,5) TVP en VSD-sluiting 1 (0,8) 3 gecombineerde ingrepen 2 (1,5) CABG, Bentall en MVR 1 (0,8) CABG, MVR en TVP 1 (0,8) Intra-procedurele factoren
Duur CPB (min), mediaan (min. – max.)
Geïsoleerde ingrepen 114 (58 – 171) Gecombineerde ingrepen 154 (80 – 368) Duur XCT (min), gemiddelde (min. – max.)
Geïsoleerde ingrepen 71 (38 – 149) Gecombineerde ingrepen 107 (53 – 174)
Tabel 5. Operatieve en intra-procedurele gegeven bij heroperatie aan de aortaklep. N = 131
Vroeg postoperatieve parameters
Vroeg postoperatieve interventies en complicaties
Vroege postoperatieve interventies en complicaties bij heroperatie aan de aortaklep staan weergegeven in Tabel 6. Deze vroege postoperatieve interventies en complicaties traden op in de postoperatieve periode van hospitalisatie. Onder vroege postoperatieve interventies werden eventuele verlengde ventilatie en diens duur, revisie ten gevolge van bloeding of tamponade, cardioversie, IABP en nieuwe dialyse bijgehouden. Bij vroege postoperatieve complicaties werden pulmonale complicaties, hartritmestoornissen, endocarditis, bloeding, LCOS, sepsis, neurologische events, acute nierinsufficiëntie, gastro-intestinale ischemie en multiple orgaan falen bijgehouden. Acute nierinsufficiëntie (ANI) werd omschreven als een serumcreatinine van meer dan 200 mol/l.
Pulmonale complicaties kwamen voor bij 21 (16,0%) patiënten. Acht (6,1%) patiënten werden postoperatief verlengd beademd na de operatie. De mediane duur van deze ventilatie was dan 8 dagen.
Vroeg postoperatieve bloeding trad op bij 21 (16,0%) patiënten. Zeventien (13,0%) van deze patiënten dienden postoperatief een revisie te ondergaan omwille van bloeding of tamponade. Bij 45 (34,6%) patiënten trad postoperatief een hartritmestoornis op. De voornaamste hartritmestoornis die optrad was een VKF bij 34 (26,0%) patiënten. Overige hartritmestoornissen die optraden werden beschreven in Tabel 6. Zes (4,6%) dienden een cardioversie te ondergaan
omwille van VKF. Acht (6,1%) patiënten, met inbegrip van alle 6 (4,5%) patiënten die een derdegraads atrioventriculaire blok (AVBIII) doormaakten, kregen perioperatief een PM ingeplant. Bij 12 patiënten (9,2%) trad vroeg postoperatief een LCOS op als complicatie. Twaalf patiënten (9,2%) kregen perioperatief dan ook een IABP voor mechanische cardiale ondersteuning.
Bij 33 patiënten (25,2%) trad postoperatief een acute nierinsufficiëntie op. Elf patiënten (8,4%), die preoperatief geen dialysepatiënten waren, dienden postoperatief hiervoor een dialyse te ondergaan.
Bij geen enkele patiënt trad vroeg postoperatief een recidiverende endocarditis op. Overige complicaties werden weergeven in Tabel 6.
Postoperatieve interventies Verlengde ventilatie, n (%) 8 (6,1)
Duur indien verlengde ventilatie (d), gemiddelde (min. – max.)
8 (2 – 12)
Revisie ten gevolge van bloeding of tamponade, n (%) 17 (13,0) Cardioversie, n (%) 6 (4,6) PM, n (%) 8 (6,1) IABP, n (%) 12 (9,2) Nieuwe dialyse, n (%) 11 (8,4) Postoperatieve complicaties, n (%) Pulmonaal 21 (16,0) Cardiaal Hartritmestoornissen 45 (34,4) VKF 34 (26,0) VK-flutter 1 (0,8) VT 1 (0,8) VES 3 (2,4) AVIII 6 (4,6) Endocarditis 0 (0,0) Bloeding 21 (16,0) LCOS 12 (9,2) Sepsis 7 (5,3) Neurologisch event 2 (1,5) Acute nierinsufficiëntie 33 (25,2) Gastro-intestinale ischemie 2 (1,5) MOF 5 (3,8)
Hospitalisatie en mortaliteit
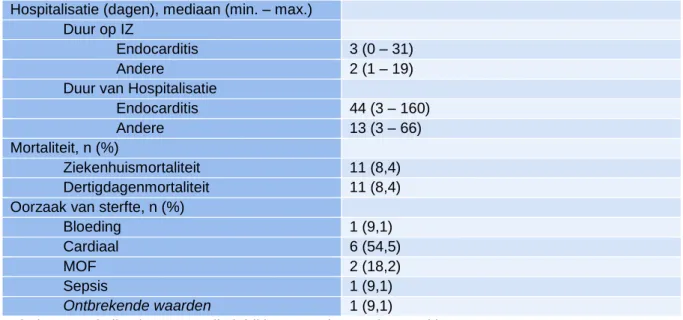
Parameters voor hospitalisatie en mortaliteit voor patiënten die een heroperatie aan de aortakep ondergingen zijn weergegeven in Tabel 7. Parameters voor hospitalisatie omvatten de duur op intensieve zorgen (IZ) en de duur van hospitalisatie. Deze werden apart weergegeven voor endocarditis als reden voor heroperatie aan de aortaklep en alle andere indicaties voor heroperatie aan de aortaklep. Bij mortaliteit werd de ziekenhuismortaliteit en dertigdagenmortaliteit vermeld, samen met de oorzaak van overlijden indien gekend.
Voor endocarditis bedroeg de duur op IZ mediaan 3 dagen en voor de overige indicaties voor heroperatie 2 dagen. De duur van de hospitalisatie bedroeg voor endocarditis mediaan 44 dagen en voor de overige indicaties voor heroperatie 13 dagen. Voor zowel de duur op IZ als de duur van de hospitalisatie was er een significant (p < 0,05) verschil tussen endocarditis en overige indicaties voor heroperatie.
Dertigdagenmortaliteit en ziekenhuismortaliteit waren identiek. Elf (8,4%) patiënten stierven tijdens de hospitalisatie of binnen een periode van 30 dagen postoperatief. Van deze patiënten overleed 1 op de operatietafel. Nog eens 4 patiënten stierven bijkomend in de periode van 2 maand tot 1 jaar postoperatief. De oorzaak van deze sterfte werd weergegeven in Tabel 7. De meerderheid van deze patiënten, namelijk 6 (54,5%), overleden aan cardiale verwikkeling.
Hospitalisatie (dagen), mediaan (min. – max.) Duur op IZ
Endocarditis 3 (0 – 31) Andere 2 (1 – 19) Duur van Hospitalisatie
Endocarditis 44 (3 – 160) Andere 13 (3 – 66) Mortaliteit, n (%)
Ziekenhuismortaliteit 11 (8,4) Dertigdagenmortaliteit 11 (8,4) Oorzaak van sterfte, n (%)
Bloeding 1 (9,1)
Cardiaal 6 (54,5)
MOF 2 (18,2)
Sepsis 1 (9,1)
Ontbrekende waarden 1 (9,1)
Tabel 7. Hospitalisatie en mortaliteit bij heroperatie aan de aortaklep. N = 131
Linkerventrikelfunctie was bij 71 (59,2%) van de patiënten goed. Twee (1,7%) van de patiënten had echter wel een zeer slechte linkerventrikelfunctie.
De gradiënten over de aortaklep waren als volgt: de piekgradiënt was 18 mmHg en de gemiddelde gradiënt was 10 mmHg.
Zevenenzestig (63,3%) van de patiënten hadden geen aortaklepinsufficiëntie meer. Geen enkele patiënt had nog een graad 3 of graad 4 aortaklepinsufficiëntie bij ontslag uit het ziekenhuis. Tweeënnegentig patiënten (76,7%) waren in sinusritme bij ontslag. Zeventien (14,2%) verlieten het ziekenhuis terwijl ze een VKF doormaakten.
Linkerventrikelfunctie, n (%)
Goed 71 (59,2)
Matig 42 (35,0)
Slecht 4 (3,3)
Zeer slecht 2 (1,7)
Gradiënten over de aortaklep (mmHg), mediaan (min. – max.)
Piekgradiënt aortaklep 18 (2 – 51) Gemiddelde gradiënt aortaklep 10 (1 – 25) Aortaklepinsufficiëntie, n (%) Geen 76 (63,3) Graad 1 38 (31,7) Graad 2 4 (3,3) Graad 3 0 (0,0) Graad 4 0 (0,0) Hartritme en ritmestoornissen, n (%) SR 92 (76,7) VKF 17 (14,2) VES 1 (0,8) PM 10 (7,6) Pulmonale hypertensie, n (%) 7 (5,8)
Tabel 8. Echocardiografische parameters bij ontslag uit het ziekenhuis voor heroperaties aan de aortaklep. N = 120
2 maand tot 1 jaar postoperatief
De patiëntkarakteristieken bij consultatie na 2 maand tot 1 jaar postoperatief werden weergegeven in Tabel 9. Deze patiëntenkarakteristieken bevatten onder ander de NYHA-klasse van de patiënt en morbiditeiten die optraden in de periode 2 maand tot 1 jaar postoperatief en tijdens een consultatie in het ziekenhuis werden vastgesteld. De 4 (3,05%) patiënten die overleden in de periode van 2 maand tot 1 jaar postoperatief werden bijkomend geëxcludeerd.
Zessentachtig (74,1%) patiënten waren in NYHA-klasse I en hadden dus geen beperking meer van de fysieke activiteit. Geen enkele patiënt was nog in NYHA-klasse IV.