GEZONDHEIDSECONOMISCHE
EVALUATIE VAN HORMOONGEBRUIK
IN DE MENOPAUZE
PARTIM CARDIOVASCULAIRE AANDOENINGEN,
PARTIM OSTEOPOROSE,
PARTIM BORSTAANDOENINGEN EN
PARTIM MATHEMATISCH MODEL
Inès De Roo
Elisabeth Schelfhout
Pauline Somers
Zoé Van Langenhove
Stamnummers:01510180 01506658 01409916 01410343
Promotors: prof. dr. Herman Depypere en prof. dr. Lieven Annemans
Masterproef voorgelegd in het kader tot het behalen van de graad Master of Medicine in de Geneeskunde
Deze pagina is niet beschikbaar omdat ze persoonsgegevens bevat.
Universiteitsbibliotheek Gent, 2021.
This page is not available because it contains personal information.
Ghent University, Library, 2021.
Voorwoord
We willen graag onze promotors prof. dr. Herman Depypere en prof. dr. Lieven Annemans bedanken voor de grote hulp bij het tot stand komen van deze masterproef. Zij waren immer paraat om vragen te beantwoorden en om ons te gidsen doorheen het proces.
Daarnaast willen we Nick Verhaeghe bedanken voor de hulp bij het opstellen van het Markovmodel en bij het uitvoeren van de sensitiviteitsanalyse. Ook Geert Schelfhout willen we bedanken voor de hulp bij problemen in verband met het model. Verder willen we dr. Glenn Van Langenhove bedanken voor het nalezen en corrigeren van onze masterproef.
Ten slotte willen we ook elkaar bedanken voor de samenwerking en goede sfeer binnen onze groep.
Inhoudsopgave
1. Abstract ... 1 2. Inleiding ... 2 2.1. Menopauze ... 2 2.2. Hormonale substitutietherapie (HST) ... 3 Evolutie van HST ... 3Huidig gebruik van HST ... 4
Effecten van HST op osteoporose ... 5
Effecten van HST op cardiovasculaire aandoeningen ... 6
Effecten van HST op borstkanker ... 8
3. Methodologie ... 10
3.1. Probleemstelling en doelstelling ... 10
3.2. Onderzoeksmethode ... 10
Zoekstrategie ... 11
Opbouw van het model ... 11
Gezondheidstoestanden ... 15
Populatie, cyclusduur en tijdshorizon ... 15
Klinische data ... 15 Economische data ... 20 Gezondheidseffecten ... 22 Kosteneffectiviteit ... 25 Sensitiviteitsanalyse ... 26 Probabilistische analyse ... 26 4. Resultaten ... 28 4.1. Kostenanalyse ... 28 4.2. Analyse gezondheidseffecten ... 29 4.3. Kosteneffectiviteitsanalyse ... 31 4.4. Sensitiviteitsanalyse ... 31 4.5. Probabilistische analyse ... 34 5. Conclusie ... 36 6. Discussie ... 37 7. Referentielijst ... 41
1
1. Abstract
Doelstelling: Het doel van deze masterproef bestaat erin een analyse te maken van de kosteneffectiviteit van hormonale substitutietherapie (HST) bij de menopauzale vrouw. Er wordt gekeken naar het effect van HST op menopauzale klachten, osteoporose, cardiovasculaire aandoeningen en borstkanker. Hierbij wordt de impact van HST op de levenskwaliteit van de vrouw en op de kosten voor de maatschappij bestudeerd.
De onderzoeksvraag is de volgende: “Is het gebruik van HST bij menopauzale vrouwen (ouder dan 50 jaar) kosteneffectief, rekening houdend met de effecten ervan op menopauzale klachten, osteoporose, coronaire hartziekte, beroerte en borstkanker indien gestart wordt met de behandeling binnen 10 jaar na de aanvang van de menopauze?”
Methodologie: De kosteneffectiviteitsanalyse wordt gemaakt op basis van een besliskundig model van het Markov-type, over een tijdshorizon van 20 jaar. De klinische en economische data nodig voor de analyse zijn verzameld via de elektronische databases Pubmed, Embase en Google Scholar door het gebruik van diverse relevante zoektermen.
Resultaten: De totale incrementele kost bedraagt €2053,64. De kost van coronaire hartziekten, osteoporose en osteoporotische fracturen is lager bij de interventiegroep, terwijl de kost van beroerte en borstkanker hoger is.
De interventie zorgt voor een verhoging van de levenskwaliteit met 0,1567 quality adjusted life
years (QALY’s). Er is een stijging van de levenskwaliteit ten gevolge van minder coronaire
hartziekte, osteoporose en osteoporotische fracturen in de interventiegroep, terwijl er een daling van de levenskwaliteit optreedt ten gevolge van beroerte en borstkanker.
De incrementele kosteneffectiviteitsratio (IKER) bedraagt €13 107,75 per QALY.
Conclusie: Aangezien in België vaak een drempelwaarde van €35 000 per QALY voor de kosteneffectiviteit van een behandeling wordt gehanteerd, kan de behandeling van menopauzale vrouwen met HST als kosteneffectief worden beschouwd ten opzichte van de situatie waarin behandeling wordt gegeven.
2
2. Inleiding
In 1880 bedroeg de levensverwachting van de Belgische vrouw 46,6 jaar. Dit betekent dat de eierstokken functioneel bleven gedurende het hele leven. Dankzij de verbeterde gezondheidszorg, het terugdringen van infectieziekten en ontwikkelingen op vlak van sociale zekerheid, voeding en onderwijs steeg de levensverwachting voor vrouwen in 2018 naar 83,7 jaar (1). Dit wil zeggen dat er tegenwoordig veel vrouwen een derde van hun leven in de menopauze doorbrengen, aangezien die gemiddeld optreedt op 51-jarige leeftijd. Dit fenomeen treedt echter niet op bij de man, omdat deze zijn hele leven lang hormonen blijft produceren.
2.1. Menopauze
Een vrouw bevindt zich in de menopauze wanneer ze een jaar amenorroe heeft doorgemaakt. Dit houdt in dat zij gedurende een jaar geen maandstonden heeft gehad. De stop van de menstruele cyclus treedt gewoonlijk niet abrupt op, maar wordt voorafgegaan door een periode waarin de cyclusduur grotere variaties aanneemt. Men spreekt daarom over de menopauzale transitie (2). Door de natuurlijke vermindering van de follikelreserve en de omgevende granulosacellen, die oestrogeen produceren, komen vrouwen in een periode van een verminderde hormonale productie. De lage waarde van oestrogeen in het bloed leidt tot een slechtere levenskwaliteit voor de vrouw op diverse gebieden, onder andere door oestrogeen-dervingssymptomen. Men rapporteert vasomotorische symptomen zoals opvliegers, ook tijdens de nacht, en vaginale droogte door atrofie van de mucosa (3). Behalve urogenitale atrofie kan er ook symptomatische atrofie ter hoogte van andere slijmvliezen, zoals in het neus-keel-oor-gebied, optreden (2). Andere mogelijke symptomen zijn slaapstoornissen, prikkelbaarheid, stijfheid van de gewrichten, botontkalking, daling van het libido, depressie, geheugen- en concentratieverlies en spier- en gewrichtspijn (3). De periode waarin er sprake is van een laag oestrogeengehalte gaat niet alleen gepaard met bovengenoemde symptomen, maar ook met een vergroot risico op cardiovasculaire aandoeningen (4). Zo wordt er een significante toename van de bloeddruk, het lipidengehalte in het bloed en het abdominaal vet geconstateerd. Een mogelijke verklaring voor de stijging van de bloeddruk is de daling van de oestrogenen, die normaliter bijdragen aan de vasodilatatie van de bloedvaten. Het verband tussen de oestrogeenspiegel en cardiovasculaire aandoeningen is echter minder duidelijk dan dat met osteoporose of borstkanker, wat gezien de multifactoriële etiologie van cardiovasculaire aandoeningen niet
3
verwonderlijk is. Toch is het duidelijk dat een vroege menopauze een hogere cardiovasculaire morbiditeit en mortaliteit met zich meebrengt. Ook de invloed van hormonen op borstkanker is complex. Recente inzichten tonen aan dat het later dan gemiddeld optreden van de menopauze of het toedienen van hormonen na de menopauze hoogstens een beperkte toename van het risico op borstkanker veroorzaken, maar het zou de borstkanker op zich niet induceren (2).
In een online bevraging aan 696 Belgische menopauzale vrouwen (45 tot 60 jaar oud) uit 2016 rapporteerde 77% van deze vrouwen last te hebben van menopauzale klachten. 40% van de vrouwen met meer dan drie symptomen bleef onbehandeld (5). De grote diversiteit en uitgebreidheid aan klachten duidt de nood aan het overwegen van behandeling.
2.2. Hormonale substitutietherapie (HST)
Evolutie van HST
Hormonale substitutietherapie (HST) bestaat reeds sinds de jaren ’60. Toen werd er voor het eerst gebruikgemaakt van oestrogeen als behandeling voor vrouwen in de menopauze. Een aantal jaren later werd het echter duidelijk dat het geven van oestrogeen zorgde voor een hogere incidentie van endometriumcarcinomen. Nadien werd ontdekt dat het associëren van een progestageen aan oestrogeen ervoor zorgde dat het risico op endometriumcarcinomen verlaagde. Hierdoor werd HST opnieuw frequent voorgeschreven, vooral om osteoporose te voorkomen (6, 7).
Rond 1990 werd aangenomen dat hormonale substitutietherapie voor een vermindering van cardiovasculaire aandoeningen en een daling van de algemene mortaliteit zorgde. Dit werd onderzocht in de Women’s Health Initiative (WHI) hormone therapy trials. Hierbij werd gebruik gemaakt van synthetisch oestrogeen in combinatie met een synthetisch progestageen. Deze studie toonde initieel echter aan dat er net een groter cardiovasculair risico bestond, met name door de toename van trombo-embolische aandoeningen. Verder werd er een toename van het risico op borstkanker bij de combinatietherapie (oestrogeen en progestageen) vastgesteld, terwijl monotherapie (enkel oestrogeen) de kans op borstkanker significant verminderde. Er werd geen significant effect op de mortaliteit bij het gebruik van HST gerapporteerd (7). De populatie vrouwen opgenomen in de WHI-studie bestond echter voor 65-70% uit vrouwen ouder dan 60 jaar en bovendien vertoonde slechts 12% van de vrouwen matige of ernstige vasomotorische symptomen. Het hebben van vasomotorische klachten was een exclusiecriterium om deel te nemen aan de WHI-studie, aangezien het niet ethisch zou zijn om deze vrouwen gedurende vijf jaar placebo te geven. (2).
4
Uit de 18 jaar durende follow-up van de WHI-studie volgde de geruststelling dat toediening van hormonen aan menopauzale vrouwen niet gepaard ging met significante verschillen in algemene, cardiovasculaire en kanker-gerelateerde mortaliteit. De algemene mortaliteit werd nadien ook onderzocht in de verschillende leeftijdsgroepen. Het starten met HST bij jonge menopauzale vrouwen (50-59 jaar) vermindert de totale mortaliteit met bijna 40% ten opzichte van vrouwen van dezelfde leeftijdscategorie in de placebogroep en ook ten opzichte van vrouwen die met HST starten op een leeftijd van 70-79 jaar.
Daarnaast is er ook minder osteoporose, minder dementie en is de totale mortaliteit ten gevolge van borstkanker (niet significant) lager. Na 18 jaar opvolging werd er nog steeds een reductie in de algemene mortaliteit opgemerkt, deze was echter niet significant (6, 7).
Huidig gebruik van HST
Hormonale substitutietherapie kan gegeven worden aan vrouwen die de menopauze bereikt hebben aangezien de eigen oestrogeenproductie vanaf dat moment vrijwel volledig stil is gevallen. Lage doseringen volstaan om bij de meerderheid van de vrouwen een redelijke respons te bereiken, hoewel de onderzochte effecten dosisafhankelijk zijn. Zo zijn de dosissen oestradiol frequent lager dan 1 mg per dag bij orale toediening of tussen 25 en 50 µg per dag bij transdermale toediening. Na 12 weken wordt de dosis indien nodig verhoogd, aangezien de plateau-respons dan intreedt (2).
Er zijn twee mogelijke types van behandeling. De eerste is een behandeling met natuurlijke oestrogenen (oestradiol) of geconjugeerde equine oestrogenen (CEE). De tweede optie is een combinatie van natuurlijke oestrogenen (oestradiol) met een progestatief (natuurlijk progesteron of een synthetisch progestageen: medroxyprogesteronacetaat, dydrogesteron, norethisteron, …). Deze twee verschillende vormen hebben een andere indicatie. De hormoontherapie met alleen oestrogeen wordt gegeven aan vrouwen die een hysterectomie ondergingen of een hormoonspiraal (Mirena® of Kyleena®) hebben. De combinatietherapie van progestagenen met oestrogenen wordt gegeven aan vrouwen die nog een (intacte) uterus hebben om endometriumcarcinomen te voorkomen (8). De therapie toont een heel complexe spreiding van zowel voor- als nadelen op diverse eindpunten, sommige daarvan kunnen verschillen op basis van het type hormoon dat gegeven wordt (8-10).
Bij elke vrouw moeten de consequenties van die relatieve oestrogeendeficiëntie afgewogen worden tegenover het potentieel risico van de hormoonbehandeling. Er moet ook rekening gehouden worden met de impact op het levenslang risico op het ontwikkelen van hart- en
5
vaatziekten, beroerte, botbreuken en borst- of endometriumcarcinomen (9, 10). De risico’s en de voordelen van HST hangen af van de leeftijd van de vrouw en de tijd sinds de start van de menopauze. Ook het type van hormoontherapie zou belangrijk zijn voor het risico op borstcarcinomen (11).
De behandeling van de vasomotorische symptomen blijft de belangrijkste indicatie voor hormonale substitutietherapie met oestrogenen met of zonder progestagenen. Het blijkt effectief te zijn bij vrouwen met overgangsklachten aangezien de therapie de frequentie en ernst van de warmteopwellingen vermindert samen met andere veel voorkomende klachten zoals urogenitale atrofie, concentratiestoornissen en nachtzweten. Daarnaast heeft het ook een positief effect op de gemoedstoestand en de nachtrust, wat bijdraagt tot een verbetering van de levenskwaliteit (8, 9, 11).
Effecten van HST op osteoporose
HST heeft een positief effect op de preventie en behandeling van osteoporose met een significante daling in het aantal breuken. De daling is het grootst wanneer de therapie snel in de menopauze opgestart wordt (8).
Zoals reeds hogerop aangehaald, zorgt de lage oestrogeenwaarde in de menopauze voor een verlies van botmineraaldensiteit. Oestrogeen zorgt voor inhibitie van de osteoclasten, dit zijn de cellen die zorgen voor botafbraak. Osteoporose ontstaat door een toegenomen afbraak door de osteoclasten en afgenomen opbouw door de osteoblasten (dit zijn de cellen die zorgen voor botaanmaak). Hierdoor treedt verlies van botmassa op en wordt de normale architectuur van het bot onderbroken. Dit leidt tot botbroosheid en een groter risico op botfracturen. De meest voorkomende fracturen ten gevolge van osteoporose zijn gelokaliseerd ter hoogte van de heup, wervelzuil, voorarm en bovenarm.
De risicofactoren voor het ontwikkelen van osteoporose zijn het vrouwelijk geslacht, de menopauze, de leeftijd, de inname van glucocorticoïden (gedurende meer dan 3 maand), de etniciteit en voorafgaande fracturen. Daarnaast zijn er nog veranderlijke risicofactoren, namelijk een calcium- of vitamine D-tekort en levensstijlkeuzes zoals alcoholinname, roken, dieet en fysieke activiteit.
Eén op drie vrouwen zal te maken hebben met een botbreuk ten gevolge van osteoporose. Voornamelijk breuken van de heup en wervel liggen aan de basis van de toegenomen morbiditeit en mortaliteit (12).
6
Effecten van HST op cardiovasculaire aandoeningen
95% van de vrouwen die hart- en vaatziekten ontwikkelen zijn menopauzaal. Zo heeft de menopauzale vrouw 2,6 keer meer risico op cardiovasculaire events in vergelijking met premenopauzale leeftijdsgenoten. Hiervoor zijn er meerdere mogelijke verklaringen. Veroudering is de belangrijkste risicofactor in kader van het ontwikkelen van cardiovasculaire events. Maar ook een verhoogde bloeddruk, een verhoogd lipidengehalte in het bloed, drager zijn van het APO-A4 allel en een verstoord suikermetabolisme zijn belangrijke cardiovasculaire risicofactoren (13, 14). De menopauze op zich verhoogt eveneens het risico. Het oestrogeen geproduceerd tijdens de reproductieve fase van de vrouw heeft veel voordelige en beschermende effecten. Het heeft een anti-atherosclerotische werking en anti-inflammatoire eigenschappen waardoor de plaque-vorming daalt. Daarenboven draagt het bij tot de endotheel-gemedieerde vasodilatatie. Het verlies aan endogeen oestrogeen tijdens de menopauze heeft een negatief effect op het lipidenprofiel. Het low density lipoprotein (LDL) en de triglyceriden nemen toe en het high density lipoprotein (HDL) neemt af in concentratie. Daarnaast treden ook heel wat andere veranderingen op vanaf de menopauze, zoals een toename in gewicht, een verandering van de vetverdeling, een stijging van de bloeddruk en nog heel wat andere metabole factoren. Het risico op cardiovasculaire events ligt nog hoger bij vrouwen die heel vroeg (jonger dan 40-45 jaar) de menopauze bereiken en bij vrouwen die premenopauzaal een oestrogeenspiegel hebben die lager is dan gemiddeld (10, 15).
Doordat menopauzale vrouwen cardiovasculaire risicofactoren ontwikkelen, stijgt het risico op het doormaken van een beroerte. Een beroerte of cerebrovasculair accident (CVA) is een stoornis in de bloedvoorziening van de hersenen waarbij een deel van de hersenen te weinig zuurstof krijgt met als gevolg dat hersencellen in het zuurstofarme gebied kunnen afsterven. Zo kunnen hersenfuncties tijdelijk of levenslang verloren gaan. Beroerte is een belangrijke oorzaak van tijdelijke en blijvende invaliditeit en ook de vierde belangrijkste doodsoorzaak. De voornaamste risicofactoren zijn leeftijd, roken, dyslipidemie, diabetes, obesitas en genetische factoren. Daarnaast is er een lineaire relatie tussen de bloeddruk en het risico op een beroerte. Premenopauzale vrouwen hebben een zeer kleine kans op het doormaken van een CVA, maar het risico vergroot met toenemende leeftijd. Het risico op een beroerte verdubbelt zelfs in de 10 jaar na het begin van de menopauze en vrouwen die een vroege menopauze doormaken hebben een nog hoger risico (16). Bij een blanke vrouw met een leeftijd van 45 tot 54 jaar wordt het risico geschat op 0,59 tot 1,02 per 1000 vrouwen per jaar (17). Daarom is het begin van de menopauze het ideale moment om in te zetten op de preventie van beroertes. Het geven van oestrogeen in een lage dosis gaat het risico op beroerte niet verhogen (16). Andere belangrijke cardiovasculaire aandoeningen zijn de coronaire hartziekten. Deze ontstaan wanneer er een onevenwicht is tussen de bloedvoorziening en de zuurstofnood van
7
de hartspier. De bloedstroom kan verstoord worden door een mechanische obstructie zoals een trombose, spasme, embool of een vernauwing van de bloedvaten. Een obstructie is vaak het gevolg van atherosclerose. Coronaire hartziekten kunnen aanleiding geven tot een brede variatie van klinische presentaties, gaande van stabiele angor tot acuut myocardinfarct, waardoor ze ook bijdragen tot de cardiovasculaire morbiditeit en mortaliteit (18).
Cardiovasculaire mortaliteit vormt de belangrijkste doodsoorzaak in onze samenleving. Het cardiovasculaire sterfterisico bij de normale Belgische vrouwelijke populatie bedraagt 0,85% voor vrouwen tussen de 50-54 jaar en 1,58% in de leeftijdscategorie 55-59 jaar (13). Het risico op hart- en vaatziekten is zeer sterk afhankelijk van de leeftijd. In de jongere leeftijdsgroepen is het risico het grootst bij de mannelijke populatie maar het verschil tussen de geslachten daalt bij toenemende leeftijd doordat het cardiovasculair risico bij de vrouwen toeneemt in de menopauze. De prevalentie van sterfte door hart- en vaatziekten bij vrouwen binnen de leeftijdsgroep van 45-49 jaar bedraagt 0,18 op 1000. Dit aantal neemt licht toe tot de leeftijd van 60 jaar. Vanaf 60 jaar zien we een sterke stijging in prevalentie van mortaliteit en wanneer de leeftijd van 69 jaar bereikt wordt, zien we een exponentiële stijging in sterfte aan hart- en vaatziekten (10).
De resultaten van HST omtrent de effecten op hart- en vaatziekten zijn zeer tegenstrijdig. Er zijn geen bewijzen uit observationele studies van jarenlange opvolging dat hormoontherapie dat het risico op hart- en vaatziekten verhoogt als de therapie gestart wordt rond het begin van de menopauze. Sterker nog, observationele studies hebben op lange termijn voordelen aangetoond op vlak van hart- en vaatziekten en de algemene mortaliteit (19). Door het gebruik van HST tijdens de menopauze daalt de mortaliteit door alle oorzaken met 20-40% en is er een reductie van 30% van het cardiovasculaire risico (20% na 7,5 jaar en 40% na 15 jaar) (8, 9). Het is echter zo dat de gerandomiseerde trials (RCT) geen verbetering aantonen op vlak van cardiovasculaire morbiditeit en mortaliteit (13). Een mogelijke verklaring hiervoor is dat de vrouwen die deelnamen aan de RCT’s vaak ouder waren en de gemiddelde leeftijd veel hoger was in vergelijking met de leeftijd van de vrouwen uit de observationele studies (19). De vroegere grote RCT’s (Heart and Estrogen/progestin Replacement Sudy (HERS)-studie en WHI-studie) konden niet bewijzen dat er een positief effect was van hormonale substitutietherapie op cardiovasculaire preventie. Meer recente studies en sub-analyses van deze gerandomiseerde studies hebben echter een nieuwe term geïntroduceerd, namelijk de
timing hypothese (19). Deze hypothese stelt dat er een window of opportunity bestaat waarin
het voordelig is om met de behandeling te starten. Als de hormoontherapie toegediend wordt vroeg na de start van de menopauze en/of bij jonge vrouwen, worden gunstige effecten bekomen, maar mogelijk is de therapie schadelijk als er op latere leeftijd of laat menopauzaal begonnen wordt. Hormoontherapie gegeven aan symptomatische menopauzale vrouwen jonger dan 60 jaar en gestart binnen de eerste 10 jaar van de menopauze levert het grootste
8
voordeel. HST vertraagt de progressie van atherosclerose indien het opgestart wordt tijdens de vroege menopauze (11). Aan de andere kant is het bekend dat, wanneer de coronaire arteriën reeds aangetast zijn door atherosclerose, de hormoontherapie kan zorgen voor plaque-instabiliteit. Het risico op aangetaste bloedvaten is groter op oudere leeftijd, daarom kan HST die opgestart is 10 jaar na aanvang van de menopauze meer kwaad dan goed doen (8-11). Bij het gebruik van HST bedraagt de odds ratio (OR) voor events door coronair lijden 0,68 (95% CI 0,48-0,96) wanneer het opgestart wordt minder dan 10 jaar na de menopauze en bij vrouwen jonger dan 60 jaar ten opzichte van de controlegroep waarbij er geen HST opgestart wordt. Wanneer het later dan 10 jaar na de menopauze en bij vrouwen ouder dan 60 jaar opgestart wordt, bedraagt de OR 1,03 (95% CI 0,91-1,16). Bij de vergelijking tussen HST bij jongere en oudere menopauzale vrouwen bedraagt de OR 0,66 (95% CI 0,46-0,95) (20). Bij de vrouwen die gestart zijn met HST minder dan 10 jaar na de menopauze is de mortaliteit lager (RR 0,70; 95% CI 0,52-0,95) en is er minder kans op coronaire hartziekte (RR 0,52; 95% CI 0,29-0,96). Er is echter wel een verhoogd risico op veneuze trombo-embolie (RR 1,74; 95% CI 1,11-2,73) bij het gebruik van hoog gedoseerde orale preparaten (10).
Effecten van HST op borstkanker
Hormonale substitutietherapie blijkt dus een positief effect te hebben op osteoporose en cardiovasculaire aandoeningen, wanneer er vroeg in de menopauze mee gestart wordt. Het is echter ook belangrijk om het effect ervan op borstkanker na te gaan.
Borstkanker is de meest voorkomende kanker bij niet-rokende vrouwen. De meerderheid van de borstkankers ontstaan uit de epitheelcellen van de melkkanalen. De meest voorkomende tumor die hieruit ontstaat is het infiltrerend ductaal carcinoom (16).
In België worden er jaarlijks ongeveer 10 500 nieuwe gevallen van borstkanker geregistreerd. Elk jaar overlijden er meer dan 2300 mensen aan borstkanker. Ongeveer één vrouw op negen zal borstkanker krijgen voor de leeftijd van 75 jaar. Het is de meest voorkomende vorm van kanker bij vrouwen. Bij een langdurig gebruik van hormonale substitutietherapie is er tijdens het gebruik een licht verhoogd risico op borstkanker. 5 à 10 jaar na de beëindiging van het gebruik is het risico weer genormaliseerd. Van 10 000 50-jarige vrouwen die geen hormonale substitutietherapie nemen, zullen er per jaar gemiddeld 36 à 37 vrouwen borstkanker krijgen. Wanneer deze vrouwen dit wel zouden nemen, komen er maximaal 7 à 8 vrouwen die borstkanker krijgen bij. Wanneer het gaat om 60-jarige vrouwen, zullen er per jaar gemiddeld 40 à 41 per 10 000 vrouwen borstkanker krijgen wanneer zij geen HST nemen en wanneer zij dat wel doen, komen er 9 à 10 bij. Bij 70-jarigen zijn er jaarlijks gemiddeld 34 à 35 per 10 000 vrouwen die borstkanker krijgen zonder de inname van HST en 8 à 9 vrouwen meer wanneer
9
zij HST gebruiken (20). Deze cijfers zijn inschattingen voor de inname van hoog gedoseerde oestrogenen in combinatie met synthetische progestagenen. De cijfers zijn anders, indien natuurlijk oestrogeen en natuurlijk progesteron gebruikt wordt. Het gebruik van oestrogeen zonder een progestageen zou de kans op borstkanker met 30% verminderen (21, 22). Voor vrouwen zonder verhoogd risico op borstkanker maar met ernstige menopauzale klachten kunnen de voordelen van HST opwegen tegen de verhoging van het risico op borstkanker (23).
Figuur 1: Absoluut aantal sterftes bij vrouwen van 0-90 jaar ten gevolge van de aandoeningen opgenomen in de studie (borstkanker, cardiovasculaire aandoeningen en osteoporose) (24)
Cardiovasculaire aandoeningen vormen nog steeds een veel grotere oorzaak van sterfte bij menopauzale vrouwen dan borstkanker en osteoporose (25). Het is dus belangrijk om het risico op cardiovasculaire aandoeningen bij menopauzale vrouwen te verminderen door het gebruik van HST. Het is aangetoond dat vrouwen die gedurende 10 jaar gerandomiseerd hormonale substitutietherapie hebben ontvangen, vroeg opgestart na de menopauze, een significant gedaald risico op mortaliteit, hartfalen en myocardinfarct hebben zonder een gestegen risico op kanker, veneuze trombo-embolie of beroerte (26).
10
3.
Methodologie
3.1.
Probleemstelling en doelstelling
Het doel van deze masterproef bestaat erin een analyse te maken van de kosteneffectiviteit van hormonale substitutietherapie bij de menopauzale vrouw. Er wordt gekeken naar het effect van HST op menopauzale klachten op korte termijn, op osteoporose, op cardiovasculaire aandoeningen en op borstkanker. Hierbij wordt de impact van HST bestudeerd wat betreft de levenskwaliteit van de vrouw en de kosten voor de maatschappij.
De gezondheidseconomische evaluatie wordt gemaakt aan de hand van een nieuw opgesteld economisch model van het Markov-type. Dit model omvat een vergelijking tussen het geven van hormoonbehandeling aan menopauzale vrouwen (deze behandeling wordt gegeven vanaf de leeftijd van 50 jaar tot 64 jaar) en het niet geven van deze behandeling.
Gezondheidseconomische analyses zijn van aanzienlijk belang in de evaluatie van nieuwe behandelingen. In dit kader worden de gezondheidseffecten van de interventie afgewogen tegen de verschillende kosten die ermee gepaard gaan. Kosten worden uitgedrukt in euro’s, gezondheidseffecten in quality-adjusted life years (QALY’s). De kosten die gepaard gaan met het toepassen van de interventie (in dit geval het geven van hormonale substitutietherapie) worden vergeleken met de kosten indien geen interventie wordt toegepast. Het verschil tussen beiden wordt benoemd als de incrementele kost. Dezelfde berekening wordt uitgevoerd voor de QALY’s, zo bekomt men het incrementele aantal QALY’s. Door de incrementele kost te delen door de incrementele QALY wordt de incrementele kosteneffectiviteitsratio (IKER) bekomen, dit is met andere woorden de extra kost per gewonnen QALY.
De onderzoeksvraag van deze masterproef is de volgende: “Is het gebruik van HST bij menopauzale vrouwen (ouder dan 50 jaar) kosteneffectief rekening houdend met de effecten ervan op menopauzale klachten, osteoporose, coronaire hartziekte, beroerte en borstkanker indien gestart wordt met de behandeling binnen 10 jaar na de aanvang van de menopauze?”
3.2. Onderzoeksmethode
De kosteneffectiviteitsanalyse wordt gemaakt op basis van een besliskundig model van het Markov type. Markov modellen zijn door de intuïtieve wijze waarop zij zowel gezondheidsuitkomsten als kosten behandelen, bijzonder geschikt
11
voor gezondheidseconomische evaluaties. Met name in chronische aandoeningen kennen deze modellen waardevolle toepassingen (27).
Een Markov model wordt gedefinieerd door drie belangrijke kenmerken: de verschillende toestanden waarin de patiënt zich kan bevinden, de transitiekansen tussen deze toestanden en de cyclus waarop de transitiekansen betrekking hebben. Patiënten bevinden zich op elk moment in één van de toestanden beschreven in het model, dit zijn de verschillende aandoeningen opgenomen in het model. Naarmate de tijd vordert, kan men ofwel in diezelfde toestand blijven, ofwel opschuiven naar een andere toestand. De overgangen tussen de verschillende toestanden worden transities genoemd en zijn onderhevig aan bepaalde kansen, de zogenaamde transitiekansen. Transitiekansen worden berekend over een welbepaalde periode of cyclus. Wanneer men de som van alle perioden berekent, bekomt men totale duurtijd van het model (28).
Zoekstrategie
De voornaamste bronnen van artikels gebruikt in deze thesis waren de elektronische databases Pubmed, Embase en Google Scholar. Er werd gezocht door middel van verschillende combinaties van volgende zoektermen: ‘menopause’, ‘menopausal hormone
replacement therapy’, ‘HRT’, ‘estrogen’, ‘menopausal women’, ‘Belgium’, ‘Belgian women’,
‘menopausal symptoms’, ‘menopausal osteoporosis’, ‘osteoporosis’, ‘osteoporotic fractures’, ‘breast cancer’, ‘stroke’, ‘coronary heart disease’, ‘epidemiology’, ‘incidence’, ‘mortality’, ‘relative risk’, ‘relative risk reduction’, ‘hazard ratio’, ‘Markov model’, ‘cost’, ‘cost-effectiveness’, ‘quality of life’, ‘quality adjusted life years’, ‘utility scores’ en ‘utilities’. Er werd eveneens verder gezocht via de ‘sneeuwbalmethode’ bij relevante artikels. Er werd gefilterd op publicaties waarvan de full text beschikbaar was. Alleen Engelstalige artikels werden gebruikt. De resultaten werden manueel gefilterd op titel en abstract.
Opbouw van het model
Een Markovmodel laat toe in te schatten hoeveel van de patiënten zich op elk moment in een bepaalde toestand bevinden. Er worden in realiteit twee modellen met elkaar vergeleken: één model voor vrouwen die behandeld worden met HST en één model voor vrouwen die geen hormoontherapie krijgen. Kortom is het de bedoeling om de proportie gezonde, zieke en overleden patiënten op lange termijn te vergelijken tussen beide groepen. Deze proporties
12
worden vervolgens gebruikt om de totale kost en de totale kwaliteitsvolle levensverwachting (in QALY’s) met en zonder behandeling te berekenen.
Aan de start van het model bevindt elke vrouw zich in de toestand ‘at risk’, geen enkel individu heeft op dit moment één van de besproken aandoeningen. Gedurende iedere cyclus die volgt, vinden er verplaatsingen (transities) plaats tussen de verschillende toestanden, dit wordt voorgesteld in figuur 2. Elk gezond individu is onderhevig aan een bepaalde kans op het ontwikkelen van één van de aandoeningen, dan wel op sterfte. Deze kansen worden de transitiekansen genoemd en gelden voor het verloop van een afzonderlijke cyclus. Per cyclus kan elk individu in het model slechts één transitie doormaken, het is bijvoorbeeld niet mogelijk dat een vrouw in eenzelfde cyclus borstkanker ontwikkelt én een myocardinfarct doet. Er wordt bovendien vanuit gegaan dat alle transitiekansen over de volledige duurtijd van het model constant blijven.
Voor de verschillende toestanden wordt er een opdeling gemaakt tussen het eerste jaar waarin de aandoening is opgetreden en de verdere opvolging ervan. Hiervoor wordt gekozen omdat de kosten, de mortaliteit en de levenskwaliteit van aandoeningen in het eerste jaar sterk kunnen verschillen met deze in de verdere opvolging.
Zo zal een vrouw die op een gegeven moment borstkanker ontwikkelt, zich gedurende deze cyclus verplaatsen naar de toestand ‘borstkanker’. In de cyclus die daarop volgt, resten voor de vrouw twee mogelijke opties: ofwel kan de vrouw in de verdere opvolging terecht komen (‘borstkanker +’), ofwel kan ze overlijden (‘dood’).
Wanneer een individu in het model de diagnose van osteoporose krijgt, kan ze in de daaropvolgende cyclus overgaan naar de toestand osteoporose met een pathologische fractuur (‘fracturen’). Het is anderzijds ook mogelijk dat een vrouw met osteoporose geen fractuur doet. Dan blijft ze in dezelfde toestand als voorheen, namelijk ‘osteoporose’. Indien een vrouw wel een fractuur doet, blijft ze dus één cyclus in de toestand ‘fracturen’, om daarna automatisch in de opvolging (‘fracturen +’) te belanden. Uiteraard is het ook hier mogelijk om rechtstreeks vanuit de toestand ‘osteoporose’, ‘fracturen’ of ‘fracturen +’ over te gaan naar de eindtoestand ‘dood’.
Een persoon die op een gegeven moment coronaire hartziekte ontwikkelt, blijft gedurende één cyclus in deze toestand (‘CHZ’). In de daaropvolgende cyclus kan naar de opvolging overgegaan worden (‘CHZ +’), dan wel naar de eindtoestand ‘dood’. Patiënten die een beroerte doormaken, zullen het model op een analoge wijze doorlopen.
13
Een Markovmodel beschrijft niet alleen de kansen om na een welbepaald aantal cycli in een welbepaalde gezondheidstoestand terecht te komen, het beschrijft ook de kosten en de levenskwaliteit die met elk van deze toestanden gepaard gaan.
In het model worden volgende gezondheids- en ziektetoestanden geïncludeerd: 1. Gezond (at risk)
2. Coronaire hartziekte (CHZ)
3. Coronaire hartziekte, opvolging (CHZ+) 4. Cerebrovasculair accident (Beroerte)
5. Cerebrovasculair accident, opvolging (Beroerte+) 6. Borstkanker
7. Borstkanker, opvolging (Borstkanker+) 14. Osteoporose
15. Osteoporose met pathologische fracturen (Fracturen)
16. Osteoporose met pathologische fracturen, opvolging (Fracturen+) 17. Dood
14 Figuur 2: Pijlenschema evolutie aandoeningen
15
Omdat de aanwezigheid van menopauzale klachten een belangrijk effect kan hebben op de levenskwaliteit van de vrouw, wordt in het model een opdeling gemaakt tussen vrouwen met en vrouwen zonder menopauzale klachten. De proportie vrouwen met menopauzale klachten zal kleiner zijn in de groep die hormoonsubstitutie krijgt, dit heeft impact op de levenskwaliteit. In het model wordt ervanuit gegaan dat het enige verschil tussen vrouwen met en zonder menopauzale klachten in de levenskwaliteit vervat zit. De transitiekansen, kosten, utiliteiten en de relatieve risicoreducties (RRR) door hormoonbehandeling voor de verschillende aandoeningen blijven voor beide groepen gelijk.
Gezondheidstoestanden
In het model wordt coronaire hartziekte (CHZ) gedefinieerd als een acuut myocardinfarct of ischemische hartziekte met of zonder angina. Onder de toestand beroerte worden zowel een ischemisch als een hemorragisch cerebrovasculair accident (CVA) opgenomen. Borstkanker wordt voor de eenvoud van het model niet ingedeeld in primaire en gemetastaseerde tumoren, maar geïnterpreteerd als invasieve borstkanker. Osteoporose met en zonder fracturen wordt, omwille van het grote verschil in kosten, mortaliteit en levenskwaliteit, in afzonderlijke gezondheidstoestanden besproken. Er wordt opnieuw voor de eenvoud van het model geen onderscheid gemaakt tussen de verschillende types fracturen, deze worden gezamenlijk ondergebracht in een enkele toestand ‘fracturen’.
Populatie, cyclusduur en tijdshorizon
De gekozen populatie in het model betreft menopauzale Belgische vrouwen, met een leeftijd van 50 jaar of ouder. De interventiegroep omvat vrouwen die met hormoonbehandeling gestart zijn binnen 10 jaar na aanvang van de menopauze. De duur van een cyclus is arbitrair vastgelegd op 1 jaar. Het model bestaat uit 20 cycli en beschrijft dus een opvolging van 20 jaar.
Klinische data
Omdat het risico op het ontwikkelen van de aandoeningen opgenomen in het model en het risico op sterven aan of met deze aandoeningen afhankelijk zijn van de leeftijd, wordt er
16
gebruik gemaakt van leeftijdscategorieën in het model. Er wordt gewerkt met categorieën van 5 jaar. De eerste leeftijdscategorie bestaat met andere woorden uit vrouwen van 50 tot 54 jaar, de laatste categorie uit vrouwen van 80 tot 84 jaar. In het model zijn de transitiekansen voor elke aandoening opgedeeld in deze leeftijdsklassen. De transitiekansen zijn gebaseerd op probabiliteiten afkomstig uit epidemiologisch onderzoek en nationale registers.
3.2.5.1. Prevalentie menopauzale klachten
Onderzoek bij menopauzale vrouwen tussen 45 en 60 jaar toont aan dat 23% van de vrouwen geen impact ondervindt van de menopauze op de levenskwaliteit. Daartegenover rapporteert 77% van de vrouwen wel degelijk last te hebben van klachten (5). De gemiddelde duur van menopauzale klachten bedraagt 7 jaar (29).
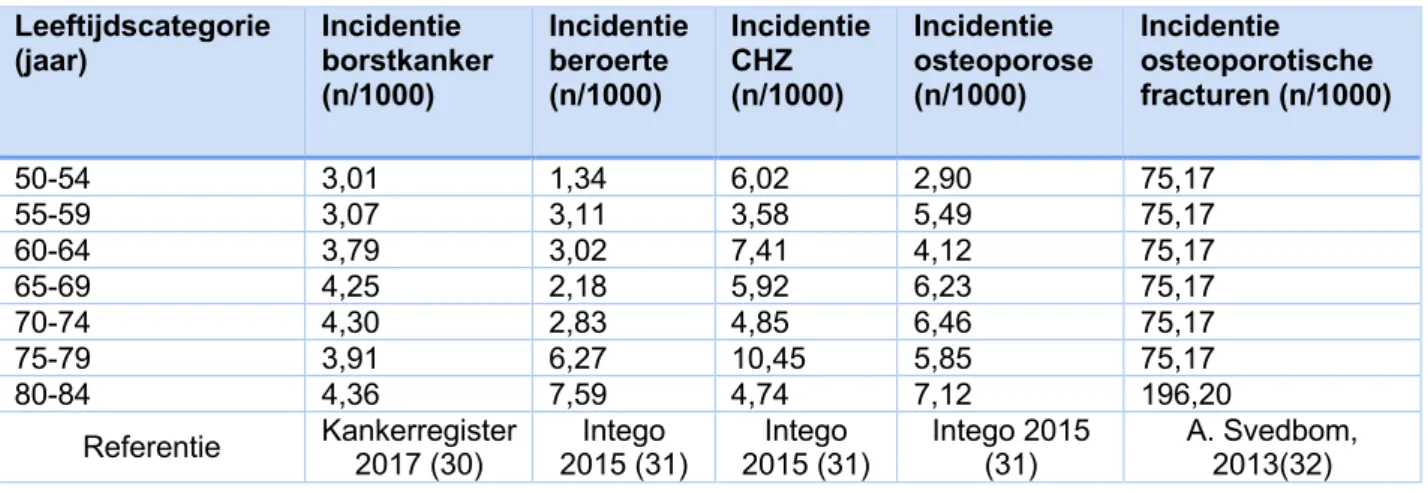
3.2.5.2. Incidentie
De leeftijdsspecifieke incidentie voor borstkanker is te raadplegen op de site van het Belgisch Kankerregister. Deze cijfers dateren van 2017 (30).
De leeftijdsspecifieke incidentie van osteoporose en beroerte is beschikbaar via het Vlaams huisartsenregistratienetwerk Intego, een online raadpleegbare databank van de KU Leuven met verzamelde Vlaamse epidemiologische gegevens sinds 1994. De gebruikte incidentiecijfers zijn deze van de jaarlijkse contactgroep (per 1000 patiënten) en dateren van 2015. Voor de incidentie van CHZ wordt eveneens deze databank geraadpleegd. Hierbij wordt de som genomen van de incidentiecijfers van ischemische hartziekte met en zonder angor en van acuut myocardinfarct (31)
.
De leeftijdsspecifieke incidentie van osteoporotische fracturen is berekend op basis van de incidentiecijfers van fracturen bij Belgische vrouwen gevonden in de literatuur (32). Hiervoor wordt de volgende berekening uitgevoerd. De incidentie van fracturen bij de Belgische vrouwen wordt vermenigvuldigd met het aantal Belgische vrouwen in die leeftijdsklasse om de absolute aantallen fracturen te bekomen. Vervolgens worden deze absolute aantallen gedeeld door het aantal vrouwen met osteoporose per leeftijdsklasse. Er wordt een gewogen gemiddelde berekend voor de leeftijdscategorie 50-79 jaar en voor de leeftijdscategorie 80+ jaar. Dit resulteert in een geschatte incidentie van osteoporotische fracturen van 7,52% voor vrouwen van 50-79 jaar en van 19% voor vrouwen ouder dan 80 jaar.
17
Tabel 1: Leeftijdsspecifieke incidentiecijfers (per 1000 persoonsjaren) per aandoening bij Belgische vrouwen Leeftijdscategorie (jaar) Incidentie borstkanker (n/1000) Incidentie beroerte (n/1000) Incidentie CHZ (n/1000) Incidentie osteoporose (n/1000) Incidentie osteoporotische fracturen (n/1000) 50-54 3,01 1,34 6,02 2,90 75,17 55-59 3,07 3,11 3,58 5,49 75,17 60-64 3,79 3,02 7,41 4,12 75,17 65-69 4,25 2,18 5,92 6,23 75,17 70-74 4,30 2,83 4,85 6,46 75,17 75-79 3,91 6,27 10,45 5,85 75,17 80-84 4,36 7,59 4,74 7,12 196,20
Referentie Kankerregister 2017 (30) 2015 (31) Intego 2015 (31) Intego Intego 2015 (31) A. Svedbom, 2013(32)
3.2.5.3. Mortaliteit
De mortaliteitcijfers opgenomen in het model zijn berekend of uit de literatuur gehaald. De gemiddelde algemene mortaliteitcijfers van de verschillende aandoeningen gebruikt in het model zijn afkomstig van Statbel en dateren van 2018 (33).
De mortaliteit voor vrouwen ‘at risk’ is de kans op sterfte veroorzaakt door aandoeningen die niet in het model zijn opgenomen. Dit komt neer op de algemene mortaliteit zonder het aandeel van de sterfte ten gevolge van de verschillende aandoeningen in het model. Dit aandeel van de sterfte veroorzaakt door andere aandoeningen wordt berekend aan de hand van de ‘Statistiek van doodsoorzaken in België 2016’ (24).
Voor elke aandoening wordt het onderscheid gemaakt tussen mortaliteit in het eerste jaar met de aandoening en na het eerste jaar met dezelfde aandoening.
De leeftijdsspecifieke mortaliteit in het eerste jaar en na het eerste jaar voor beroerte en CHZ zijn gebaseerd op deze in een gelijkaardig Markovmodel van N. Verhaeghe et al. (34-37).
De conditionele mortaliteit van osteoporose komt nagenoeg overeen met de sterfte in de groep vrouwen die ‘at risk’ zijn. Hiervoor wordt het aantal sterftes ten gevolge van osteoporose zonder fracturen (dit is nagenoeg 0), opgeteld bij het aantal sterftes veroorzaakt door andere ziektetoestanden die niet in het model zijn opgenomen. Deze cijfers zijn afkomstig van Statbel (24).De conditionele mortaliteit van een bepaalde aandoening omvat namelijk het aantal sterftegevallen met deze aandoeningen, niet direct als gevolg van deze aandoening. Daarom
18
wordt voor de verschillende aandoeningen de natuurlijke mortaliteit voor de leeftijdscategorie in kwestie steeds mee in rekening gebracht.
Voor de berekening van de mortaliteit in het eerste jaar na osteoporotische breuken wordt er beroep gedaan op Belgische gegevens over fracturen in het algemeen. Het totaal aantal sterftes in het eerste jaar te wijten aan fracturen wordt gedeeld door het totaal aantal fracturen in België 2010 (32). Hierbij wordt vervolgens per leeftijdscategorie de natuurlijke mortaliteit opgeteld, zodat deze berekening aanduidt hoeveel mensen sterven met de aandoening. De leeftijdsspecifieke mortaliteit van osteoporotische fracturen na het eerste jaar is berekend aan de hand van de in de literatuur gevonden impact van verschillende types fracturen op de natuurlijke mortaliteit. Per type fractuur wordt er een factor toegekend die de verhoogde kans op sterfte ten opzichte van de natuurlijke sterfte weergeeft. Zo wordt er aangenomen dat heup- en klinische wervelfracturen de kans op sterfte met een factor 1,779 verhogen. Aan andere osteoporotische fracturen wordt er na 1 jaar geen verhoogde mortaliteit toegeschreven (38). In het Markovmodel wordt een eigen vermenigvuldigingsfactor gebruikt voor alle types fracturen. Hiervoor wordt er een gewogen gemiddelde factor berekend aan de hand van de frequentieverdeling van fracturen op Belgisch niveau (39). Deze factor wordt tenslotte voor elke leeftijdscategorie vermenigvuldigd met de natuurlijke mortaliteit. Dit geeft de volgende formule:
Mortaliteit ‘fracturen+’ = (21% x 1,779 + 14% x 1,779 + 65% x 1) x (natuurlijke mortaliteit per leeftijd).
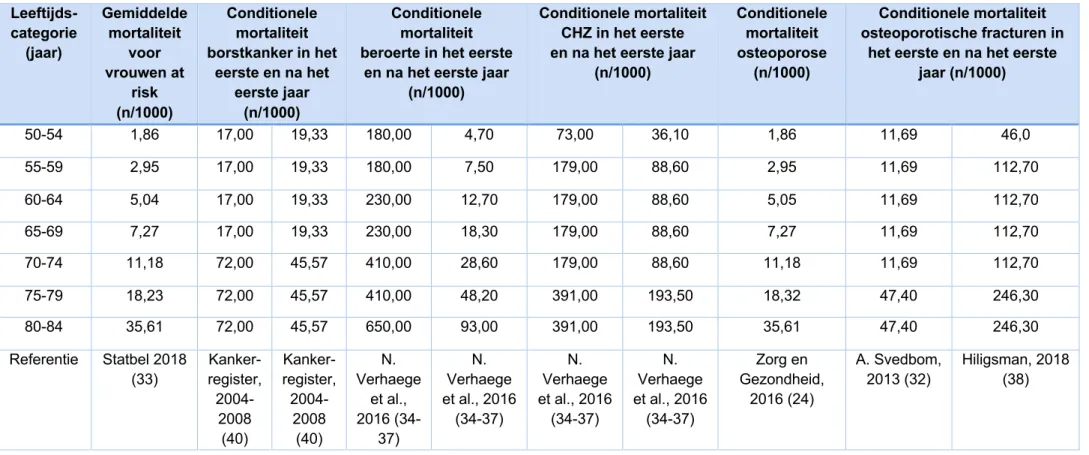
Een overzicht van de gehanteerde mortaliteitscijfers gebruikt in dit model, wordt weergegeven in tabel 2.
19
Tabel 2: Leeftijdsspecifieke mortaliteitscijfers (per 1000 persoonsjaren) in het eerste jaar en na het eerste jaar (+) per aandoening bij Belgische vrouwen
Leeftijds-categorie (jaar) Gemiddelde mortaliteit voor vrouwen at risk (n/1000) Conditionele mortaliteit borstkanker in het eerste en na het eerste jaar (n/1000) Conditionele mortaliteit beroerte in het eerste
en na het eerste jaar (n/1000)
Conditionele mortaliteit CHZ in het eerste en na het eerste jaar
(n/1000) Conditionele mortaliteit osteoporose (n/1000) Conditionele mortaliteit osteoporotische fracturen in
het eerste en na het eerste jaar (n/1000) 50-54 1,86 17,00 19,33 180,00 4,70 73,00 36,10 1,86 11,69 46,0 55-59 2,95 17,00 19,33 180,00 7,50 179,00 88,60 2,95 11,69 112,70 60-64 5,04 17,00 19,33 230,00 12,70 179,00 88,60 5,05 11,69 112,70 65-69 7,27 17,00 19,33 230,00 18,30 179,00 88,60 7,27 11,69 112,70 70-74 11,18 72,00 45,57 410,00 28,60 179,00 88,60 11,18 11,69 112,70 75-79 18,23 72,00 45,57 410,00 48,20 391,00 193,50 18,32 47,40 246,30 80-84 35,61 72,00 45,57 650,00 93,00 391,00 193,50 35,61 47,40 246,30 Referentie Statbel 2018 (33) Kanker-register, 2004-2008 (40) Kanker-register, 2004-2008 (40) N. Verhaege et al., 2016 (34-37) N. Verhaege et al., 2016 (34-37) N. Verhaege et al., 2016 (34-37) N. Verhaege et al., 2016 (34-37) Zorg en Gezondheid, 2016 (24) A. Svedbom, 2013 (32) Hiligsman, 2018 (38)
20
3.2.5.4. Impact van hormonale substitutietherapie
Om na te gaan welk effect hormonale substitutietherapie heeft op de verschillende aandoeningen wordt er gebruikt gemaakt van relatieve risico’s (RR). Deze RR’s zijn afkomstig uit de literatuur. In tabel 3 worden de RR’s opgenomen in het model met hun overeenkomstige referentie weergegeven. Het RR van osteoporose is gebaseerd op het RR van fractuur afkomstig uit de literatuur. Hiervoor wordt gekozen omdat osteoporose pas symptomatisch wordt wanneer er een osteoporotische fractuur optreedt. Dit is gewettigd aangezien de kans op fractuur evenredig daalt met de kans op osteoporose.
Tabel 3: RR per aandoening met gebruik van HST
Aandoening RR (betrouwbaarheidsinterval) Referentie
CHZ 0,52 (0,29-0,96) Boardman et al. (10)
Beroerte 1,24 (1,1-1,41) Boardman et al. (10)
Borstkanker 1,00 (0.83-1,22) Fournier et al., 2008 (41)
Osteoporose met fracturen 0,76 (0,69-0,83) Manson et al., 2015 (42, 43) Vasomotorische klachten 0,36 (0,27-0,49) Manson et al., 2013 (44)
Economische data
In het model wordt er gebruik gemaakt van de directe kost om de kost van elke aandoening en de kost van hormonale substitutietherapie te bepalen. De indirecte kost, zijnde de kost ten gevolge van ziekteverzuim, wordt niet opgenomen in het model.
De kosten van cardiovasculaire aandoeningen en borstkanker zijn gebaseerd op deze weergegeven in een gelijkaardig Markovmodel van N. Verhaeghe (34-37). Deze kosten zijn opgesplitst in de kosten in het eerste jaar met de aandoening en de kosten na het eerste jaar. Dit onderscheid is belangrijk aangezien de kosten in het eerste jaar hoger zijn. Daarbij worden de kosten eveneens geïndexeerd zodat deze vergelijkbaar zijn aan de waarde van de euro in 2019. De eerstejaarskost van CHZ bestaat uit de som van de kosten van zowel myocardinfarct, fataal myocardinfarct als onstabiele angina pectoris in het eerste jaar. De kost van CHZ na het eerste jaar omvat de som van de kosten van de follow-up van myocardinfarct en de follow-up van angina pectoris.
21
De kost van osteoporose wordt opgesplitst in de kost voor osteoporose en de kost voor fracturen. Beide komen uit ‘Osteoporosis in the Europian Union: a compendium of country-
specific reports’ (32).
Als kost van osteoporose wordt er gebruik gemaakt van de fracture prevention cost. Deze gerapporteerde kost wordt gedeeld door het aantal vrouwen met osteoporose om zo de kost voor één vrouw te bekomen.
Bij de kost van fracturen wordt er nogmaals een onderscheid gemaakt tussen de kost in het eerste jaar en na het eerste jaar. Om de kost per fractuur te berekenen, wordt de first year
fracture cost gedeeld door het totaal aantal fracturen in 2010. De kost na het eerste jaar wordt
op een vergelijkbare manier berekend, maar in plaats van de first year fracture cost wordt de
long term disability cost gebruikt.
Aangezien vrouwen nog steeds osteoporose hebben bij het optreden van een fractuur, zullen ze de behandeling hiervoor blijven nemen. Daarom is de kost hiervan telkens opgeteld bij de kost van ‘fracturen’ en ‘fracturen +’. De totale kost van fracturen wordt bekomen door de respectievelijke kost van elk type fractuur te vermenigvuldigen met de health status, die de distributie van alle types fracturen representeert. Opnieuw wordt de gezondheidsindexering toegepast.
De kost van hormonale substitutietherapie wordt als volgt bepaald. Er kan gekozen worden voor de orale toediening van oestrogeen in monotherapie gecombineerd met progesteron in monotherapie of voor de orale toediening van een combinatiepreparaat. Bij de eerste optie moet er van elk type monotherapie één pil ingenomen worden per dag. Bij de tweede optie, namelijk het combinatiepreparaat, wordt de dagdosis van zowel oestrogeen als progesteron in één pil verwerkt. Het gebruikte oestrogeenpreparaat Progynova® (estradiol oraal 1 mg) kost voor 3 maand €7,16 zonder remgeld. Het progesteronpreparaat Nogest® (nomegestrol oraal 5 mg) kost voor 3 maand €14,12 zonder remgeld. De combinatie van beide zorgt voor een totaalprijs van €88,38 op jaarbasis zonder remgeld, dit is dus de kost voor de verzekering. Het combinatiepreparaat Laclimella ® (estradiol + diënogest oraal 1 mg + 2 mg) daarentegen kost €71,80 voor 6 maand, wat een totaalprijs geeft van €143,60 op jaarbasis. Al deze kosten zijn afkomstig van het BCFI (45). Aangezien de kost van oestrogeen in monotherapie met progesteron in monotherapie goedkoper is, wordt hiervoor gekozen in het model. Vrouwen die behandeld worden met HST gaan gemiddeld tweemaal per jaar naar de huisarts voor opvolging van de behandeling. Daarom worden er bij de kost van HST twee consultaties per jaar met een geaccrediteerde huisarts bijgeteld. Hiervan bedraagt de kost zonder remgeld €44,54 (46). De kost van de behandeling samen met de kost van de consultaties geeft als totaalkost voor HST
€
132,92 op verzekeringsniveau.22
Het is noodzakelijk om rekening te houden met de discontovoet aangezien het Markovmodel een 20-jarige opvolging weergeeft. De discontovoet bedraagt jaarlijks 3%.
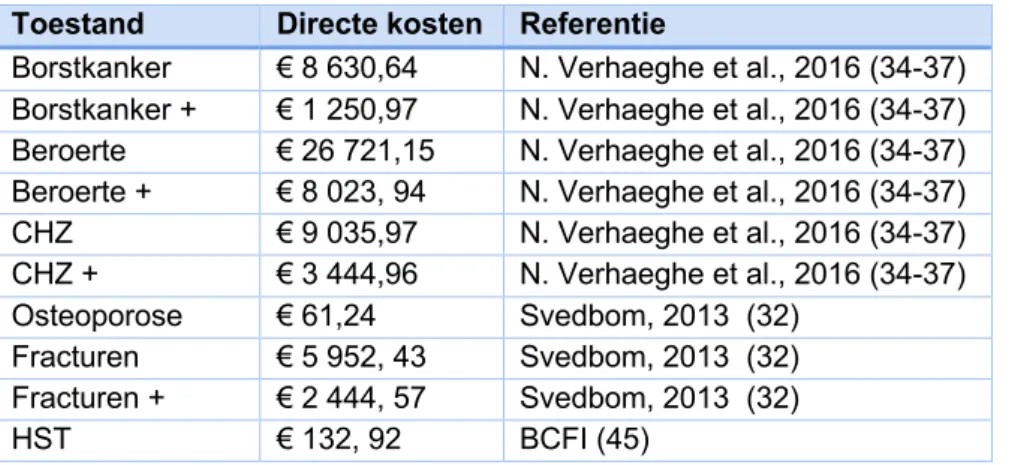
Een overzicht van deze kosten is te vinden in tabel 4.
Tabel 4: Kost per aandoening (in het eerste jaar en na het eerste jaar (+)) en kost interventie
Toestand Directe kosten Referentie
Borstkanker € 8 630,64 N. Verhaeghe et al., 2016 (34-37) Borstkanker + € 1 250,97 N. Verhaeghe et al., 2016 (34-37) Beroerte € 26 721,15 N. Verhaeghe et al., 2016 (34-37) Beroerte + € 8 023, 94 N. Verhaeghe et al., 2016 (34-37) CHZ € 9 035,97 N. Verhaeghe et al., 2016 (34-37) CHZ + € 3 444,96 N. Verhaeghe et al., 2016 (34-37) Osteoporose € 61,24 Svedbom, 2013 (32) Fracturen € 5 952, 43 Svedbom, 2013 (32) Fracturen + € 2 444, 57 Svedbom, 2013 (32) HST € 132, 92 BCFI (45)
Gezondheidseffecten
De gezondheidseffecten van de interventie worden ingeschat aan de hand van QALY’s, die op basis van utiliteiten worden berekend. Een utiliteit is een waarde gelegen tussen 0 (dood) en 1 (perfecte gezondheid) die de levenskwaliteit die ermee gepaard gaat, kwantificeert. Door de utiliteit van een bepaalde aandoening te vermenigvuldigen met het aantal jaar dat er geleefd wordt met die specifieke aandoening, wordt de gewenste QALY van de aandoening berekend.
De utiliteiten voor iedere aandoening worden opgedeeld per leeftijdscategorie, op basis van verschillende leeftijdsspecifieke basisutiliteiten voor gezonde vrouwen. Er wordt voor iedere aandoening een vaststaande ‘penalty’ bepaald, die van de leeftijdsafhankelijke basisutiliteit wordt afgetrokken om de uiteindelijke utiliteit per aandoening en per leeftijd te kunnen bepalen. Deze penalty’s worden weergegeven in tabel 5. De utiliteiten voor gezonde vrouwen worden gebaseerd op een analyse van Ruben Willems, die zich voor deze cijfers gebaseerd heeft op de Belgische gezondheidsenquête van 2018. De penalty’s voor de utiliteiten van ‘borstkanker’, ‘borstkanker +’, ‘beroerte’, ‘beroerte +’, ‘CHZ’ en ‘CHZ +’ komen uit het gelijkaardig Markovmodel van N. Verhaeghe. Hierbij moet vermeld worden dat deze gegevens niet van België zijn, maar afkomstig zijn uit buitenlandse literatuur. In het model wordt de utiliteit van ‘osteoporose’ gelijkgesteld aan de gezonde utiliteit. Hier is voor gekozen omdat er geen symptomen van osteoporose met impact op de levenskwaliteit aanwezig zijn tot de eerste fractuur optreedt (47). De utiliteiten van osteoporotische fracturen zijn berekend dankzij
23
multipliers gevonden in de literatuur (48). In de literatuur wordt de utiliteit van elke type breuk apart vermeld, maar in het model wordt er voor de eenvoud hierin geen onderscheid gemaakt. Daarom is er een gewogen gemiddelde utiliteit berekend op basis van de frequentiedistributie van de verschillende types fracturen op Belgisch niveau (39). De op deze manier bekomen totale multiplier wordt vervolgens vermenigvuldigd met de utiliteit voor gezonde vrouwen. Dit geeft de utiliteit van osteoporotische fracturen in het algemeen. Door het verschil tussen deze utiliteit en de gezonde utiliteit te nemen, wordt de penalty voor osteoporotische fracturen berekend. Om tot het eindresultaat te komen wordt de penalty voor de osteoporotische fracturen per leeftijdscategorie van de gezonde utiliteit afgetrokken.
Om de impact van menopauzale klachten op de levenskwaliteit in te schatten, wordt er gebruik gemaakt van utiliteiten voor vasomotorische klachten (49). Er wordt een algemene utiliteit voor vasomotorische klachten berekend uit de verschillende EQ-5D scores voor milde, matige en ernstige vasomotorische klachten. De formule voor het gewogen gemiddelde is de volgende: (EQ-5D milde ernst x aantal + EQ-5D matige ernst x aantal + EQ-5D ernstig x aantal) / (totaal aantal vrouwen met vasomotorische klachten).
Dit wordt vervolgens afgetrokken van de EQ-5D score voor vrouwen zonder vasomotorische klachten om zo de penalty te bekomen. Deze penalty (0,026) wordt ingevoerd in het model.
Tabel 5: penalty's op de gezonde utiliteit per aandoening
Toestand Penalty Referentie
CHZ 0,280 N. Verhaeghe et al., 2016 (34-37) Beroerte 0,340 N. Verhaeghe et al., 2016 (34-37) Borstkanker 0,235 N. Verhaeghe et al., 2016 (34-37) Osteoporose 0,000
Fracturen 0,163 M. Hiligsmann et al., 2017(48) Fracturen + 0,044 M. Hiligsmann et al., 2017(48) Menopauzale
klachten
0,026 J. Whiteley et al., 2013 (49)
Omdat het aantal vrouwen met menopauzale klachten lager is in de interventiegroep dan in de controlegroep, wordt het model opgesplitst. 77% van de Belgische vrouwen geeft aan dat de menopauze gepaard gaat met verminderde levenskwaliteit door het optreden van symptomen (5). De groep die hormonale substitutietherapie krijgt, zal in sterk verminderde mate last hebben van deze klachten. Er wordt gerekend met een risicoreductie van 64% (44). Op deze manier wordt er een verschillende basisutiliteit berekend voor de interventie- en de controlegroep. In beide groepen wordt een gewogen gemiddelde genomen van de utiliteit voor gezonde vrouwen en voor vrouwen met menopauzale klachten. De formule voor dit gewogen gemiddelde is de volgende:
24
Basisutiliteit = (proportie vrouwen met menopauzale symptomen x utiliteit menopauzale symptomen) + (proportie vrouwen zonder menopauzale symptomen x utiliteit indien geen menopauzale symptomen).
Zo bedraagt de utiliteit voor gezonde vrouwen van 45 tot 54 jaar in de algemene bevolking een waarde van 0,755 (50).
In de controlegroep heeft dus 77% van de vrouwen last van menopauzale klachten, zodat de basisutiliteit als volgt wordt berekend:
Basisutiliteit = 0,77 x (0,755 – 0,026) + 0,23 x 0,755 = 0,735.
In de interventiegroep wordt dit percentage verrekend met de risicoreductie door HST: Basisutiliteit = (0,77 x 0,36) x (0,755 – 0,026) + (1 – 0,77 x 0,23) x 0,755 = 0,748.
Een overzicht van de geïncludeerde utiliteiten in het gezondheidseconomisch model is voorgesteld in tabel 6. Tot de leeftijd van 64 jaar wordt er rekening gehouden met de effecten van menopauzale klachten op de levenskwaliteit, zoals hierboven beschreven. Na deze leeftijd wordt in het model verondersteld dat menopauzale klachten niet meer voorkomen (29).
25 Tabel 6: Utiliteit per toestand
Toestand 45-54 jaar 55-64 jaar 65- 74 jaar 75 + jaar Referentie
HST Controle HST Controle Gezond 0,748 0,735 0,751 0,738 0,747 0,620 Gezondheidsenquête 2018 (50) CHD 0,468 0,455 0,471 0,458 0,467 0,340 N. Verhaeghe et al., 2016 (34-37) CHD+ 0,468 0,455 0,471 0,458 0,467 0,340 N. Verhaeghe et al., 2016 (34-37) Stroke 0,408 0,395 0,411 0,398 0,407 0,280 N. Verhaeghe et al., 2016 (34-37) Stroke + 0,408 0,395 0,411 0,398 0,407 0,280 N. Verhaeghe et al., 2016 (34-37) Borstkanker 0,513 0,500 0,516 0,503 0,512 0,385 N. Verhaeghe et al., 2016 (34-37) Borstkanker + 0,513 0,500 0,516 0,503 0,512 0,385 N. Verhaeghe et al., 2016 (34-37) Osteoporose 0,748 0,735 0,751 0,738 0,747 0,620 Gezondheidsenquête 2018 (50) Fracturen 0,584 0,571 0,588 0,575 0,583 0,456 Gezondheidsenquête 2018 (50) Fracturen + 0,704 0,691 0,707 0,695 0,703 0,576 N. Verhaeghe et al., 2016 (34-37)
De gezondheidseconomische evaluatie modelleert een opvolging van 20 jaar, daarom is het noodzakelijk om te disconteren. Zo is er rekening gehouden met de toekomstige waarde van de utiliteiten. Jaarlijks wordt er daarom een discontovoet van 1,5% gehanteerd bij het totaal aan QALY’s.
Kosteneffectiviteit
In de evaluatie van nieuwe behandelingen speelt de kosteneffectiviteit een cruciale rol. De berekening van de kosteneffectiviteit van hormonale substitutietherapie gebeurt aan de hand van de incrementele kosteneffectiviteitsratio (IKER). Dit is de verhouding van het verschil in kosten tussen de twee interventies en het verschil in gezondheidseffect tussen de twee interventies. Bij interventie 1 wordt er hormonale substitutietherapie gegeven aan menopauzale vrouwen en bij interventie 2 wordt deze hormonale substitutietherapie niet gegeven. De IKER is afhankelijk van de gezondheidseffecten en de kosten van de behandeling en toont de kost per gewonnen QALY. Het berekenen van deze IKER kan eenvoudig in drie stappen.
26
Eerst wordt het netto kostenverschil berekend. Hiervoor wordt het verschil berekend in kosten die optreden bij het geven van HST en de kosten die optreden indien de therapie niet wordt opgestart.
Om vervolgens het verschil in gezondheidseffecten tussen de twee mogelijke interventies te bepalen, wordt er gebruik gemaakt van het verschil in aantal toegenomen QALY’s tussen de populatie menopauzale vrouwen met HST en de populatie menopauzale vrouwen zonder therapie.
Als laatste stap kan de IKER berekend worden door het verschil in kosten tussen de twee mogelijke alternatieven te delen door het verschil in QALY’s tussen de twee. Door gebruik te maken van deze IKER kan de mate van kosteneffectiviteit van HST bepaald worden.
Sensitiviteitsanalyse
In de sensitiviteitsanalyse wordt de impact van de belangrijkste parameters op de IKER onderzocht om de gevoeligheid van het model aan onzekerheid te toetsen. Er wordt een one-way sensitiviteitsanalyse uitgevoerd, hierbij worden alle parameters afzonderlijk gevarieerd binnen vooraf vastgestelde intervallen. De parameters opgenomen in de one-way sensitiviteitsanalyse zijn de volgende: de kosten van de verschillende aandoeningen (waar nodig opgesplitst in het eerste jaar en daarna), de kosten van behandeling, de transitiekansen (mortaliteitcijfers in en na het eerste jaar van de aandoeningen en incidentiecijfers), de risicoreducties ten gevolge van HST-gebruik en de utiliteiten toegewezen aan de verschillende gezondheidstoestanden. Het bereik van variatie voor de verschillende kosten en transitiekansen omvat een vast interval, gaande van 90 tot 110%. De relatieve risicoreducties en utiliteiten variëren naargelang hun respectievelijke 95%-betrouwbaarheidsintervallen en standaardfouten, verkregen uit de literatuur.
Probabilistische analyse
De verschillende parameters worden gelijktijdig aan variatie onderworpen in een probabilistische sensitiviteitsanalyse. In een dergelijke analyse wordt aan elk van de betrokken inputvariabelen een bepaalde kansverdeling toegekend, waaraan deze onderhevig zijn. Kosten worden verondersteld een gamma-distributie te volgen, relatieve risicoreducties een lognormale distributie en utiliteiten een bèta-distributie. De parameters worden dus niet voorgesteld als waarden variërend binnen een vastgesteld bereik, maar worden in termen van een bepaalde distributie uitgedrukt. Vervolgens wordt het model 10 000 keer uitgevoerd,
27
waarbij telkens voor iedere parameter een toevallig gekozen waarde uit hun respectievelijke distributie gebruikt wordt in de berekening van de IKER. Op die manier wordt de IKER 10 000 maal berekend. Deze resultaten worden gebruikt om de robuustheid van het model te toetsen.
28
4. Resultaten
De kosteneffectiviteit van hormonale substitutietherapie wordt onderzocht door de impact van deze interventie op de gezondheidseffecten en op de verschillende kosten te vergelijken met de situatie waarbij geen hormonale substitutietherapie wordt gegeven.
4.1. Kostenanalyse
Het gebruik van HST bij menopauzale vrouwen heeft een impact op de kosten. In tabel 7 wordt het effect op de totale kost op individueel niveau over 20 jaar opvolging in de interventiegroep vergeleken met deze in de controlegroep. De weergegeven totale kost omvat de som van de directe kost van elke aandoening en in de interventiegroep eveneens de jaarlijkse implementatiekost van de hormoonbehandeling. In de laatste kolom wordt de incrementele kost weergegeven, dit is het verschil tussen de totale kost in de interventiegroep en deze in de controlegroep. In tabel 8 wordt de distributie van de kosten per aandoening weergegeven.
Tabel 7: Effect op de totale kost op individueel niveau over 20 jaar opvolging
Populatie Totale kost zonder HST (€) Totale kost met HST (€) Incrementele kost (€)
Menopauzale vrouwen (50-84 jaar)
5604,77 7658,42 2053,64
Tabel 8: Distributie van de kosten
Kost zonder HST (€) Kost met HST (€) Incrementele kost (€)
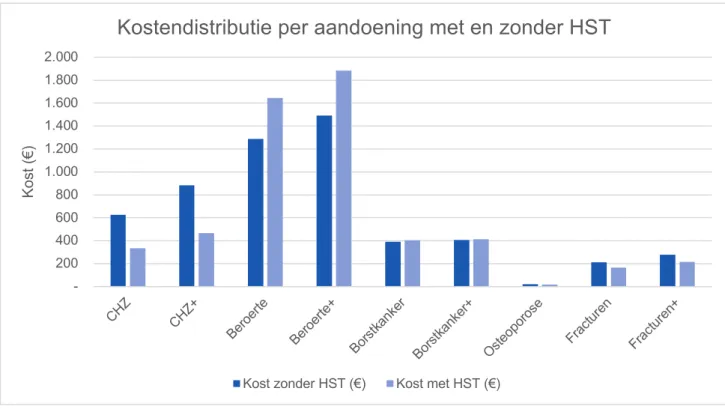
CHZ 627,69 335,03 -292,66 CHZ+ 882,51 467,87 -414,64 Beroerte 1288,96 1644,65 355,68 Beroerte+ 1491,61 1884,05 392,44 Borstkanker 392,59 403,08 10,49 Borstkanker+ 407,28 414,92 7,65 Osteoporose 22,00 17,09 -4,92 Fracturen 213,30 165,72 -47,57 Fracturen+ 278,84 215,64 -63,20 HST 0,00 2110,38 2110,38 TOTAAL 5604,77 7658,42 2 053,64 De kost van CHZ, osteoporose en osteoporotische fracturen is lager bij de interventiegroep. De kost van beroerte en borstkanker is echter hoger. Dit wordt grafisch weergegeven in figuur
29
3. Doordat het geven van de interventie (HST) duurder is dan geen interventie is de incrementele kost positief.
Figuur 3: Kostdistributie per aandoening met en zonder HST
4.2. Analyse gezondheidseffecten
Het gebruik van HST bij menopauzale vrouwen heeft een impact op de levenskwaliteit. In tabel 9 wordt de impact van de interventie over 20 jaar op de levenskwaliteit weergegeven. De gezondheidseffecten worden op individueel niveau weergegeven voor zowel de interventiegroep als de controlegroep. Het incrementeel aantal QALY’s geeft het verschil in gezondheidseffecten tussen de interventiegroep en de controlegroep weer. Dit stelt dus de gezondheidswinst op individueel niveau ten gevolge van hormonale substitutietherapie voor.
Tabel 9: Effect op de gezondheid op individueel niveau na 20 jaar opvolging
Populatie QALY zonder HST QALY met HST Incrementeel aantal QALY’s
Menopauzale vrouwen (50-84 jaar) 9,0486 9,2053 0,1567 200 400 600 800 1.000 1.200 1.400 1.600 1.800 2.000 CHZ CHZ+ Bero erte Bero erte + Borst kanke r Borst kanke r+ Osteo poro se Fract uren Fract uren + Ko st ( €)
Kostendistributie per aandoening met en zonder HST
30 Tabel 10: distributie van de QALY's
QALY’s zonder HST QALY’s met HST Incrementeel aantal QALY’s
Gezond 8,3420 8,6141 0,2720 CHZ 0,0293 0,0158 -0,0135 CHZ+ 0,1143 0,0609 -0,0534 Beroerte 0,0142 0,0182 0,0040 Beroerte+ 0,0624 0,0792 0,0168 Borstkanker 0,0206 0,0213 0,0007 Borstkanker+ 0,1374 0,1405 0,0031 Osteoporose 0,2522 0,1963 -0,0558 Fracturen 0,0157 0,0122 -0,0035 Fracturen+ 0,0605 0,0468 -0,0137
Figuur 4: Vergelijking van het aantal QALY’s met en zonder HST
Tabel 10 stelt de verdeling van de QALY’s over de verschillende aandoeningen weer. Deze cijfers stellen niet alleen voor welke levenskwaliteit bij de verschillende gezondheidstoestanden hoort, maar hangen eveneens af van het aantal vrouwen dat zich in de respectievelijke toestanden bevindt. Zo zal het aantal vrouwen dat zich na 20 jaar opvolging in de toestand CHZ bevindt een stuk kleiner zijn in de interventiegroep dan in de controlegroep. Het aantal QALY’s wordt vervolgens berekend door het aantal vrouwen te vermenigvuldigen
0 1 2 3 4 5 6 7 8 9
QALY's zonder HST QALY's met HST
GEZOND CHZ CHZ+
BEROERTE BEROERTE+ BORSTKANKER
BORSTKANKER+ OSTEOPOROSE FRACTUREN
31
met de utiliteit van de toestand in kwestie. Ondanks de verbeterde levenskwaliteit die HST als resultaat heeft, zal voor verschillende aandoeningen het aantal QALY’s kleiner zijn in de interventiegroep dan in de controlegroep, doordat het aantal vrouwen met deze aandoening afneemt onder hormoonbehandeling. Dit wordt gecompenseerd doordat in de interventiegroep meer vrouwen gezond blijven, aan een hogere levenskwaliteit. Figuur 4 stelt een vergelijking in het aantal QALY’s tussen interventie en controle voor, waarbij ook de onderlinge distributie van het aantal QALY’s tussen de verschillende aandoeningen en de gezonde toestand is weergegeven. Hierbij komt de balk voor de QALY’s van de vrouwen onder hormoonbehandeling hoger uit dan deze voor de controlegroep.
4.3. Kosteneffectiviteitsanalyse
Het resultaat van de IKER is de verhouding van het netto kostenverschil en het verschil in QALY’s. Het verschil is telkens gemaakt tussen de populatie menopauzale vrouwen met HST en de populatie menopauzale vrouwen met de klassieke therapie. Door gebruik te maken van deze IKER is de mate van kosteneffectiviteit van de HST bepaald.
De IKER bedraagt €13 107,75 per QALY.Aangezien in België vaak een drempelwaarde van €35 000 per QALY gehanteerd wordt, betekent dit dat HST kosteneffectief is ten opzichte van de controle, in dit geval de situatie waarin geen behandeling wordt gegeven.
4.4. Sensitiviteitsanalyse
Dankzij de sensitiviteitsanalyse is het mogelijk om het effect ten gevolge van het variëren van de kost van de aandoening, de kost van HST, de utiliteiten, de relatieve risico’s en de transitiekansen op de IKER na te gaan. Deze resultaten zijn visueel voorgesteld in enkele tornado-diagrammen.
Figuur 5 toont het effect van variatie van de verschillende inputparameters op de kosteneffectiviteit. Hieruit blijkt dat de waarde van de IKER bij uitstek zeer sterk gevoelig is aan de parameter ‘relatieve risicoreducties (RRR) coronaire hartziekte (CHZ)’. Dit valt te verklaren door het relatief brede 95% betrouwbaarheidsinterval van deze variabele. Ook variatie in de parameters ‘RRR beroerte’, ‘utiliteit gezond’ (voor zowel de interventie- als de controlegroep) en ‘RRR borstkanker’ heeft een belangrijk effect op de waarde van de IKER. De maximale IKER bedraagt in deze analyse 69 419 euro per QALY, de minimale IKER 7 944 euro per QALY.
32
Figuur 6 en figuur 7 geven het effect van variatie van de verschillende parameters op de teller en de noemer van de IKER (respectievelijk de incrementele kost en het incrementeel aantal QALY’s) weer. Het incrementeel aantal QALY’s is eveneens hoofdzakelijk gevoelig aan variatie van de parameter ‘RRR CHZ’. De incrementele kost is voornamelijk gevoelig aan variatie in de parameters ‘RRR beroerte’ en ‘RRR CHZ’, maar ook de parameter ‘kost HST’ heeft een belangrijke impact.
Figuur 5: Sensitiviteitsanalyse, impact op de kosteneffectiviteit van de interventie
5000 15000 25000 35000 45000 55000 65000
RRR CHZ RRR BEROERTE UTILITEIT GEZOND interventie UTILITEIT GEZOND controle RRR BORSTKANKER KOST HST INCIDENTIE CHZ INDICENTIE BEROERTE RRR OSTEOPOROSE KOST CHZ+ KOST BEROERTE+ KOST BEROERTE KOST CHZ MORTALITEIT BEROERTE OSTEOPOROSE -> FRACTUREN INCIDENTIE OSTEOPOROSE INCIDENTIE BORSTKANKER KOST FRACTUREN+ MORTALITEIT CHZ KOST FRACTUREN MORTALITEIT OSTEOPOROSE KOST BORSTKANKER KOST BORSTKANKER+ KOST OSTEOPOROSE MORTALITEIT FRACTUREN MORTALITEIT BORSTKANKER UTILITEIT FRACTUREN UTILITEIT FRACTUREN+ UTILITEIT BORSTKANKER UTILITEIT OSTEOPOROSE UTILITEIT BEROERTE UTILITEIT CHZ MORTALITEIT GEZOND UTILITEIT BORSTKANKER+ UTILITEIT CHZ+ UTILITEIT BEROERTE+
Kosteneffectiviteit van de interventie (€ per QALY)
33
Figuur 6: Sensitiviteitsanalyse, impact op het incrementeel aantal QALY’s
Figuur 7: Sensitiviteitsanalyse, impact op de incrementele kost
0 0,05 0,1 0,15 0,2 0,25
RRR CHZ UTILITEIT GEZOND interventie UTILITEIT GEZOND controle RRR BEROERTE RRR BORSTKANKER INCIDENTIE CHZ INDICENTIE BEROERTE RRR OSTEOPOROSE UTILITEIT BEROERTE+ MORTALITEIT GEZOND UTILITEIT CHZ+ UTILITEIT BORSTKANKER+ MORTALITEIT CHZ OSTEOPOROSE -> FRACTUREN MORTALITEIT BEROERTE UTILITEIT CHZ UTILITEIT BEROERTE INCIDENTIE OSTEOPOROSE UTILITEIT OSTEOPOROSE UTILITEIT BORSTKANKER INCIDENTIE BORSTKANKER MORTALITEIT OSTEOPOROSE UTILITEIT FRACTUREN+ UTILITEIT FRACTUREN MORTALITEIT FRACTUREN MORTALITEIT BORSTKANKER
Incrementeel aantal QALYs
Afname parameter Toename parameter
€1.600 €1.800 €2.000 €2.200 €2.400 €2.600 RRR BEROERTE RRR CHZ KOST HST RRR BORSTKANKER INDICENTIE BEROERTE INCIDENTIE CHZ KOST CHZ+ KOST BEROERTE+ KOST BEROERTE KOST CHZ MORTALITEIT BEROERTE RRR OSTEOPOROSE MORTALITEIT CHZ INCIDENTIE OSTEOPOROSE KOST FRACTUREN+ OSTEOPOROSE -> FRACTUREN KOST FRACTUREN MORTALITEIT GEZOND INCIDENTIE BORSTKANKER KOST BORSTKANKER MORTALITEIT OSTEOPOROSE KOST BORSTKANKER+ KOST OSTEOPOROSE MORTALITEIT FRACTUREN MORTALITEIT BORSTKANKER Incrementele kost
34
4.5. Probabilistische analyse
Figuur 8 geeft het resultaat van de probabilistische sensitiviteitsanalyse weer in de vorm van een scatterplot. Elk punt geeft de IKER van één berekening van het model weer. In het totaal is dit 10 000 maal uitgevoerd, dus zijn er 10 000 punten weergegeven. De zwarte lijn toont de in België doorgaans gehanteerde grens van kosteneffectiviteit aan, dus €35 000 per QALY. Het merendeel van de punten ligt onder deze grens, wat de robuustheid van het model weerspiegelt.
Figuur 8: Probabilistische analyse
-3.000 -1.000 1.000 3.000 5.000 7.000 9.000 -0,6 -0,4 -0,2 0,0 0,2 0,4 0,6 0,8 1,0 IN CR EM EN TE LE K O ST INCREMENTEEL EFFECT