Hoofdstuk 1
Materialen en stoffen
Paragrafen
Practica
Hoofdstuk 1 – Materialen en stoffen
§1.2 Stoffen §1.1 Materialen §1.3 Scheidings-methoden §1.4 Stoffen verhitten §1.7 De plastic auto komt eraan Proef 4 Extraheren Proef 3
Destilleren Proef 5 Kaarsvet verhitten Proef 6 Platina en magnesium Oplossingen en emulsies Hoe werkt de
§1.1 Materialen
Je leert:
• het verschil te beschrijven tussen natuurlijke en synthetische materialen; • te beschrijven wat duurzaamheid weergeeft;
• te beschrijven wat additieven bij plastics betekenen;
• te beschrijven wat zelfherstellende materialen zijn en hoe ze werken; • te beschrijven wat een composiet is.
Kunststoffen zijn materialen die niet meer zijn weg te denken uit onze maatschappij. Maar ook natuurlijke materialen worden nog steeds gebruikt.
§1.1 Materialen
Natuurlijke materialen
§1.1 Materialen
Van oude naar nieuwe materialen
§1.1 Materialen
Van oude naar nieuwe materialen
§1.1 Materialen
Van oude naar nieuwe materialen
§1.1 Materialen
Synthetische materialen
§1.1 Materialen
Additieven
Kleurstoffen, zoals indigo.
Weekmakers, om kunststoffen zachter, flexibeler en minder breekbaar te maken.
§1.1 Materialen
§1.1 Materialen
§1.1 Materialen
§1.1 Materialen
Je kunt nu:
• het verschil beschrijven tussen natuurlijke en synthetische materialen; • beschrijven wat duurzaamheid weergeeft;
• beschrijven wat additieven bij plastics betekenen;
• beschrijven wat zelfherstellende materialen zijn en hoe ze werken; • beschrijven wat een composiet is.
§1.2 Stoffen
Je leert:
• op micro- en macroniveau te beschrijven wat zuivere stoffen en wat mengsels zijn; • het verschil uit te leggen tussen homogene en heterogene mengsels;
• te beschrijven wat een suspensie en wat een emulsie is;
• het verschil tussen het temperatuurverloop bij smelten en koken van een zuivere stof en een mengsel in woorden en in een grafiek weer te geven;
• hoe je het massapercentage en het volumepercentage kunt berekenen;
• te beschrijven wat de TGG-waarde inhoudt en te rekenen met de TGG-waarde.
Stoffen vormen de basis voor het maken van
materialen. Aan stofeigenschappen zoals geur, kleur en oplosbaarheid kun je een stof herkennen. Materialen zijn meestal mengsels. Zie je de eigenschappen van de stoffen terug in de mengsels?
§1.2 Stoffen
Van materiaaleigenschappen naar stofeigenschappen
§1.2 Stoffen
Mengsels en zuivere stoffen
Mengsel: ‘Combinatie van twee of meer stoffen (bestanddelen).’
Zuivere stof: ‘Stof die uit maar één bestanddeel bestaat.’
§1.2 Stoffen
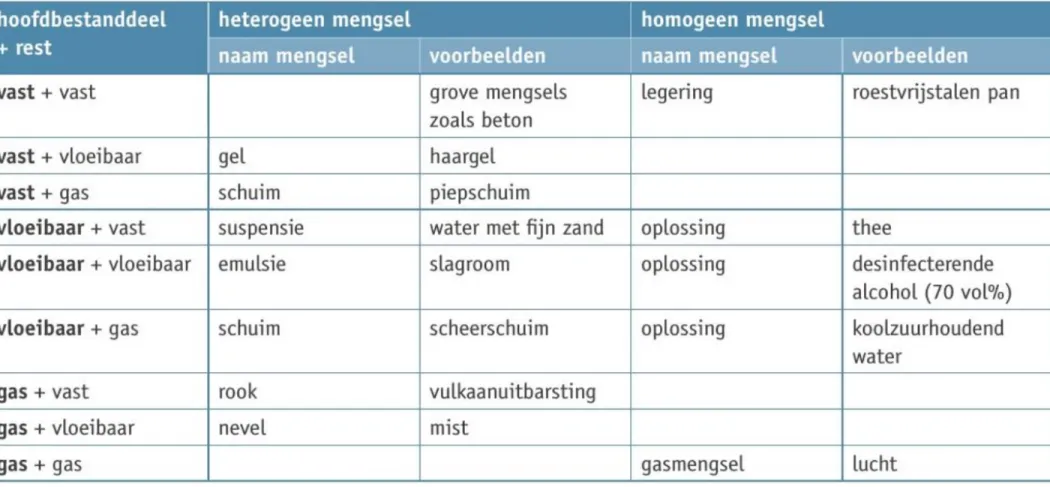
Homogene mengsels
‘Mengsel dat zich in één fase bevindt: vloeibaar, vast of gasvormig. De verschillende bestanddelen zijn niet meer onderscheidbaar.’
§1.2 Stoffen
Heterogene mengsels
‘Mengsel waarvan de verschillende bestanddelen nog van elkaar te onderscheiden zijn.’
§1.2 Stoffen
§1.2 Stoffen
Zuivere stof of mengsel?
Het temperatuurverloop tijdens het verwarmen van een zuivere stof (links) en van een mengsel (rechts).
§1.2 Stoffen
De samenstelling van mengsels
§1.2 Stoffen
De samenstelling van mengsels
§1.2 Stoffen
De samenstelling van mengsels
concentratie = volumemassa c = m
V
c = concentratie (g/L) m = massa (g)
§1.2 Stoffen
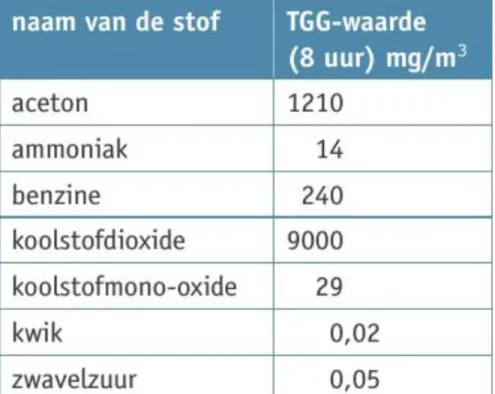
TGG-waarde
‘Grenswaarde die aangeeft hoeveel er van een stof in de lucht mag voorkomen.’
§1.2 Stoffen
§1.2 Stoffen
Je kunt nu:
• op micro- en macroniveau beschrijven wat zuivere stoffen en wat mengsels zijn;
• het verschil uitleggen tussen homogene en heterogene mengsels; • beschrijven wat een suspensie en wat een emulsie is;
• het verschil tussen het temperatuurverloop bij smelten en koken van een zuivere stof en een mengsel in woorden en in een grafiek weergeven;
• het massapercentage en het volumepercentage berekenen;
§1.3 Scheidingsmethoden
Je leert:
• te beschrijven voor welk soort mengsel de volgende scheidingsmethoden gebruikt kunnen worden en waarop het principe van scheiding berust:
o filtreren o bezinken / centrifugeren o destilleren / indampen o extraheren o adsorberen o chromatograferen
Zoals het woord schei-kunde al aangeeft, is het scheiden van mengsels in zuivere stoffen een belangrijk onderdeel in de scheikunde. Er zijn verschillende soorten mengsels en ook
verschillende manieren om mengsels te scheiden.
§1.3 Scheidingsmethoden
Scheiden van een mengsel
Berust op verschil in stofeigenschap(pen).
kookpunt deeltjesgrootte
dichtheid
oplosbaarheid
§1.3 Scheidingsmethoden
§1.3 Scheidingsmethoden
§1.3 Scheidingsmethoden
Centrifugeren
§1.3 Scheidingsmethoden
§1.3 Scheidingsmethoden
§1.3 Scheidingsmethoden
Extraheren
§1.3 Scheidingsmethoden
Adsorberen
LET OP!
Er is een verschil tussen adsorptie en absorptie. Bij adsorptie hechten de moleculen zich aan de buitenkant van het adsorptiemateriaal. Bij absorptie dringen de moleculen het materiaal binnen. Een spons absorbeert dus water terwijl Norit
§1.3 Scheidingsmethoden
§1.3 Scheidingsmethoden
Een scheidingsmethode kiezen
§1.3 Scheidingsmethoden
Je kunt nu:
• beschrijven voor welk soort mengsel de volgende scheidingsmethoden gebruikt kunnen worden en waarop het principe van scheiding berust:
o filtreren o bezinken / centrifugeren o destilleren / indampen o extraheren o adsorberen o chromatograferen
§1.4 Stoffen verhitten
Je leert:
• te beschrijven dat bij een chemische reactie beginstoffen verdwijnen en omgezet worden in reactieproducten;
• uit te leggen dat een fase-overgang geen chemische reactie is; • te beschrijven wanneer je spreekt van een verbrandingsreactie; • te beschrijven wanneer je spreekt van en ontledingsreactie.
Je hebt zelf vast wel eens water
gekookt in een waterkoker, sterretjes of vuurwerk aangestoken, of een eitje gebakken. Hierbij worden stoffen verhit. Naast een temperatuurstijging vinden bij verhitting nog andere veranderingen plaats.
§1.4 Stoffen verhitten
§1.4 Stoffen verhitten
Chemische reacties
§1.4 Stoffen verhitten
Verbranden
§1.4 Stoffen verhitten
Ontleden
§1.4 Stoffen verhitten
Je kunt nu:
• beschrijven dat bij een chemische reactie beginstoffen verdwijnen en omgezet worden in reactieproducten;
• uitleggen dat een faseovergang geen chemische reactie is; • beschrijven wanneer je spreekt van een verbrandingsreactie; • beschrijven wanneer je spreekt van een ontledingsreactie.
§1.7 De plastic auto komt eraan
Auto’s moeten nog energiezuiniger worden en dat kan door al dat zware staal te vervangen door het veel lichtere kunststof. Er is alleen nog geen geschikt
materiaal. Het Twentse onderzoeksinstituut TPRC werkt aan materialen en technologieën die de autowereld mogelijk op zijn kop gaan zetten.