ANASTOMOTISCHE STRICTUUR NA DE
CORRECTIE VAN SLOKDARMATRESIE
EEN SYSTEMATISCH LITERATUUR
ONDERZOEK
Sarah Delaet
Stamnummer: 01508181Promotor: Prof. Dr. Stephanie Van Biervliet
Promotor: Dr. Lucas Matthyssens
Masterproef voorgelegd in het kader tot het behalen van de graad Master of Medicine in de Geneeskunde Academiejaar: 2018 – 2020
Deze pagina is niet beschikbaar omdat ze persoonsgegevens bevat.
Universiteitsbibliotheek Gent, 2021.
This page is not available because it contains personal information.
Ghent University, Library, 2021.
Voorwoord
Met het schrijven van deze masterproef eindig ik het theoretische deel van mijn opleiding Geneeskunde aan de Universiteit Gent. Dit vroeg niet alleen vele inspanningen, maar ook motivatie om de opdracht tot een goed eind te brengen. Ik heb voor heel wat uitdagingen komen te staan, maar heb er eveneens uit geleerd. Niet enkel over het onderwerp slokdarmatresie, maar ook over de mogelijkheden die endnote biedt en over wetenschappelijk schrijven.
Dat deze masterproef een werk van lange adem is geweest, staat buiten twijfel. Dit literatuuronderzoek zou niet tot stand gekomen zijn zonder hulp.
Allereerst wil ik mijn promotoren, Prof Dr. Stephanie Van Biervliet en Dr. Lucas Matthyssens bedanken. Zij hebben mij begeleid doorheen het hele traject. Voor feedback en vragen kon ik steeds bij hun terecht. Ondanks hun drukke agenda, namen ze de tijd om mij te begeleiden. Ook wil ik vrienden en familie bedanken, die mij onvoorwaardelijke gesteund en aangemoedigd hebben wanneer de motivatie even ver te zoeken was.
Ik wens U een interessante leeservaring toe.
Delaet Sarah
Inhoud
Abstract ... 1
Afkortingen lijst ... 2
Inleiding ... 3
Deel 1: Oesophageale atresie ... 3
Deel 2: Anastomotische strictuur van de slokdarm na OA ... 7
Vraagstelling ... 8
Methodologie ... 9
Resultaten ... 11
1. Patiënten populatie literatuur onderzoek en strictuur prevalentie ... 11
2. Strictuur in functie van risicofactoren ontstaan ... 11
2.1. Type OA... 12
2.2. Operatieve factoren ... 13
2.3. Peri- en postoperatieve factoren ... 14
3. Strictuur behandeling ... 16
Discussie ... 18
Referentielijst ... 23
Abstract
DOEL: Anastomotische strictuur (AS) is een belangrijke comorbiditeit na het herstel van congenitale slokdarmatresie (oesophageale atresie, OA). In deze masterproef wordt een systematisch literatuuroverzicht gemaakt van de strictuur frequentie in de populatie en de factoren die een rol spelen in de ontwikkeling van deze vernauwing.
METHODE: Systematische review van de wetenschappelijke publicaties waarin AS is beschreven bij patiënten die na de geboorte een correctie ondergingen van OA. Artikels werden geïncludeerd uit de zoekmachines Pubmed, Embase en Web of Science. De literatuur zoektocht werd beperkt tot studies gepubliceerd binnen 2000 - 2019. Waar mogelijk werden de resultaten geanalyseerd aan de hand van univariatie analyse (Chi-square test).
RESULTATEN: De studie includeerde 73 publicaties met in het totaal 4999 OA patiënten (Gross type A: 377, type B: 57, type C: 4361, type D: 75, type E: 87). AS kwam gemiddeld in 37% van de OA correcties voor, variërend per Gross type. De verscheidenheid van definities voor strictuur in de literatuur is problematisch. Standaardbehandeling van AS bestaat uit het dilateren met ballon en/of bougie. Op univariate analyse waren een lange afstand tussen beide oesophagusstompen (p < 0,001), tractie op de anastomose (p < 0,001), end-to-end anastomosetechniek (p < 0,001), lekkage (p < 0,001) en de aanwezigheid van gastro-oesophagale reflux (p < 0,001) significant geassocieerd met verhoogd risico op AS. Congenitale hartziekten (p = 0,082), het plaatsen van transanastomotische nasogastrische tube (p = 0,370) en eosinofiele oesophagitis (p = 0,384) waren niet significant geassocieerd met een hoger risico op AS. Eveneens bleken operatieve technieken zoals thoracotomie versus thoracoscopie (p = 0,327) een gelijkaardig risico te hebben op AS, hetzelfde gold voor primair versus uitgesteld herstel (p = 0,614). Over het profylactisch gebruik van zuurremming was er veel discussie, maar het effect bleek in dit literatuuronderzoek eerder nihil.
CONCLUSIE: Aan de hand van de bevindingen uit dit literatuur onderzoek is men in staat een beter inzicht te krijgen in de risicofactoren op het ontwikkelen van AS, namelijk lange afstand tussen beide oesophagusstompen, tractie op de anastomose, end-to-end anastomose, lekkage en gastro-oesophageale reflux. Dit is nuttig om enerzijds de ouders te informeren over het potentieel risico op AS en anderzijds om huidige aanpak aan te passen en het risico in de toekomst te beperken. Verder onderzoek kan gebeuren, maar vereist eenduidige definiëring van AS.
Afkortingen lijst
OA Oesophageale atresie of slokdarm atresie TOF Tracheo-oesophageale fistel
AS Anastomotische strictuur
LGOA “Long gap” oesophageale atresia E-E End-to-end anastomose
E-S End-to-side anastomose GOR Gastro-oesophageale reflux EoE Eosinofiele oesophagitis
TAT Transanastomotische nasogastrische tube of sonde CHD Congenital heart disease of congenitale hartaandoeningen PARM Profylactische anti-reflux medicatie of therapie
Inleiding
Deel 1: Oesophageale atresie
Slokdarmatresie (oesophageale atresie, OA) is een aangeboren aandoening die wordt gekenmerkt door afwezigheid van een continue verbinding van de slokdarm tot de maag. Het is één van de meest voorkomende gastro-intestinale malformaties met een incidentie van 1:2500 tot 1:4500 levendgeborenen (1-3). OA komt in ongeveer 50% van de patiënten voor in combinatie met andere congenitale malformaties, waaronder vertebrale, anorectale, cardiale, renale, urinaire en lidmaat afwijkingen (2). Vroeg in de embryonale ontwikkeling ontstaat de respiratoire tractus uit de primitieve voordarm als een divertikel. Dit divertikel gaat distaal over in splanchnisch mesoderm en vormt er de twee hoofdbronchi. Tegelijkertijd ontstaat een tracheo-oesophageale groeve, die de bovenste respiratoire tractus (trachea) en digestieve tractus (oesophagus) van elkaar gaat splitsen. Onvolledige splitsing vormt de basis van een tracheo-oesophageale fistel (TOF) (4). De exacte etiologie van OA blijft tot op heden onbekend, al zijn er argumenten voor genetische factoren en omgevingseffecten (2).
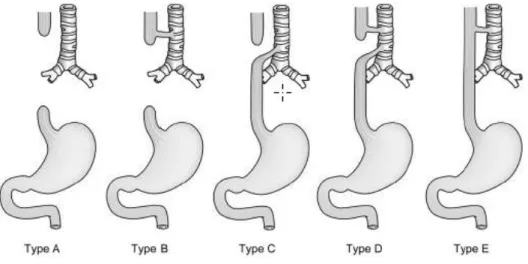
De meest gebruikte classificatie om OA anatomisch in te delen is de classificatie volgens Gross, zie Figuur 1. Gross type C (OA met distale TOF) is de meest voorkomende variant, gevonden in 85% van de gevallen. Gross types A (zonder TOF, 7%), B (met proximale TOF,1%) en D (met zowel proximale als distale TOF, 3%) zijn zeldzamer. Gross type E (geïsoleerd TOF zonder slokdarmafsluiting, 4%) valt buiten het onderwerp van deze thesis en is ook relatief weinig voorkomend (4, 5).
Bij kinderen zonder distale TOF (Gross types A en B) is er meestal sprake van een grotere onderbreking tussen de twee slokdarmuiteinden, hier wordt gesproken van een ‘long gap’ OA (LGOA) en dit heeft therapeutische implicaties (5). Er is veel discussie omtrent de exacte definitie van LGOA. Deze wordt typisch uitgedrukt als een ‘gap’ lengte van meer dan twee vertebrale wervellichamen door kinderchirurgen (6). De INoEA werkgroep publiceerde een consensus rapport waarin gesuggereerd wordt dat een OA met afwezigheid van intra-abdominale lucht gedefinieerd kan worden als een LGOA (7).
De diagnose van OA wordt gesteld in de vroege postnatale periode, soms kan men een prenataal vermoeden hebben. De aanwezigheid van polyhydramnios en een kleine maag op prenatale echografie hebben een voorspellende waarde voor OA van 55%. De aanwezigheid van andere geassocieerde malformaties kan dit vermoeden versterken. Postnataal zullen klinische symptomen zoals speekselvloed, aspiratie en cyanose bij voeding OA doen vermoeden (4). De diagnose wordt gesteld door het plaatsen van een nasogastrische sonde, welke niet verder kan ingebracht worden dan het proximale uiteinde van de oesophagus. Omdat valse geruststelling kan optreden bij het opkrullen van de sonde in de pouch of volgen van een fistel traject, dient de positie van de sonde radiografisch bevestigd te worden (6). Aanwezigheid van lucht in de maag is indicatief voor een distale TOF, terwijl de afwezigheid van lucht meestal wijst op de afwezigheid van een distale TOF, een grotere kans op LGOA en een complexere chirurgische behandeling (4, 6). Bij onduidelijkheid over de diagnose kan een contraststudie uitgevoerd worden met het risico op aspiratie van dit contrast (4).
De primaire behandeling voor OA is chirurgisch. De eerste succesvolle primaire anastomose bij een kind met OA werd uitgevoerd in 1941 door Cameron Haight (8). Door de vooruitgang in de chirurgische technieken, anesthesie, neonatale intensieve zorgen en nutritionele support verschoof men de focus van mortaliteit naar morbiditeit en problemen met levenskwaliteit (1, 9). OA veroorzaakt morbiditeit op zowel kinderleeftijd als bij adolescenten. De problemen beschreven na chirurgie voor OA zijn voornamelijk anastomotische strictuur (AS, in 20-50% van de patiënten), gastro-oesophageale reflux (GOR, 17-75%), oesophagitis (25-83%), gastrische metaplasie en Barret oesophagus (4-11%), dysfagie (48-85%), oesophageale dysmobiliteit (bij quasi alle patiënten aanwezig), recurrente fistel vorming (8-10%), lekkage (3-20%) en het ontstaan van carcinomen (enkele zeldzame gevallen) (3, 6, 9-11). De huidige overleving voor kinderen geboren met OA bedraagt meer dan 95%, de prognose zal in sterke mate bepaald worden door het al dan
Meestal is de heelkundige behandeling van OA geen absolute urgentie en kan er preoperatief voldoende tijd genomen worden voor opsporen van geassocieerde malformaties en stabilisatie van de baby. In deze periode wordt de proximale stomp continu leeggezogen met een replogle sonde om aspiratie te beperken. Enkel bij een fors gedilateerde maag met risico op perforatie en bij kinderen met ‘Respiratory Distress Syndrome (RDS)’ en achteruitgang van de respiratoire status, zal men sneller ingrijpen. Pasgeborenen die de eerste 24 uur na geboorte chirurgie ondergaan hebben immers een hoger complicatie risico (6).
De klassieke open benadering voor de heelkundige behandeling van OA, met of zonder distale TOF, is al jaren de standaard. Via een rechter posterolaterale thoracotomie en extrapleurale toegang wordt de TOF afgebonden om aspiratie van maaginhoud te voorkomen en de ventilatie dynamiek van de trachea te herstellen. Vervolgens wordt ook de continuïteit van de oesophagus hersteld door de twee slokdarmstompen aan elkaar vast te hechten (6). Recente chirurgische vooruitgang zorgde ervoor dat we de morbiditeit geassocieerd met open chirurgie kunnen verminderen door thoracoscopische chirurgie. Deze minimaal invasieve techniek heeft exact dezelfde operatieve doelstellingen, maar heeft als voordeel dat de pijn, littekenvorming en lange termijn musculoskeletale deformaties zoals sclerose verminderen. Via 3 mm en 5 mm poorten (trocars) wordt intern gewerkt in de thorax, waarbij een pneumothorax wordt aangelegd voor een betere visualisatie. Postoperatief kan een thoraxdrain worden achtergelaten via één van de poortincisies (6).
‘Long gap’ OA (LGOA) blijft een chirurgische uitdaging omdat beide slokdarmstompen niet primair aan elkaar gezet kunnen worden. Prioriteit blijft het behoud van de oesophagus. Bij de uitgestelde primaire anastomose probeert men de stompen te laten groeien waarvoor verschillende technieken beschreven zijn. In de tussenperiode zal een gastrostomie nodig zijn om het kind te voeden. Afhankelijk van de techniek zal eventueel een replogle sonde voor aspiratie van de proximale stomp nodig blijven (6, 12). Thoracoscopische tractietechnieken kunnen tegenwoordig direct na de geboorte uitgevoerd worden waarbij het kind onder parenterale voeding blijft, zonder nood aan gastrostomie (12). Bij de Kimura techniek wordt de proximale oesophagusstomp onder de vorm van een cutaan stoma naar buiten gebracht en progressief door middel van herhaalde ingrepen verder naar beneden verplaatst. De Foker procedure is ook een extrathoracale elongatie techniek, waarbij tractiesuturen worden aangelegd aan de proximale en distale oesophagus uiteinden. Door progressief toenemende tractie zullen deze elongatie stimuleren. Er bestaat nog discussie of de elongatie bekomen door tractie het gevolg is van oprekking of echte groei. Een uitgestelde primaire anastomose wordt dan uitgevoerd op het moment dat de twee uiteinden bij elkaar gebracht kunnen worden (6, 13). Wanneer dit echter faalt, moet overgegaan worden tot vervanging van de
oesophagus. Hiervoor worden verschillende structuren gebruikt die allen hun complicaties hebben. Men kan gebruik maken van een getubuleerde maag, een buisvormige reconstructie van de oesophagus met weefsel van de grote curvatuur van de maag. Dit geeft een verkleinde maar nog steeds functionele maag. Een tweede optie is een gastrische transpositie of het optrekken van de maag en vervolgens hechten van de maag aan het proximale slokdarmeinde. Als laatste optie kan men een interpositie van dundarm of colon gebruiken om de oesophagus te reconstrueren. Hierbij wordt een segment geïsoleerd en geïnterponeerd tussen proximale en distale oesophagus of maag. Er is in de literatuur geen duidelijke evidence-based voorkeur voor afkomst van het segment dat hiervoor gebruikt wordt, de keuze wordt gemaakt door de chirurg en zijn expertise met de technieken (6).
Complicaties na heelkundige behandeling van OA zijn frequent en de oorsprong van belangrijke morbiditeit. De belangrijkste vroege postoperatieve complicaties zijn anastomotische lekkage, strictuur en recurrente tracheo-oesophageale fistel (TOF) (6).
Anastomotische lekkage komt voor in 3-20% van de patiënten met als grootste risicofactor anastomotische tensie. Grote lekken treden binnen de 48 u postoperatief op en presenteren zich met acute deterioratie, tensiepneumothorax en sepsis. Urgente thoraxdrainage is vereist, maar operatieve herinterventie is slechts nodig bij (quasi) volledige disruptie van de oesophagus of onmogelijkheid om de pneumothorax te controleren. Kleinere lekken worden typisch gedetecteerd op routine contraststudie in asymptomatische kinderen en komen frequenter voor. Ze helen in principe spontaan (6).
Anastomotische strictuur (zie verder) komt waarschijnlijk voor bij gemiddeld één derde van de patiënten met OA. Dilataties zijn de effectieve behandeling, met laag risico op perforatie (<2% per episode) (6).
Recurrente TOF formatie is zeldzaam (8-10% van de patiënten) maar leidt tot recurrente luchtweginfecties en levensbedreigende events. Correctie kan open (chirurgisch) of endoscopisch, (met laser ablatie en occlusie met fibrine of cyanoacrylaat lijm) (6, 10).
Stemband paralyse is een zeldzame complicatie in 3-4% van de gevallen en ontstaat door intraoperatieve beschadiging van de N. laryngeus recurrens. Unilaterale paralyse geneest spontaan, bilaterale vereist chirurgische behandeling via tracheostomie.
Laattijdig kan ook gastro-oesophageale reflux (GOR) en tracheomalacie optreden. Deze complicaties zijn een belangrijke oorzaak voor morbiditeit (6).
Deel 2: Anastomotische strictuur van de slokdarm na OA
AS is een vernauwing van de oesophagus ter hoogte van de anastomose na de correctie voor OA (1). Deze vernauwing resulteert in gastrointestinale symptomen als dysfagie en regurgitatie. Ook respiratoire symptomen als gevolg van aspiratie leidend tot zuurstofdesaturatie, hoesten en herhaalde respiratoire infecties (1, 13). Op het moment van symptomatische presentatie is er vaak al sprake van een hooggradige strictuur (11). Al correleren de symptomen niet steeds met de ernst van de vernauwing op een contrast radiografie (1). Het blijft een belangrijke comorbiditeit van OA herstel ondanks de verbetering van de chirurgische materialen en technieken (9, 11). Hoewel de hoger vermelde klachten kunnen wijzen op een strictuur, is er een belangrijke overlap met andere condities zoals oesophageale dysmotiliteit, recurrente TOF, GOR, tracheomalacie, laryngeale kloven en stemband dysfunctie (1, 13). Om deze problemen tijdig te detecteren is een multidisciplinaire opvolging van deze patiënten nodig. Bij klinisch vermoeden van een AS kan de aanwezigheid bevestigd worden aan de hand van een oesophagogram en/of endoscopie. Het voordeel van de radiografie is dat het toelaat zowel oesophageale morfologie als geassocieerde afwijkingen en pulmonaire problemen te objectiveren. De endoscopie laat toe om diagnose en behandeling te combineren. De ernst van de stenose kan daarintegen beter ingeschat worden met statische radiologische beelden, dit is moeilijk via endoscopie (13).
De hoeksteenbehandeling voor AS secundair aan OA is dilatatie. Het is een bevestigde effectieve behandeling met doel om de symptomen te verlichten, orale voeding mogelijk te maken en risico op pulmonaire aspiratie te verkleinen (13). Dit kan via bougie of ballon, endoscopisch of fluoroscopisch, uitgevoerd worden, maar gebeurt best onder narcose gezien het een pijnlijke procedure is (1, 13). Bij de Savary-Gilliard Bougie wordt een geleidingsdraad geplaatst van slokdarm tot in de maag waarover bougies met wisselende maximale diameter geschoven worden tot de gewenste diameter bekomen wordt (1). De Maloney Bougie wordt wegens zijn hoger perforatie risico als gevolg van de blinde insertie steeds minder gebruikt (1). Bij de ballon dilatatie wordt een ballon met behulp van röntgenbeeldvorming of endoscopie ter hoogte van de strictuur geplaatst en vervolgens geleidelijk opgeblazen onder controle van een manometer. Er zijn verschillen in maximale inflatiedruk en inflatieduur beschreven (1). Anno 2019 is er onduidelijkheid in de literatuur over de superioriteit van een dilatatietechniek, dit gaan we in deze literatuurstudie verder trachten te onderzoeken.
Om het risico op perforatie te minimaliseren, zal men wachten met de eerste dilatatie tot minstens drie weken na de anastomose (1). Er kan bij de dilataties een onderscheid worden gemaakt in twee
groepen, enerzijds selectieve en anderzijds routine dilatatie. Selectieve dilatatie is dilatatie van een klinisch significante (symptomatische) strictuur. Routine dilatatie is dilatatie van een asymptomatische vernauwingen vastgesteld bij postoperatieve controle met contrast oesophagografie of endoscopie (13). In de literatuur is onduidelijk welke indicatie superieur is, ook dit zullen we met deze literatuurstudie trachten te onderzoeken. De respons op dilatatie is variabel. Strictuur resolutie treedt op na een gemiddelde van 3,2 dilataties per patiënt (9).
Volgens de ESPGHAN-ESGE richtlijnen, spreekt men van een refractaire strictuur wanneer een anastomotische vernauwing niet tot normale leeftijds-verwachte diameter gedilateerd kan worden na een maximum van vijf dilataties binnen een interval van vier weken. Bij de onmogelijkheid een aanvaardbare diameter te behouden voor vier weken eens de leeftijds-verwachte diameter bereikt werd, spreekt men van een recurrente strictuur. Zowel refractair als recurrente stricturen vormen een uitdaging in de opvolging van deze patiënten (14). Bij de behandeling van deze moeilijkere stricturen wordt gepoogd de littekenvorming te beperken door medicatie zoals steroïden of mitomycine C ter hoogte van de stenose aan te brengen. Verder kan er geprobeerd worden de slokdarm open te houden aan de hand van een stent die men over de stenotische zone heen plaatst (1). Er bestaan momenteel biodegradeerbare stents die enkele maanden ter plaatse kunnen blijven maar de ervaring is beperkt. Chirurgische resectie of oesophageale vervanging (met jejunum, colon of gastrische interpositie) wordt enkel in overweging genomen bij refractaire strictuur na falen van alle conservatieve therapieën (1).
Vraagstelling
Het doel van dit systematisch literatuuroverzicht is een inzicht te krijgen in hoe frequent AS voorkomt in de populatie OA en welke factoren geassocieerd zijn met het optreden van AS. Dit laatste met oog op eventueel verbetering van de behandeling om het optreden van deze complicatie in de toekomst te beperken.
Methodologie
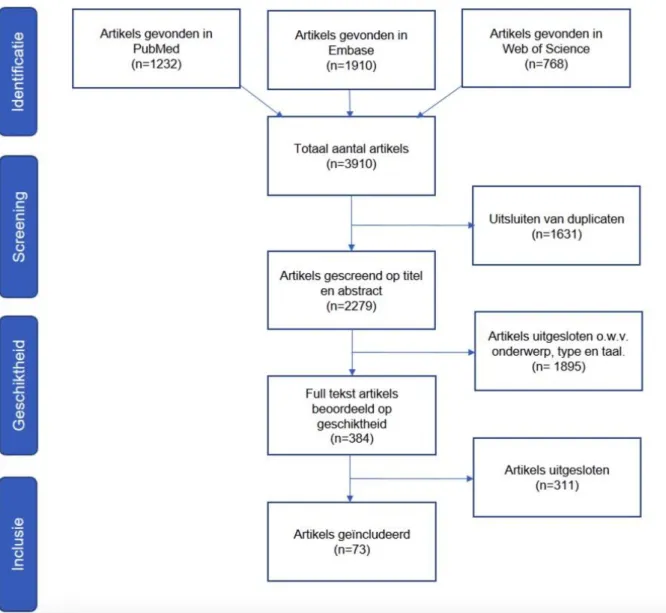
Voor deze systematische review werd er gewerkt volgens het PRISMA principe. De zoekopdracht naar artikels werd uitgevoerd in databases Pubmed, Embase en Web Of Science met volgende zoekterm: ‘esophageal atresia AND (strict* OR dilat* OR stenosis)’. Dit gaf 3910 resultaten, na uithalen van de duplicaties (1631 publicaties) resteerden er nog 2279 unieke artikels. Studies relevant voor deze review werden geselecteerd met inclusie criteria: oorspronkelijke papers met meer dan 10 patiënten en geschreven in Nederlands, Engels, Duits of Frans. Exclusie criteria waren: reviews, editorials, opiniestukken, Gross type E OA, strictuur na interpositie, strictuur secundair aan andere fenomenen dan operatie voor OA of bij dieren. Het proces van titel en abstract screening excludeerde 1895 artikels, de resterende 384 artikels ondergingen full-tekst screening. Omwille van de sterke evolutie in de opvang en behandeling van neonaten met OA, werden studies gepubliceerd voor het jaar 2000 niet geïncludeerd. Indien full tekst niet online beschikbaar was via Ugent of andere bronnen, werden artikels betalend aangevraagd via de interbibliothecaire dienst om een zo volledig mogelijk beeld te krijgen van de reeds gepubliceerde literatuur. Voor deze review werden finaal 73 artikels geïncludeerd. Studieresultaten werden geëxtraheerd in een elektronische spreadsheet (Excel). Data werd waar mogelijk geanalyseerd aan de hand van de Chi-square test (SPSS). Een p-waarde < 0,05 werd gezien als statistisch significant.
Resultaten
1. Patiënten populatie literatuur onderzoek en strictuur prevalentie
De 73 geïncludeerde studies rapporteerden de resultaten van 4999 patiënten met OA. De verdeling over de verschillende types, uit alle studies samen, staat vermeld in Tabel 1. In bijlage een overzicht van de geïncludeerde artikels met studiekenmerken (Bijlage 1).
Tabel 1: Verdeling types OA in literatuur.
Type OA Aantal (totaal 4999)
Type A 377 7,5% Type B 57 1,2% Type C 4361 87,2% Type D 75 1,5% Type E 87 1,7% Type F 1 <0,01% onbekend 41 0,8%
AS kwam in gemiddeld 37% van de gevallen na OA correctie voor. In de literatuur was er een sterk uiteenlopende definitie van strictuur en frequent ontbrak deze zelfs volledig. In 22% (16/73) van de geïncludeerde studies werd strictuur gedefinieerd als er symptomen waren. In de 57 andere publicaties (78%) was AS onduidelijk gedefinieerd of waren het asymptomatische vernauwingen te zien op routine postoperatieve controles. Hoe de diagnose van AS gesteld werd, was slechts in 28 studies (38,4%) vermeld. Hiervan gebruikten 24 studies een contrast RX (slikfoto) en 13 studies een endoscopie, waaronder 9 studies die beide technieken hanteerden. In de andere 45 studies (61,6%) werd hierover niets vermeld.
2. Strictuur in functie van risicofactoren ontstaan
Bij de factoren die beschreven werden als een mogelijke beïnvloedende factor op het ontstaan van AS, zijn er een aantal die niet beïnvloedbaar zijn, zoals type OA, de afstand tussen de twee slokdarmstompen, de aanwezigheid van congenitale hartaandoeningen (congenital heart disease, CHD). Er werd ook gekeken naar de operatieve technieken en postoperatieve factoren, omdat hier
een verandering in beleid eventueel de ontwikkeling van AS zou kunnen beïnvloeden. Waar mogelijk werd een univariate analyse gedaan om na te gaan of de risicofactor aanleiding gaf tot een verandering in risico op het ontwikkelen van een AS. In bijlage een overzicht van alle statistische resultaten (Bijlage 2).
2.1.
Type OA
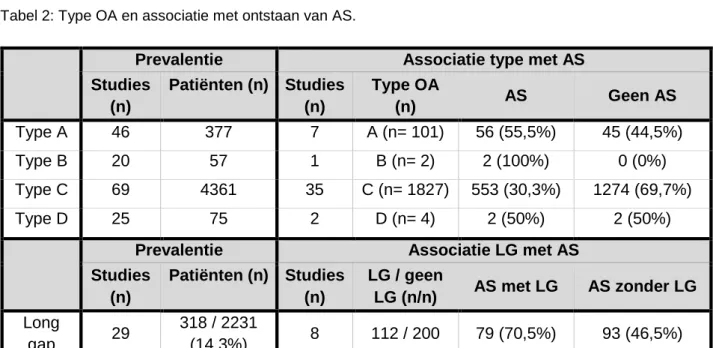
De frequentie van het ontwikkelen van AS varieerde sterk in functie van het type OA. De hoeveelheid data waarop de frequentie gebaseerd is, varieerde eveneens zeer sterk, zie Tabel 2. Een andere belangrijke factor bij het ontstaan van AS was de afstand van de gap bij de OA tijdens de operatie. Opnieuw vormde definitie hier een probleem. Sommige studies definieerden de afstand van de gap aan de hand van het aantal centimeters tussen de 2 slokdarmstompen (bijvoorbeeld: “> 2 cm”), anderen baseerden zich op het aantal wervellichamen (bijvoorbeeld: “> 2 wervels”). De aanwezigheid van een “long gap” (LGOA) ging gepaard met een sterk significante toename in AS (p < 0,001).
Tabel 2: Type OA en associatie met ontstaan van AS.
Prevalentie Associatie type met AS
Studies (n) Patiënten (n) Studies (n) Type OA (n) AS Geen AS Type A 46 377 7 A (n= 101) 56 (55,5%) 45 (44,5%) Type B 20 57 1 B (n= 2) 2 (100%) 0 (0%) Type C 69 4361 35 C (n= 1827) 553 (30,3%) 1274 (69,7%) Type D 25 75 2 D (n= 4) 2 (50%) 2 (50%)
Prevalentie Associatie LG met AS
Studies (n) Patiënten (n) Studies (n) LG / geen LG (n/n) AS met LG AS zonder LG Long gap 29 318 / 2231 (14,3%) 8 112 / 200 79 (70,5%) 93 (46,5%)
2.2.
Operatieve factoren
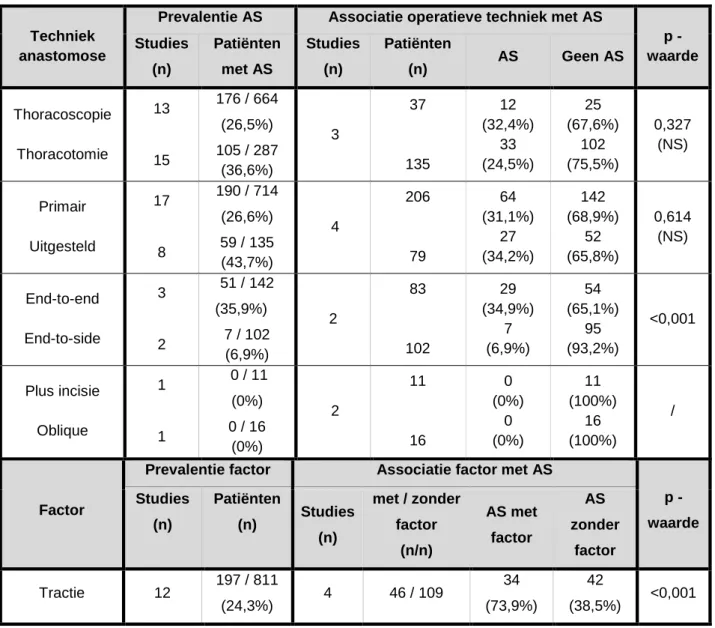
Operatieve technieken werden in de literatuur frequent beschreven, zie Tabel 3.
Technisch kan de benadering op twee verschillende manieren gebeuren: via thoracotomie of thoracoscopie. Van de 664 patiënten die een thoracotomie ondergingen, ontwikkelden 176 patiënten (26,5%) een strictuur. De thoracoscopische methode werd beschreven bij 287 patiënten waarvan er 105 patiënten (36,6%) een strictuur kregen. Slechtst drie studies vergeleken thoracotomie (n = 135) en thoracoscopie (n = 37) en konden geen significant verschil aantonen in het voorkomen van AS (p = 0,327). Wel moet rekening gehouden worden met het feit dat thoracoscopische procedures geconverteerd werden naar een open procedure omwille van peroperatieve moeilijkheden in 43/312 (13,8%) procedures. De variatie in de literatuur was echter zeer groot, van 0% tot 58,3%.
De chirurg zal steeds proberen om de slokdarmstompen in één tijd aan elkaar te zetten (een primair herstel), doch soms is dit technisch niet mogelijk en krijgt de patiënt een uitgesteld herstel. Primair herstel werd gecompliceerd door een postoperatieve AS in 26,6% (190/714) van de patiënten, terwijl dit bij uitgesteld herstel in 43,7% (59/135) van de patiënten het geval was. De vier studies die primair (n = 206) en uitgesteld (n = 79) herstel vergeleken, konden echter geen significant verschil aantonen in het voorkomen van AS (p = 0,614).
De manier waarop de slokdarmstompen aan elkaar gehecht werden bij primair herstel werd expliciet vermeld bij 142 patiënten (drie studies) die een end-to-end anastomose (E-E) kregen en bij 102 (twee studies) die een end-to-side anastomose (E-S) kregen. Een strictuur was aanwezig bij 35,9% (51/142 patiënten) van de E-E anastomose en bij 6,9% (7/102) van de E-S anastomose. Bij twee studies werd een vergelijking gemaakt tussen de E-E (n=83) en de E-S (n=102) techniek. Er was een significante verhoging van het risico op AS bij de E-E anastomose in vergelijking met E-S anastomose (p < 0,0001).
Verder werden er nog twee andere alternatieve anastomose technieken beschreven, de “oblique anastomose” (n=16) en de “plus incisie” (n=11) in een beperkt aantal patiënten, waarbij geen (0%) stricturen optraden.
Bij de ingreep kan soms ook door de chirurg vastgesteld worden dat de slokdarmuiteinden slechts aan elkaar gehecht konden worden mits tractie op de slokdarmstompen. Dit was geassocieerd met een significant hogere frequentie aan AS (p < 0,001). Bij de aanwezigheid van tractie op de naad ontwikkelde 73,9% een AS, ten opzichte van 38,5% van de patiënten die geen tractie had.
Tabel 3: Operatieve technieken en associatie met ontstaan van AS.
Techniek anastomose
Prevalentie AS Associatie operatieve techniek met AS
p -waarde Studies (n) Patiënten met AS Studies (n) Patiënten (n) AS Geen AS Thoracoscopie Thoracotomie 13 15 176 / 664 (26,5%) 105 / 287 (36,6%) 3 37 135 12 (32,4%) 33 (24,5%) 25 (67,6%) 102 (75,5%) 0,327 (NS) Primair Uitgesteld 17 8 190 / 714 (26,6%) 59 / 135 (43,7%) 4 206 79 64 (31,1%) 27 (34,2%) 142 (68,9%) 52 (65,8%) 0,614 (NS) End-to-end End-to-side 3 2 51 / 142 (35,9%) 7 / 102 (6,9%) 2 83 102 29 (34,9%) 7 (6,9%) 54 (65,1%) 95 (93,2%) <0,001 Plus incisie Oblique 1 1 0 / 11 (0%) 0 / 16 (0%) 2 11 16 0 (0%) 0 (0%) 11 (100%) 16 (100%) / Factor
Prevalentie factor Associatie factor met AS
p -waarde Studies (n) Patiënten (n) Studies (n) met / zonder factor (n/n) AS met factor AS zonder factor Tractie 12 197 / 811 (24,3%) 4 46 / 109 34 (73,9%) 42 (38,5%) <0,001 NS = niet significant
2.3.
Peri- en postoperatieve factoren
De peri- en postoperatieve risicofactoren voor AS, vermeld in de literatuur, werden samengevat in Tabel 4.
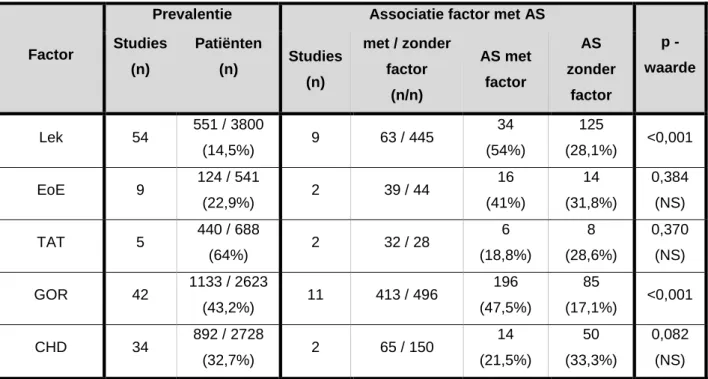
Een ingreep werd gecompliceerd door een postoperatieve lek ter hoogte van de naad in 14,5% van de OA patiënten. Dit ging gepaard met een significant verhoogd risico op AS (p < 0,001). Bij de aanwezigheid van een postoperatief lek steeg het risico op AS naar 53,9% ten opzichte van
Na de ingreep wordt soms een transanastomotische nasogastrische tube (TAT) achtergelaten. Dit was niet geassocieerd met een toename aan AS (p = 0,370). Bij plaatsing van een TAT ontwikkelde 18,8% een strictuur ten opzichte van 28,6% waarbij er geen TAT geplaatst werd.
Het risico op het ontwikkelen van een eosinofiele oesophagitis (EoE) is hoger bij patiënten met OA. Er was echter geen associatie met het ontwikkelen van AS (p = 0,384). Bij 41% van de patiënten met EoE trad een AS op, ten opzichte van 31,8% zonder EoE.
Bij 43,2% van de OA populatie werd de diagnose gastro-oesophageale reflux (GOR) gesteld aan de hand van pH-monitoring of pH-impedantie. Bij het bundelen van de resultaten werd een significante associatie gevonden tussen GOR en AS (p < 0,001). Patiënten met GOR hadden in 47,5% een AS ten opzichte van 17,1% van de patiënten zonder GOR.
GOR werd behandeld met zuurremmers (PPI of H2A) of een anti-reflux operatie (maagfundoplicatie) in 17,2% patiënten.
Zuurremming wordt echter niet alleen op indicatie van GOR gestart, maar soms ook profylactisch. In het totaal werd dit gerapporteerd bij 65,3% van de OA patiënten (1871/2865) in de studies die hierover informatie meegaven. De meerderheid van OA patiënten werd profylactisch behandeld (n=810), 310 patiënten kregen een therapeutische behandeling en bij 751 patiënten was de indicatie niet gekend. Er werden twee groepen zuurremmers beschreven, de protonpomp-inhibitoren (PPI’s) en de H2-receptorantagonisten (H2A). In de literatuur werden 641 patiënten (34,3%) behandeld met PPI, 491 (26,2%) met H2A, 78 patiënten (4,2%) kregen synchrone behandeling van PPI en H2A en bij de resterende 661 patiënten was er onduidelijkheid (35,3%). De relatie tussen profylactische zuurremming en AS werd onderzocht in 707 patiënten, waarvan 43,6% (308 patiënten) een AS ontwikkelde. Opnieuw werden verschillende profylactische regimes beschreven: 412 patiënten (58,3%) PPI, 17 patiënten (2,4%) H2A en onbekend bij 278 patiënten (39,3%).
Aangeboren malformaties zoals congenitale hartdefecten (CHD) komen frequent voor in de OA populatie. In de literatuur werd een prevalentie beschreven van 32,7%. Deze prevalentie varieerde zeer sterk van 5,2% - 77,8%. Er waren slechts twee studies die de relatie tussen CHD en ontstaan van strictuur onderzochten. AS trad op bij 8 van patiënten met CHD (8/55, 14,5%), in vergelijking met 18 patiënten (18/66, 27,3%) zonder CHD. Er werd geen significant verband aangetoond (p = 0,090). Een andere studie onderzocht de relatie “ernstig CHD” in vergelijking met “matig of geen CHD”, waarbij vooral kinderen met ernstige CHD (n=10) vaker AS ontwikkelden (6/10, 60%). Van de 84 patiënten zonder CHD of met een mildere vorm van CHD, ontwikkelden 32 patiënten (38,1%)
een AS. De aanwezigheid van “ernstige CHD” had geen significante invloed op het ontstaan van AS (p = 0,306). Er was globaal geen significante associatie van CHD met het voorkomen van AS (p = 0,082).
Tabel 4: Peri- en postoperatieve risicofactoren en associatie met het ontstaan van AS.
Factor
Prevalentie Associatie factor met AS
p -waarde Studies (n) Patiënten (n) Studies (n) met / zonder factor (n/n) AS met factor AS zonder factor Lek 54 551 / 3800 (14,5%) 9 63 / 445 34 (54%) 125 (28,1%) <0,001 EoE 9 124 / 541 (22,9%) 2 39 / 44 16 (41%) 14 (31,8%) 0,384 (NS) TAT 5 440 / 688 (64%) 2 32 / 28 6 (18,8%) 8 (28,6%) 0,370 (NS) GOR 42 1133 / 2623 (43,2%) 11 413 / 496 196 (47,5%) 85 (17,1%) <0,001 CHD 34 892 / 2728 (32,7%) 2 65 / 150 14 (21,5%) 50 (33,3%) 0,082 (NS) NS = niet significant
3. Strictuur behandeling
De standaardbehandeling van AS bestaat uit het dilateren van de anastomotische vernauwing met ballon en/of bougie.
Van de 1259 patiënten (25,2% van de totale onderzoekspopulatie) met gegevens over dilatatie, ondergingen 274 patiënten (21,8%) ballon dilatatie, 93 patiënten (7,4%) bougie dilatatie en bij 892 patiënten (70,8%) was de dilatatie methode niet gespecificeerd.
Deze dilataties konden met fluoroscopie (5 studies, 6,8 %) of endoscopie (13 studies, 17,8%) begeleid worden, waarvan in vier publicaties beide methodes gebruikt werden. In de resterende studies (75,4%) was dit niet gegeven. Voor de diameter bepaling van de dilatatie, was slechts in drie studies hiervoor een referentie te vinden, namelijk volgens de diameter van de duim van het kind.
Zowel routinedilatatie van asymptomatische stricturen, als selectieve dilataties van klinisch significante symptomatische stricturen werden uitgevoerd in dit literatuuronderzoek. Van de 1259 patiënten met gegevens over dilatatie, ondergingen 552 patiënten (43,8%) een selectieve dilatatie, 80 patiënten (6,4%) ondergingen routine dilatatie naar aanleiding van postoperatieve routine controle contrast oesophagografie of endoscopie. Van de overblijvende 627 patiënten (49,8%) was er onduidelijkheid over de indicatie voor dilatatie omwille van de vage definiëring van strictuur in deze 39 studies.
Discussie
Aangezien OA een congenitale aandoening van de slokdarm is die postoperatief gepaard gaat met belangrijke morbiditeit waaronder AS, werd met dit literatuuroverzicht gepoogd om een beter inzicht te krijgen in de prevalentie en risico factoren op het ontwikkelen van AS: enerzijds om ouders hierover te informeren, anderzijds om de huidige aanpak aan te passen en zo het risico in de toekomst te beperken.
De geïncludeerde studies bestonden voor 90,4% (66/73) uit retrospectief onderzoek of case series wat de kwaliteit van de bekomen resultaten negatief beïnvloed. Er waren weinig prospectieve interventie studies (9,6%, 7/73) om de getrokken besluiten te ondersteunen. Ondanks het feit dat lange termijn prospectieve opvolgstudies voor een zeldzame aandoening moeilijk realiseerbaar zijn, vormt de kwaliteit van de beschikbare literatuur een belangrijke beperking voor dit onderzoek. Eventueel zou het aanleggen van een nationaal register over deze problematiek een oplossing kunnen zijn, gezien de patiënten dan systematisch prospectief opgevolgd worden.
AS blijft één van de frequente complicaties na OA herstel, waarvan de frequentie in de literatuur sterk varieerde (van 0% tot 76,2%). Deze variatie werd zeker voor een stuk beïnvloed door de variabele definitie van strictuur. Zoals vermeld in de resultaten waren er onderzoeksgroepen die systematisch onderzoeken uitvoerden om vernauwingen op te sporen, waarvan de klinische relevantie niet steeds duidelijk was, terwijl anderen eerder wachtten op klinische last. Om in de toekomst in staat te zijn resultaten te vergelijken, zal het belangrijk zijn dezelfde definities te gebruiken. Voor de meer complexere stricturen zoals recurrente en refractaire stricturen, werd er wel reeds een consensus definitie geformuleerd in de ESPGHAN-ESGE richtlijnen (14).
Het gebrek aan een universele definitie van AS bemoeilijkte ook het bepalen van risicofactoren en beïnvloedt mogelijk de resultaten foutief.
Er werd een duidelijke associatie aangetoond tussen het type slokdarmatresie en de frequentie van AS. Sommige types OA kwamen echter zeer zelden voor, waardoor het aantal onderzochte patiënten sterk varieerde.
Een grotere afstand tussen de twee stompen was eveneens geassocieerd met significant meer AS. Doch wegens de onduidelijkheid in de literatuur over de definitie van “long gap” OA, is het vergelijken van studieresultaten ook hier moeilijk. Vervolgens moet ook hier het verschil in populatie
de resultaten. Wanneer de afstand tussen de slokdarmstompen groot is dan verhoogt het risico op een uitgesteld herstel of een slokdarm vervangende ingreep. De literatuurstudie toonde aan dat AS procentueel meer voorkwam bij uitgesteld herstel. Dit kan een gevolg zijn van de indicatie voor een uitgestelde operatie of de oesophageale verlengingsprocedure die gebruikt werd. Tenslotte zal ook tractie op de naad geassocieerd zijn met AS. Dit kan beïnvloed zijn door het feit dat tractie op de naad frequent het gevolg is van een lange afstand tussen beide stompen, anderzijds kunnen operatietechnieken die de stompen mobiliseren eveneens een invloed hebben op de tractie. Tenslotte is er eveneens het verband tussen anastomotische tractie en lekkage van de naad. Het literatuur onderzoek toonde aan dat de lengte van de gap, het optreden van lekkage en de aanwezigheid van tractie op de naad allemaal significant vaker geassocieerd waren met het optreden van AS. Gezien de factoren echter ook onderling aan elkaar verbonden zijn, is het moeilijk om te weten welke factoren de belangrijkste zijn. Hiervoor zou een multivariate analyse moeten gebeuren, doch deze was op basis van de huidige literatuur niet mogelijk.
De operatieve benaderingstechniek (thoracotomie of thoracoscopie) kon statistisch slechts in een kleine subgroep geanalyseerd worden en was niet significant geassocieerd met AS. In de literatuur is er echter nog steeds discussie. Brain et al. (15) beschreven meer AS na thoracotomie, Nice et al. (16) meer AS na thoracoscopie, terwijl Lin et al. (17) daarentegen geen verschil zagen. Beide heelkundige benaderingstechnieken zijn equivalent volgens de meerderheid van de studies, met uitzondering van Nice et al. (16) waar een multivariate analyse werd uitgevoerd en thoracoscopie geassocieerd was met verhoogd risico op AS. Deze uiteenlopende besluiten het gevolg zijn van verschillen in indicatiestelling tot thoracoscopie, leercurve van de chirurg en nood tot conversie. Opnieuw kunnen verschillen in de populatie grootte de resultaten beïnvloeden. Thoracoscopische benadering werd geassocieerd met minder pijn, snellere extubatie, snellere orale voeding en kortere hospitalisatie. Gezien de incisies kleiner zijn, werden er ook cosmetische voordelen als gevolg van het sparen van de intercostale spieren, preventie van scoliosis en het vermijden van n. thoracicus longus letsels (wig scapula) eraan geassocieerd (17). De techniek is echter niet mogelijk bij alle patiënten. Een laag geboortegewicht, CHD, long gap OA en slechte algemene toestand maken de benadering moeilijk (16, 17). Perioperatieve moeilijkheden kunnen het converteren naar een thoracotomische procedure noodzakelijk maken (17, 18). Gerandomiseerde studies zijn nodig om aan te duiden welke techniek nu superieur is.
De anastomosetechniek om de slokdarmstompen aan elkaar vast te hechten (to-end of end-to-side) was significant geassocieerd met het ontstaan van AS. Uit dit literatuuronderzoek kan
besloten worden dat E-S anastomose significant geassocieerd was met een lager risico op AS. Mogelijke verklaring hiervoor is de bewaring van de segmentale bevloeiing, waardoor de mucosale doorbloeding bewaard blijft. Het gevolg hiervan is lagere kans op ischemie en in de praktijk bleek dit ook het voorkomen AS te minderen (19).
Andere anastomose technieken zoals de “oblique anastomose” (n = 16) beschreven door Catalano et al. (20) en “plusvormige incisie met zigzaganastomose” (n = 11) beschreven door Melek et al. (21) zouden helemaal niet gepaard gaan met AS. Zij postuleerden dat de verlenging van de sutuur zou ervoor zorgen dat er minder tractie per oppervlakte is, waardoor de neiging om te vernauwen zou afnemen. Beide onderzochte populaties waren echter zeer klein, bovendien werden enkel patiënten geïncludeerd waarbij geen tractie op de naad was en tenslotte werd er geen duidelijke definitie van strictuur gehanteerd. Deze technieken werden tot op heden nog niet beschreven in andere centra. Toekomstig onderzoek zal de nieuwe techniek moeten vergelijken met de klassieke in een vergelijkbare patiënten populatie om resultaten te weerleggen of bevestigen.
Het achterlaten van een transanastomotische nasogastrische sonde was niet geassocieerd met het voorkomen van AS, maar gaf wel de mogelijkheid om snel met enterale voeding te starten (22).
GOR trad op bij 43,2% van de OA patiënten na de corrigerende ingreep voor OA. De oorzaak is meest waarschijnlijk multifactorieel. Transiënte distale slokdarm-sfincterrelaxatie, intrinsieke slokdarmdysmotiliteit, een korter intra-abdominale slokdarmsegment, peroperatieve beschadiging van de nervus vagus en anatomische verandering in de hoek van His zijn factoren die hierin een rol zouden kunnen spelen. De diagnostische techniek (pH-monitoring of pH-impedantie) kan een invloed hebben op de beschreven prevalentie.
GOR wordt standaard behandeld met zuurremmers. Bij onvoldoende controle met medicamenteuze therapie zal anti-reflux chirurgie (maagfundoplicatie) overwogen worden, dit gebeurde bij 17, 2% van de patiënten. GOR was significant geassocieerd met het optreden van AS, doch de studie resultaten varieerden sterk. Deze variatie kan het gevolg zijn van de manier waarop GOR gediagnosticeerd werd en het al dan niet gebruik van profylactische zuurremming. De huidige NASPGHAN-ESPGHAN richtlijnen adviseren om kinderen met OA gedurende het eerste levensjaar te behandelen met zuurremming om GOR te voorkomen, vervolgens een pH-impedantie uit te voeren om de verdere behandeling te sturen. In verdere opvolging moet regelmatig gescreend worden naar het optreden van GOR bij deze kinderen, zelf tot in de adolescentie (3).
43,6% hiervan ontwikkelde een AS. Dit is vergelijkbaar met de normale frequentie van AS in een OA populatie, waaruit dan besloten kan worden dat het profylactisch toedienen van zuurremmers niet geassocieerd is met voorkomen van AS. Langdurige profylactische toediening van H2A zou volgens Murase et al. (23) geassocieerd zijn met minder frequent optreden van AS op lange termijn, terwijl kortdurende profylaxie geen invloed had. Retrospectieve studies met PPI profylactische anti-reflux therapie (PARM) waren niet geassocieerd met een vermindering van de AS in vergelijking met een historische controlegroep (24-26). Door te vergelijken met een historische controle groep met eventueel gedateerde en ongestandaardiseerde zorg kunnen de resultaten beïnvloed worden (26). Vergelijking met een gerandomiseerde gelijkaardige cohorte verkiest de voorkeur. De duur van PARM toediening is variabel in de literatuur gaande van 3 maand tot 1 jaar, doch kon eveneens met de verlengde therapie geen significant verschil op het voorkomen van AS bekomen worden (27). Er moet verder onderzocht worden of het nuttig is om deze PARM te integreren in het beleid, aan welke dosis en hoelang deze dan gecontinueerd moet worden postoperatief om zijn eventuele protectieve effect te bereiken. Bovendien werd er in de literatuur erg weinig aandacht geschonken aan de nadelige lange termijneffecten van PPI toediening, namelijk invloed op het microbioom en verhoogd risico pulmonaire en gastrointestinale infecties. Ondanks afwezigheid van evidentie voor profylactische zuurremming postoperatief, suggereren huidige NASPGHAN-ESPGHAN richtlijnen dat elk kind na EA correctie profylactisch behandeld moet worden met PPI’s gedurende 1 jaar (3). EoE had in dit literatuuronderzoek geen significante associatie met het ontstaan van AS. Chan et al. (28) toonde echter aan dat de behandeling van EoE het voorkomen van strictuur en het aantal dilatatiesessies significant verminderde. Er wordt geadviseerd EoE te excluderen bij strictuur met GOR alvorens over te gaan tot chirurgische reflux-operaties (maagfundicoplastie) aan de hand van endoscopie met bioptname (3).
In dit literatuur onderzoek had CHD geen significante associatie met het ontstaan van AS. Nice et al. (16) daarentegen concludeerden met een multivariate analyse dat de aanwezigheid van CHD geassocieerd was met een lager risico op AS. Dit verschil kan te verklaren zijn door een selectie van CHD patiënten met een lager AS risico als gevolg van de exclusie van gestorven kinderen uit deze publicatie. Het feit dat kinderen met CHD en verhoogd risico op AS, eventueel een grotere kans hebben om te sterven, zou een mogelijk verstorende factor kunnen geweest zijn. De associatie van ernstig CHD met een type OA dat mogelijk frequenter gepaard gaan met AS zou hierin ook een verstorende factor kunnen zijn en moet zeker meegenomen worden in toekomstig onderzoek.
NASPGHAN-ESPGHAN richtlijnen adviseren AS enkel als klinisch relevant te beschouwen bij patiënten met symptomen (3). De huidige literatuur bevat echter ook veel studies waarbij er gescreend werd voor vernauwing postoperatief en zo werden dus asymptomatische stricturen eveneens gedilateerd. Koivusalo et al. (29) vergeleken dilatatie op symptomatische indicatie en op routinematige indicatie tijdens de derde week postoperatief. Ze toonden aan dat de resultaten bij beide indicaties gelijk waren maar routinedilataties leidden tot meer dilatatiesessies om hetzelfde resultaat te bekomen. Symptomatische stricturen bleken niet moeilijker te behandelen zijn. In dit literatuuronderzoek werd hoofdzakelijk gedilateerd met ballon (21,8% ballon, 7,4% bougie). Lang et al. (30) concludeerden dat ballon dilatatie minder traumatisch en effectiever was dan traditionele bougienage met Savillary-Gilliard, gezien minder dilatatiesessies nodig waren.
Er wordt geadviseerd om met de dilatatie een normale oesophageale diameter voor de leeftijd te beoogen. Er is echter geen consensus in de literatuur over de ideale diameter, noch over het interval tussen de dilatatiesessies (3). Over de diameter bepaling van de dilatatie was weinig informatie te vinden in de literatuur, slechts drie studies vermelden de diameter van de duim van het kind als referentie(27, 31, 32). Bott et al. (33) onderzochten in 2018 bij kinderen de correlatie tussen de oesophageale diameters en het gewicht. Het zou nuttig kunnen zijn om aan de hand van deze normaalwaarden in de toekomst voor de definiëring alsook voor bepaling van de diameter tot welke men moet dilateren.
Dit literatuuronderzoek toonde aan dat een lange afstand tussen beide oesophagusstompen, tractie op de anastomose, end-to-end anastomose, lekkage en gastro-oesophageale reflux risicofactoren zijn op het ontwikkelen van AS. Deze informatie kan helpen om de ouders te informeren over het potentieel risico op AS en anderzijds om huidige aanpak aan te passen en het risico in de toekomst te beperken. Verder onderzoek kan gebeuren, maar vereist eenduidige definiëring van AS.
Referentielijst
1. Baird R, Laberge JM, Levesque D. Anastomotic stricture after esophageal atresia repair: a critical review of recent literature. Eur J Pediatr Surg. 2013;23(3):204-13.
2. Pini Prato A, Carlucci M, Bagolan P, Gamba PG, Bernardi M, Leva E, et al. A cross-sectional nationwide survey on esophageal atresia and tracheoesophageal fistula. J Pediatr Surg. 2015;50(9):1441-56.
3. Krishnan U, Mousa H, Dall'Oglio L, Homaira N, Rosen R, Faure C, et al. ESPGHAN-NASPGHAN Guidelines for the Evaluation and Treatment of Gastrointestinal and Nutritional Complications in Children With Esophageal Atresia-Tracheoesophageal Fistula. J Pediatr Gastroenterol Nutr. 2016;63(5):550-70.
4. Smith N. Oesophageal atresia and tracheo-oesophageal fistula. Early Hum Dev. 2014;90(12):947-50.
5. Long AM, Tyraskis A, Allin B, Burge DM, Knight M. Oesophageal atresia with no distal tracheoesophageal fistula: Management and outcomes from a population-based cohort. J Pediatr Surg. 2017;52(2):226-30.
6. Teague WJ, Karpelowsky J. Surgical management of oesophageal atresia. Paediatr Respir Rev. 2016;19:10-5.
7. van der Zee DC, Bagolan P, Faure C, Gottrand F, Jennings R, Laberge JM, et al. Position Paper of INoEA Working Group on Long-Gap Esophageal Atresia: For Better Care. Front Pediatr. 2017;5:63.
8. Haight C. Congenital Atresia of the Esophagus With Tracheoesophageal Fistula : Reconstruction of Esophageal Continuity by Primary Anastomosis. Ann Surg. 1944;120(4):623-52. 9. Serhal L, Gottrand F, Sfeir R, Guimber D, Devos P, Bonnevalle M, et al. Anastomotic stricture after surgical repair of esophageal atresia: frequency, risk factors, and efficacy of esophageal bougie dilatations. J Pediatr Surg. 2010;45(7):1459-62.
10. Rintala RJ, Pakarinen MP. Long-term outcome of esophageal anastomosis. Eur J Pediatr Surg. 2013;23(3):219-25.
11. Sun LY, Laberge JM, Yousef Y, Baird R. The Esophageal Anastomotic Stricture Index (EASI) for the management of esophageal atresia. J Pediatr Surg. 2015;50(1):107-10.
12. van der Zee DC, Gallo G, Tytgat SH. Thoracoscopic traction technique in long gap esophageal atresia: entering a new era. Surg Endosc. 2015;29(11):3324-30.
13. Tambucci R, Angelino G, De Angelis P, Torroni F, Caldaro T, Balassone V, et al. Anastomotic Strictures after Esophageal Atresia Repair: Incidence, Investigations, and Management, Including Treatment of Refractory and Recurrent Strictures. Front Pediatr. 2017;5:120.
14. Thomson M, Tringali A, Dumonceau JM, Tavares M, Tabbers MM, Furlano R, et al. Paediatric Gastrointestinal Endoscopy: European Society for Paediatric Gastroenterology Hepatology and Nutrition and European Society of Gastrointestinal Endoscopy Guidelines. J Pediatr Gastroenterol Nutr. 2017;64(1):133-53.
15. Lugo B, Malhotra A, Guner Y, Nguyen T, Ford H, Nguyen NX. Thoracoscopic versus open repair of tracheoesophageal fistula and esophageal atresia. J Laparoendosc Adv Surg Tech A. 2008;18(5):753-6.
16. Nice T, Tuanama Diaz B, Shroyer M, Rogers D, Chen M, Martin C, et al. Risk Factors for Stricture Formation After Esophageal Atresia Repair. J Laparoendosc Adv Surg Tech A. 2016;26(5):393-8.
17. Lin CH, Duh YC, Fu YW, Hsu YJ, Wei CH. Thoracoscopic repair of esophageal atresia: Comparison with open approach. Formosan Journal of Surgery. 2018;51(3):105-10.
18. Hiradfar M, Gharavifard M, Shojaeian R, Joodi M, Nazarzadeh R, Sabzevari A, et al. Thoracoscopic Esophageal Atresia with Tracheoesophageal Fistula Repair: The First Iranian Group Report, Passing the Learning Curve. J Neonatal Surg. 2016;5(3):29.
19. Touloukian RJ, Seashore JH. Thirty-five-year institutional experience with end-to-side repair for esophageal atresia. Arch Surg. 2004;139(4):371-4; discussion 4.
20. Catalano P, Di Pace MR, Caruso AM, Salerno S, Cimador M, De Grazia E. A simple technique of oblique anastomosis can prevent stricture formation in primary repair of esophageal atresia. J Pediatr Surg. 2012;47(9):1767-71.
21. Melek M, Cobanoglu U. A new technique in primary repair of congenital esophageal atresia preventing anastomotic stricture formation and describing the opening condition of blind pouch: plus ("+") incision. Gastroenterology research and practice. 2011;2011:527323.
22. Alabbad SI, Ryckman J, Puligandla PS, Shaw K, Nguyen LT, Laberge JM. Use of transanastomotic feeding tubes during esophageal atresia repair. J Pediatr Surg. 2009;44(5):902-5.
23. Murase N, Uchida H, Kaneko K, Ono Y, Makita S, Yokota K. Prophylactic effect of H2 blocker for anastomotic stricture after esophageal atresia repair. Pediatr Int. 2015;57(3):461-4. 24. Donoso F, Lilja HE. Risk Factors for Anastomotic Strictures after Esophageal Atresia Repair: Prophylactic Proton Pump Inhibitors Do Not Reduce the Incidence of Strictures. Eur J Pediatr Surg. 2017;27(1):50-5.
25. Righini Grunder F, Petit LM, Ezri J, Jantchou P, Aspirot A, Laberge S, et al. Should Proton Pump Inhibitors be Systematically Prescribed in Patients With Esophageal Atresia After Surgical Repair? J Pediatr Gastroenterol Nutr. 2019;69(1):45-51.
26. Hagander L, Muszynska C, Arnbjornsson E, Sandgren K. Prophylactic treatment with proton pump inhibitors in children operated on for oesophageal atresia. Eur J Pediatr Surg. 2012;22(2):139-42.
27. Stenstrom P, Anderberg M, Borjesson A, Arnbjornsson E. Prolonged Use of Proton Pump Inhibitors as Stricture Prophylaxis in Infants with Reconstructed Esophageal Atresia. Eur J Pediatr Surg. 2017;27(2):192-5.
28. Chan LJ, Tan L, Dhaliwal J, Briglia F, Clarkson C, Krishnan U. Treatment outcomes for eosinophilic esophagitis in children with esophageal atresia. Dis Esophagus. 2016;29(6):563-71. 29. Koivusalo A, Pakarinen MP, Rintala RJ. Anastomotic dilatation after repair of esophageal atresia with distal fistula. Comparison of results after routine versus selective dilatation. Dis Esophagus. 2009;22(2):190-4.
30. Lang T, Hummer HP, Behrens R. Balloon dilation is preferable to bougienage in children with esophageal atresia. Endoscopy. 2001;33(4):329-35.
31. Salo M, Stenstrom P, Anderberg M, Arnbjornsson E. Anastomotic Strictures after Esophageal Atresia Repair: Timing of Dilatation during the First Two Postoperative Years. Surg J (N Y). 2018;4(2):e62-e5.
32. Stenström P, Salö M, Anderberg M, Arnbjörnsson E. Congenital heart disease and its impact on the development of anastomotic strictures after reconstruction of esophageal atresia. Gastroenterology Research and Practice. 2018;2018.
33. Bott TS, von Kalle T, Schilling A, Diez OH, Besch S, Mehlig U, et al. Esophageal Diameters in Children Correlated to Body Weight. Eur J Pediatr Surg. 2019;29(6):528-32.
34. Lal DR, Gadepalli SK, Downard CD, Ostlie DJ, Minneci PC, Swedler RM, et al. Perioperative management and outcomes of esophageal atresia and tracheoesophageal fistula. J Pediatr Surg. 2017;52(8):1245-51.
35. Macchini F, Parente G, Morandi A, Farris G, Gentilino V, Leva E. Classification of Esophageal Strictures following Esophageal Atresia Repair. Eur J Pediatr Surg. 2018;28(3):243-9.
36. Friedmacher F, Kroneis B, Huber-Zeyringer A, Schober P, Till H, Sauer H, et al. Postoperative Complications and Functional Outcome after Esophageal Atresia Repair: Results from Longitudinal Single-Center Follow-Up. J Gastrointest Surg. 2017;21(6):927-35.
37. Masuya R, Kaji T, Mukai M, Nakame K, Kawano T, Machigashira S, et al. Predictive factors affecting the prognosis and late complications of 73 consecutive cases of esophageal atresia at 2 centers. Pediatric Surgery International. 2018;34(10):1027-33.
38. Shah R, Varjavandi V, Krishnan U. Predictive factors for complications in children with esophageal atresia and tracheoesophageal fistula. Dis Esophagus. 2015;28(3):216-23.
39. Zhu H, Wang M, Zheng S, Dong K, Xiao X, Shen C. Diagnosis and management of post-operative complications in esophageal atresia patients in China: A retrospective analysis from a single institution. International Journal of Clinical and Experimental Medicine. 2018;11(1):254-61. 40. Peyvasteh M, Askarpour S, Shoushtari MHS. A study of esophageal strictures after surgical repair of esophageal atresia. Pakistan Journal of Medical Sciences. 2006;22(3):269-72.
41. Allin B, Knight M, Johnson P, Burge D. Outcomes at one-year post anastomosis from a national cohort of infants with oesophageal atresia. PLoS One. 2014;9(8):e106149.
42. Michaud L, Guimber D, Sfeir R, Rakza T, Bajja H, Bonnevalle M, et al. Anastomotic stricture following the surgical repair of esophageal atresia: Frequency, risk factors, and the efficacy of esophageal dilatation. Archives de Pediatrie. 2001;8(3):268-74.
43. Parolini F, Leva E, Morandi A, Macchini F, Gentilino V, Di Cesare A, et al. Anastomotic strictures and endoscopic dilatations following esophageal atresia repair. Pediatric surgery international. 2013;29(6):601-5.
44. Vergouwe FWT, Vlot J, H IJ, Spaander MCW, van Rosmalen J, Oomen MWN, et al. Risk factors for refractory anastomotic strictures after oesophageal atresia repair: a multicentre study. Arch Dis Child. 2018.
45. Ortiz R, Galan AS, Martinez L, Dominguez E, Hernandez F, Santamaria ML, et al. Tertiary surgery for complicated repair of esophageal atresia. Eur J Pediatr Surg. 2015;25(1):20-6.
46. Pesce M, Krishnan U, Saliakellis E, Lopez R, Lindley KJ, Thapar N, et al. Is There a Role for pH Impedance Monitoring in Identifying Eosinophilic Esophagitis in Children with Esophageal Atresia? Journal of Pediatrics. 2019;210:134-40.
47. Petit LM, Righini F, Ezri J, Jantchou P, Aspirot A, Soglio DD, et al. Prevalence and Predictive Factors of Histopathological Complications in Children with Esophageal Atresia. Eur J Pediatr Surg. 2018.
48. Dhaliwal J, Tobias V, Sugo E, Varjavandi V, Lemberg D, Day A, et al. Eosinophilic esophagitis in children with esophageal atresia. Dis Esophagus. 2014;27(4):340-7.
49. Uchida K, Inoue M, Otake K, Okita Y, Morimoto Y, Araki T, et al. Efficacy of postoperative elective ventilatory support for leakage protection in primary anastomosis of congenital esophageal atresia. Pediatric surgery international. 2006;22(6):496-9.
50. Ferrand A, Roy SK, Faure C, Moussa A, Aspirot A. Postoperative noninvasive ventilation and complications in esophageal atresia–tracheoesophageal fistula. J Pediatr Surg. 2019;54(5):945-8.
51. Nagaya M, Kato J, Niimi N, Tanaka S, Iio K. Proposal of a novel method to evaluate anastomotic tension in esophageal atresia with a distal tracheoesophageal fistula. Pediatric surgery international. 2005;21(10):780-5.
52. Iwanczak BM, Kosmowska-Miskow A, Kofla-Dlubacz A, Palczewski M, Grabinski M, Pawlowska K, et al. Assessment of Clinical Symptoms and Multichannel Intraluminal Impedance and pH Monitoring in Children After Thoracoscopic Repair of Esophageal Atresia and Distal Tracheoesophageal Fistula. Adv Clin Exp Med. 2016;25(5):917-22.
53. Cartabuke RH, Lopez R, Thota PN. Long-term esophageal and respiratory outcomes in children with esophageal atresia and tracheoesophageal fistula. Gastroenterol Rep (Oxf). 2016;4(4):310-4.
54. Banjar HH, Al-Nassar SI. Gastroesophageal reflux following repair of esophageal atresia and tracheoesophageal fistula. Saudi Med J. 2005;26(5):781-5.
55. Goodarzi M, Khazaei HA, Ashjaei B, Ghavami M, Mollaeian M, Bigdeli N, et al. Esophageal atresia: Recent five years’ mortality and morbidity. Acta Medica Iranica. 2018;56(10):660-4. 56. Seo J, Kim DY, Kim AR, Kim DY, Kim SC, Kim IK, et al. An 18-year experience of tracheoesophageal fistula and esophageal atresia. Korean J Pediatr. 2010;53(6):705-10.
57. Mortell AE, Azizkhan RG. Esophageal atresia repair with thoracotomy: the Cincinnati contemporary experience. Seminars in pediatric surgery. 2009;18(1):12-9.
58. van der Zee DC, Tytgat SHA, van Herwaarden MYA. Esophageal atresia and tracheo-esophageal fistula. Seminars in Pediatric Surgery. 2017;26(2):67-71.
59. Chang EY, Chang HK, Han SJ, Choi SH, Hwang EH, Oh JT. Clinical characteristics and treatment of esophageal atresia: a single institutional experience. J Korean Surg Soc. 2012;83(1):43-9.
60. Fonte J, Barroso C, Lamas-Pinheiro R, Silva AR, Correia-Pinto J. Anatomic Thoracoscopic Repair of Esophageal Atresia. Front Pediatr. 2016;4:142.
61. Zhang Z, Huang Y, Su P, Wang D, Wang L. Experience in treating congenital esophageal atresia in China. J Pediatr Surg. 2010;45(10):2009-14.
62. Burford JM, Dassinger MS, Copeland DR, Keller JE, Smith SD. Repair of esophageal atresia with tracheoesophageal fistula via thoracotomy: a contemporary series. Am J Surg. 2011;202(2):203-6.
63. Patel SB, Ade-Ajayi N, Kiely EM. Oesophageal atresia: a simplified approach to early management. Pediatric surgery international. 2002;18(2-3):87-9.
64. Shirota C, Tanaka Y, Tainaka T, Sumida W, Yokota K, Makita S, et al. Therapeutic strategy for thoracoscopic repair of esophageal atresia and its outcome. Pediatric Surgery International. 2019.
65. Nachulewicz P, Zaborowska K, Rogowski B, Kalinska A, Nosek M, Golonka A, et al. Thoracoscopic repair of esophageal atresia with a distal fistula - lessons from the first 10 operations. Wideochir Inne Tech Maloinwazyjne. 2015;10(1):57-61.
66. van der Zee DC, Bax NM. Thoracoscopic repair of esophageal atresia with distal fistula. Surg Endosc. 2003;17(7):1065-7.
67. Dingemann C, Zoeller C, Ure B. Thoracoscopic repair of oesophageal atresia: results of a selective approach. Eur J Pediatr Surg. 2013;23(1):14-8.
68. van der Zee DC, Bax KN. Thoracoscopic treatment of esophageal atresia with distal fistula and of tracheomalacia. Seminars in pediatric surgery. 2007;16(4):224-30.
69. Jönsson L, Friberg LG, Gatzinsky V, Kötz K, Sillén U, Abrahamsson K. Treatment and Follow-Up of Patients with Long-Gap Esophageal Atresia: 15 Years' of Experience from the Western Region of Sweden. European Journal of Pediatric Surgery. 2016;26(2):150-9.
70. Bouguermouh D, Salem A. Esophageal atresia: a critical review of management at a single center in Algeria. Dis Esophagus. 2015;28(3):205-10.
71. Lovvorn IHN, Rothenberg SS, Reinberg O, Yeung CK, Lobe TE. Update on thoracoscopic repair of esophageal atresia with and without tracheoesophageal fistula. Pediatric Endosurgery and Innovative Techniques. 2001;5(2):135-9.
72. Boumas N, D’Hondt B, De Magnee C, Reding R. Surgical treatment of esophageal atresia: our experience after 24 years. Internet Journal of Pediatrics and Neonatology. 2019;21(1).
73. Aldabbagh MH, Abdurrahman KN. Outcome of Children in Esophageal Atresia with Distal Tracheoesophageal Fistula Who Survived after Repair: A Case Series of 20 Cases. Pakistan Paediatric Journal. 2012;36(3):158-63.
74. Schmittenbecher PP. Esophageal atresia - A valid tracer diagnosis for quality assurance? Zentralblatt fur Kinderchirurgie. 2000;9(2):66-72.
75. Orford J, Cass DT, Glasson MJ. Advances in the treatment of oesophageal atresia over three decades: The 1970s and the 1990s. Pediatric Surgery International. 2004;20(6):402-7. 76. Tonz M, Kohli S, Kaiser G. Oesophageal atresia: what has changed in the last 3 decades? Pediatric surgery international. 2004;20(10):768-72.
77. Rothenberg SS, Flake AW. Experience with Thoracoscopic Repair of Long Gap Esophageal Atresia in Neonates. J Laparoendosc Adv Surg Tech A. 2015;25(11):932-5.
78. Sun S, Pan W, Wu W, Gong Y, Shi J, Wang J. Elongation of esophageal segments by bougienage stretching technique for long gap esophageal atresia to achieve delayed primary anastomosis by thoracotomy or thoracoscopic repair: A first experience from China. J Pediatr Surg. 2018;53(8):1584-7.
79. Sri Paran T, Decaluwe D, Corbally M, Puri P. Long-term results of delayed primary anastomosis for pure oesophageal atresia: a 27-year follow up. Pediatric surgery international. 2007;23(7):647-51.
80. MacKinlay GA. Esophageal atresia surgery in the 21st century. Seminars in pediatric surgery. 2009;18(1):20-2.
81. Yamoto M, Nomura A, Fukumoto K, Takahashi T, Nakaya K, Sekioka A, et al. New prognostic classification and managements in infants with esophageal atresia. Pediatric Surgery International. 2018;34(10):1019-26.
82. Yalcin S, Demir N, Serel S, Soyer T, Tanyel FC. The evaluation of deglutition with videofluoroscopy after repair of esophageal atresia and/or tracheoesophageal fistula. J Pediatr Surg. 2015;50(11):1823-7.
83. Van Der Zee DC, Vieirra-Travassos D, De Jong JR, Tytgat SHAJ. A novel technique for risk calculation of anastomotic leakage after thoracoscopic repair for esophageal atresia with distal fistula. World Journal of Surgery. 2008;32(7):1396-9.
84. Okata Y, Maeda K, Bitoh Y, Mishima Y, Tamaki A, Morita K, et al. Evaluation of the intraoperative risk factors for esophageal anastomotic complications after primary repair of esophageal atresia with tracheoesophageal fistula. Pediatric surgery international. 2016;32(9):869-73.
85. Deurloo JA, Ekkelkamp S, Schoorl M, Heij HA, Aronson DC. Esophageal atresia: Historical evolution of management and results in 371 patients. Annals of Thoracic Surgery. 2002;73(1):267-72.
86. Lee S, Lee SK, Seo JM. Thoracoscopic repair of esophageal atresia with tracheoesophageal fistula: overcoming the learning curve. J Pediatr Surg. 2014;49(11):1570-2. 87. Petrosyan M, Estrada J, Hunter C, Woo R, Stein J, Ford HR, et al. Esophageal atresia/tracheoesophageal fistula in very low-birth-weight neonates: improved outcomes with staged repair. J Pediatr Surg. 2009;44(12):2278-81.
88. Yanchar NL, Gordon R, Cooper M, Dunlap H, Soucy P. Significance of the clinical course and early upper gastrointestinal studies in predicting complications associated with repair of esophageal atresia. J Pediatr Surg. 2001;36(5):815-22.
Bijlagen
In bijlage een overzicht van de geïncludeerde artikels en studiekenmerken (Bijlage 1), alsook een overzicht van de statistische resultaten (Bijlage 2).
Bijlage 1: Overzicht geïncludeerde studies.
Referentie Studie type Studieduur (jaar)
populatie EA (n)
Studie besluit
Lal DR (34) Retrospectief 5 396 De zorg is niet gestandaardiseerd, er is veel variatie beschreven in het perioperatieve en postoperatieve beleid bij de verschillende types OA en in de verschillende ziekenhuizen.
Serhal L (9) Retrospectief 5 62 AS is een frequent optredende complicatie na OA herstel. Tractie is een duidelijk significante risicofactor voor het ontwikkelen van AS. Dilatatie met Savary-Gilliard bougie is een veilige en effectieve procedure in het behandelen hiervan.
Macchini F (35) Retrospectief 10 40 De strictuur index (SI) is een goede tool om AS in te delen in ernst en nood aan dilatatie te voorspellen. Long gap OA en tractie zijn
significante risicofactoren voor AS.
Sun LY-C (11) Retrospectief 8 45 De oesophageale anastomotische strictuur index (EASI) is een simpele en reproduceerbare tool om de ernst en ontwikkeling van AS te voorspellen. Het kan nuttig zijn in de opvolging.
Friedmacher F (36)
Prospectief 36 109 Het EA herstel wordt gekarakteriseerd door lage mortaliteit, maar frequente postoperatieve complicaties. Deze complicaties hebben een impact op latere slokdarmfunctie en moeten snel herkend en behandeld worden om deze lange termijn morbiditeit zoveel mogelijk te verminderen.
Masuya R (37) Retrospectief 32 73 GER en AS zijn de frequentste lange termijn comorbiditeit. Cardiale en chromosomale abnormaliteit zijn significant geassocieerd met mortaliteit.
Shah R (38) Retrospectief 11 100 Long gap OA en GER zijn significante risicofactoren voor het ontstaan van vroege en late AS.
Zhu H (39) Retrospectief 6 157 Postoperatieve complicaties zoals AS, lek en GER zijn frequent. Deze moeten in eerste instantie niet chirurgisch aangepakt worden en goed opgevolgd.
Peyvasteh M (40) Retrospectief 1 51 GER en lek zijn significant geassocieerd met AS. Preventie en behandeling van deze complicaties is belangrijk. De anastomotische
Allin B (41) Prospectief 1 86 AS veroorzaakt belangrijke morbiditeit. Het gebruik van PARM is niet effectief ter preventie van stricturen.
Michaud L (42) Retrospectief 5 52 AS is frequent na herstel OA, significant geassocieerd met tractie op de anastomose. GER blijkt geen significante risicofactor te zijn. Behandeling met Savary-Gilliard Bougie is een effectieve techniek, maar vaak zijn er meerdere episodes vereist.
Salö M (31) Retrospectief 7 49 De dilatatienood van de eerste 6 maanden postoperatief voorspelt de dilatatienood na 1 jaar, maar geeft geen indicatie van het aantal dilataties dat vereist zal zijn. In deze studie werd geen significant associatie gevonden voor lek, long gap, GER.
Parolini F (43) Retrospectief 8 35 GER, long gap, tractie zijn significant geassocieerd met de ontwikkeling van AS. De strictuur index (SI) op 1 maand postoperatief kan de ernst van strictuur en nood aan dilatatie voorspellen.
Vergouwe FWT (44)
Retrospectief 14 454 Lekkage, type A OA, uitgesteld herstel, GER zijn significant geassocieerd met AS.
Ortiz R (45) Retrospectief 20 23 Behoud van de eigen slokdarm is in de regel beter voor het kind, maar bij het optreden van herhaalde complicaties na OA herstel, kan radicale chirurgie vereist zijn. Snelle verwijzing naar expertise centra is aangewezen in deze situatie.
Murase N (23) Retrospectief 8 27 Lange termijn behandeling met profylactische H2A voorkomt AS die ontstaan is door GER in de late postoperatieve periode na EA herstel. Anastomotische lek en GER zijn significant geassocieerd met AS.
Donoso F (24) Retrospectief 19 128 Profylactische PPI behandeling heeft geen associatie met het voorkomen van AS. Chirurgen zouden in hoofdzaak moeten proberen de anastomose zonder al te veel tractie te bekomen. Grunder FR (25) Prospectief 11 73 Profylactische PPI behandeling heeft geen associatie met het
voorkomen van AS. Het zorgt integendeel voor meer histologische complicaties en anti-reflux chirurgie, er moet selectiever