DE KLINISCHE EN HEMODYNAMISCHE
RESULTATEN NA IMPLANTATIE VAN
DE TRIFECTA AORTAKLEPPROTHESE
Alexander Dereu
Stamnummer: 01409134
Augustijn Mortelé
Stamnummer: 01505168
Promotor: Prof. dr. Katrien François
Masterproef voorgelegd in het kader tot het behalen van de graad Master of Medicine in de Geneeskunde Academiejaar: 2018 - 2020
Deze pagina is niet beschikbaar omdat ze persoonsgegevens bevat.
Universiteitsbibliotheek Gent, 2021.
This page is not available because it contains personal information.
Ghent University, Library, 2021.
Voorwoord
De masterproef is voor ons een interessante en uitdagende ervaring geweest. We hebben gedurende deze periode veel bijgeleerd en op een intense manier kennis gemaakt met het wetenschappelijk onderzoek. We zouden graag een aantal mensen bedanken die een bijdrage hebben geleverd aan het tot stand komen van deze thesis.
Allereerst willen we onze promotor Prof. dr. Katrien François bedanken voor alle hulp en ondersteuning. Gedurende het hele traject konden we steeds met onze vragen bij haar terecht. Eveneens willen we het secretariaat van de dienst hartchirurgie bedanken voor de tijd die we er konden spenderen om te werken aan onze thesis, en in het bijzonder Martien Everaert en Tania De Bo voor de logistieke ondersteuning.
Tot slot willen we graag onze ouders en vrienden bedanken voor het geven van steun en advies. Met oprechte dank
Inhoudsopgave
1. Abstract ... 1 2. Afkortingen ... 2 3. Inleiding ... 3 3.1 De aortaklep ... 3 3.1.1 Normale anatomie ... 33.1.2 Relatie tot andere kleppen en structuren ... 3
3.1.3 Werking ... 4 3.2 Aortakleppathologie en oorzaken ... 5 3.2.1 Aortaklepstenose ... 5 3.2.1.1 Gecalcifiëerde aortaklepstenose ... 5 3.2.1.2 Bicuspiede aortaklep ... 5 3.2.1.3 Rheumatische aortaklepstenose ... 6 3.2.2 Aortaklepinsufficiëntie ... 6 3.3 Chirurgische behandeling ... 6 3.3.1 Chirurgische indicaties ... 6 3.3.2 Chirurgische technieken ... 7 3.3.3 Types klepprothesen ... 7 3.3.3.1 Mechanische klepprothesen ... 8 3.3.3.2 Biologische klepprothesen ... 8
3.3.4 Resultaten van aortaklepvervanging ... 8
3.4 Trifecta prothese ... 10
4. Doel van de studie ... 12
5. Methode ... 13 5.1 Zoekstrategie ... 13 5.2 Methode en patiënten ... 13 5.3 Database ... 14 5.4 Statistische analyse ... 15 6. Resultaten ... 16 6.1 Klinische resultaten ... 16
6.1.1 Patiëntenkarakteristieken en peroperatieve gegevens ... 16
6.2.1.1 De klepgradiënten ... 24
6.2.1.2 De echoparameters van het LV ... 26
6.2.2 Specifieke klepcomplicaties ... 27 7. Discussie ... 28 7.1 Klinisch ... 28 7.1.1 Mortaliteit en complicaties ... 28 7.1.2 Risicofactoren ... 30 7.2 Hemodynamisch ... 32
7.2.1 Trifecta vs. andere Trifecta studies ... 32
7.2.2 Trifecta vs. sutuurloze kleppen ... 33
7.2.3 Trifecta vs. andere gestente biologische AVR (SAVR) ... 33
7.2.4 Trifecta vs. TAVI ... 34
8. Beperkingen van de studie ... 34
9. Conclusie ... 35
10. Referentielijst ... 36 Addendum ... I 1. Databasegegevens ... I 2. Richtlijnen en definities ... VII
1. Abstract
Doel. De evaluatie van de klinische en hemodynamische resultaten na implantatie van de
Trifecta aortaklepprothese.
Patiënten en methoden. De studie is retrospectief. Alle patiënten bij wie van 01/01/2012 tot en
met 31/12/2017 in het UZ Gent een Trifecta aortaklepprothese werd ingeplant, geïsoleerd of als onderdeel van een gecombineerde ingreep, werden geïncludeerd in de studie (n = 182). De follow-up bedroeg gemiddeld 36 maanden. Uni- en multivariabele analyses werden uitgevoerd om risicofactoren voor mortaliteit en complicaties op te sporen. De hemodynamische gegevens werden via echocardiografische follow-up bekomen.
Resultaten. De gemiddelde leeftijd bij de operatie bedroeg 77 ± 5,5 jaar en 54,9% waren
vrouwen. Het aantal patiëntenjaren follow-up was 475. De Trifecta prothesen van 21 en 23 mm werden het meest geïmplanteerd, respectievelijk 30,2% en 40,1%. De overleving na 1 en 5 jaar bedroeg respectievelijk 85% en 70%. De afwezigheid van structurele dysfunctie na 1 en 5 jaar was respectievelijk 100% en 98%. Endocarditis kwam enkel laattijdig voor (1,8%). Trombose van de Trifecta prothese kwam niet voor. Niet-structurele dysfunctie, voornamelijk kleine
paravalvulaire lekken, was zowel vroeg- als laattijdig een mineure complicatie, respectievelijk 1,6% en 2,4%. Een pre-operatieve VKF was de belangrijkste risicofactor voor complicaties en mortaliteit. De gemiddelde piekgradiënt postoperatief en na 1 jaar follow-up bedroeg
respectievelijk 15 ± 6 en 17 ± 8 mmHg. Er was geen significante stijging van de piekgradiënten vast te stellen gedurende de follow-up.
Conclusie. De Trifecta aortaklepprothese vertoont in deze studie excellente klinische en
hemodynamische resultaten. Zowel de klinische resultaten als de klepspecifieke complicaties zijn vergelijkbaar met bestaande studies over de Trifecta of andere biologische prothesen. Op
hemodynamisch vlak lijkt de Trifecta een voordeel te bieden ten opzichte van de sutuurloze kleppen en andere biologische aortakleppen, zoals de Edwards Magna en Magna Ease, de Mitroflow en de Mosaic.
2. Afkortingen
AHT: Arteriële hypertensie LCO: Low cardiac output
AI: Aortaklepinsufficiëntie LVEF: Linker ventrikel ejectiefractie
AMI: Acuut myocardinfarct LV: Linker ventrikel
AoS: Aortaklepstenose MCV: Medtronic CoreValve
ASD: Atriaal septum defect MV: Mitraalklep
AV-knoop: Atrioventriculaire knoop MVP: Mitraalklepherstel
AVR: Aortaklepvervanging MVR: Mitraalklepvervanging
BSA: Body surface area NOAC: Nieuwe orale anticoagulantia
CABG: Coronary artery bypass grafting NYHA: New York Heart Association
COPD: Chronisch obstructief longlijden PFO: Persisterend foramen ovale
CoZo: Collaboratief Zorgplatform PPM: Patient-prosthesis mismatch
CVA: Cerebrovasculair accident RIND: Reversible ischemic neurologic deficit
Cx: Circumflex SAVR: Surgical aortic valve replacement
DB: Diastolische bloeddruk SB: Systolische bloeddruk
ECC: Extracorporele circulatie SD: Standaarddeviatie
EOA: Effective orifice area TAVI: Transcatheter aortic valve implantation
EOAI: Effective orifice area index TIA: Transiënte ischemische aanval
EPD: Elektronisch patiëntendossier Trifecta GT: Trifecta with Glide Technology
ESV: Edwards Sapien klep TSC: Totaal serum cholesterol
FEV1: Geforceerd expiratoir volume in 1 seconde
TVP: Tricuspiedklepherstel
FVC: Geforceerde vitale capaciteit VKA: Vitamine K-antagonisten
IQR: Interkwartielafstand VKF: Voorkamerfibrillatie
3. Inleiding
In deze experimentele studie bestuderen we de klinische en hemodynamische resultaten na implantatie van de Trifecta aortaklepprothese bij alle patiënten die tussen 1 januari 2012 en 31 december 2017 in het UZ Gent een Trifecta aortaklepprothese hebben ontvangen. Hierbij bestuderen we zowel de bestaande literatuur omtrent dit onderwerp en de resultaten van onze eigen experimentele studie. We vergelijken beide onderdelen met elkaar.
3.1 De aortaklep
3.1.1 Normale anatomie
De valva aortae bevindt zich tussen het linker ventrikel (LV) en de aorta (ascendens). Het is een tricuspiede klep, wat betekent dat ze bestaat uit drie klepbladen of valvulae semilunares die door hun structuur een holte of sinus aortae vormen. Een linker, rechter en non-coronair klepblad zijn te onderscheiden1, 2.
3.1.2 Relatie tot andere kleppen en structuren
De valva aortae ligt naast de valva trunci pulmonalis, valva mitralis en valva tricuspidalis vast geankerd in het fibreuze skelet van het hart. Dit fibreuze skelet is opgebouwd uit vier ringen die onderling verbonden zijn met elkaar (Figuur 1). In elke ring ligt telkens een hartklep. Aangezien de aorta zijn oorsprong dorsaal van de truncus pulmonalis kent, ligt de valva aortae ook dorsaal van de valva pulmonalis. De valva mitralis en valva tricuspidalis liggen respectievelijk
vastgeankerd in de annulus fibrosus sinister (links dorsaal van de aortaklep) en annulus fibrosus dexter (rechts dorsaal van de aortaklep). Tussen de valva aortae en valva mitralis bevindt zich enkel een fibreuze richel, deel van het fibreuze skelet. Tussen beide anuli fibrosi en tegen de valva aortae bevindt zich het geleidingsweefsel. De bundel van HIS en atrioventriculaire knoop (AV-knoop) liggen hier in het trigonum fibrosum dexter.
In de sinus aortae van het linker en rechter klepblad ontspringt respectievelijk de stam van de A. coronaria sinistra en A. coronaria dextra (Figuur 2). De linker coronair splitst nog in een ramus circumflexus (= Cx: Circumflex) en een ramus interventricularis anterior (= LAD: Left Anterior Descending)1, 2, 4.
Figuur 2: Aortaklep5
3.1.3 Werking
De aortaklep opent bij het samentrekken van het linker ventrikel (systole) en is gesloten bij het samentrekken van het linker atrium (diastole). Daartegenover staat dat de mitralisklep (tussen linker atrium en linker ventrikel) gesloten is bij de systole en open staat bij de diastole. Tijdens de systole trekt het myocard samen waardoor de druk in het met bloed gevulde linker ventrikel stijgt. De mitralisklep sluit hierdoor. Chordae tendineae en Mm. papillares verhinderen het doorslaan van de mitralisklep. Door de stijgende druk gaat de aortaklep wel open en wordt het O2-rijke
bloed in de aorta gestuwd. Bij de diastole daalt de druk in het linker ventrikel terug, waardoor het bloed in de aorta als het ware ‘terugvalt’. Bijgevolg gaan de drie sinus aortae zich vullen en sluit de aortaklep. In deze fase wordt het hart ook bevloeid met O2-rijk bloed via de oorsprong van de
coronairen in linker en rechter sinus aortae1.
De aortaklep is dus een belangrijke structuur om verschillende redenen. Ze zorgt ervoor dat het linker ventrikel zich kan vullen met geoxygeneerdbloed zonder dat bloed uit de aorta kan
terugstromen. Daarnaast laat de klep ook de toegang van het geoxygeneerdbloed naar de aorta toe. Door haar specifieke anatomische structuur ontstaan er 3 sinus aortae waarbij de linker en rechter belangrijk zijn voor de bevloeiing van het hart via de coronairen.
3.2 Aortakleppathologie en oorzaken
3.2.1 Aortaklepstenose
De aortakleppathologie met de hoogste incidentie in Europa is de aortaklepstenose (AoS). In het grootste deel van de gevallen is dit een chronische, progressieve aandoening. De stenose leidt tot een hogere afterload voor het linkerventrikel, waardoor het geleidelijk aan hypertrofie zal vertonen. Uiteindelijk zal dit resulteren in een ischemisch probleem waardoor er
linkerventrikeldysfunctie zal optreden (angor, aritmie, hartfalen)4, 6.
Stenose van de aortaklep kan door heel wat verschillende factoren worden uitgelokt. De
belangrijkste oorzaak van aortaklepstenose is degeneratieveverkalking. Calcificatie van de klep leidt tot een vernauwing van de effectieve klepopening, wat aanleiding geeft tot een
aortaklepstenose. Deze calcificatie ontwikkelt zich als antwoord op kleine beschadigingen aan de klep. Calcificatie wordt vaker en vroeger gezien bij patiënten met een congenitale bicuspiede klep. In de vorige eeuw was de rheumatische aortaklepstenose een groot probleem, maar tegenwoordig is de incidentie hiervan sterkgedaald. Bij rheumatische aortaklepstenose leidt de inflammatie ter hoogte van de klepblaadjes uiteindelijk tot verkalking en stenose. Andere
oorzaken van aortaklepstenose worden soms ook gezien in het kader van andere aandoeningen: patiënten met chronisch nierlijden hebben een hoger risico op aortaklepstenose, zeker indien ze hemodialyse ondergaan.Patiënten die bestraald zijn op de thorax, bij mammacarcinoom
bijvoorbeeld, of patiënten met de ziekte van Paget, hebben ook een hoger risico op aortaklepstenose4, 6.
3.2.1.1 Gecalcifiëerde aortaklepstenose
Zoals eerder aangehaald is dit de belangrijksteoorzaak. De incidentie neemt toe met de leeftijd, klassiek bij patiënten boven de 70 jaar. Risicofactoren voor deze oorzaak zijn gelijklopend met deze voor atherosclerose. Het betreft roken, diabetes, het mannelijk geslacht, hypertensie en verhoogde LDL- en LP(a)-waarden. Opvallend is het feit dat studies aantonen dat er geen regressie van de calcificatie optreedt indien deze factoren aangepakt worden. Men gaat er nu van uit dat eenmaal het proces van calcificatie in gang is gezet, dit autonoom verloopt4, 6.
3.2.1.2 Bicuspiede aortaklep
Deze congenitale hartafwijking kent een prevalentie van 1-2% en is soms familiaal. De
30-50 jaar. Deze afwijking kan geïsoleerd voorkomen, maar wordt ook gezien in het kader van een coarctatio aortae en een dilatatievan de aorta ascendens4, 6.
3.2.1.3 Rheumatische aortaklepstenose
De prevalentie van deze oorzaak is tot een minimum herleid in Europa. In andere delen van de wereld betreft dit echter wel nog een vrij significant deel van de oorzaken van aortaklepstenose. Heel vaak zal eerst de mitraalklep (MV) afwijkingen vertonen, gevolgd door de aortaklep4, 6.
Patiënten met stenose van de aortaklep kennen een asymptomatische periode waarin de
klepoppervlakte wel reduceert, maar dit geen symptomen met zich meebrengt. Uiteindelijk zal de stenose aanleiding geven tot klachten. Deze klachten doen zich het eerst voor bij inspanning en betreffen een gedaalde inspanningstolerantie, dyspneu, thoracale pijn tot syncope bij inspanning. Indien één van deze symptomen optreedt, moet er chirurgisch ingegrepen worden. Indien er niet ingegrepen wordt, volgt het overlijden binnen de 2 tot 3 jaar6.
3.2.2 Aortaklepinsufficiëntie
De prevalentie van een belangrijke aortaklepinsufficiëntie (AI) ligt vele malen lager dan die van een stenose. Deze insufficiëntie kan verschillende oorzaken hebben waaronder een geïsoleerde prolaps van één van de klepblaadjes, een perforatie, een dilatatie van de sinotubulaire junctie, een aneurysma van de aortawortel of een endocarditis4, 6.
3.3 Chirurgische behandeling
3.3.1 Chirurgische indicaties
Aangezien de onderzoeksvraag zich specificiek op het domein situeert van de
aortaklepprothesen, zullen we ons ook enkel richten tot de indicaties voor heelkunde voor aortakleppathologie. Er zijn duidelijke richtlijnen opgesteld die bepalen wanneer men moet overgegaan tot chirurgische interventie en wanneer niet7.
3.3.2 Chirurgische technieken
De standaardbehandeling bij een significante aortaklepstenose is de chirurgische plaatsing van een aortaklepprothese via een open techniek met extracorporele circulatie (ECC).
De laatste jaren zijn er nieuwe, minder invasieve technieken bijgekomen voor het plaatsen van een prothese. Zo zijn er nu prothesen die niet meer dienen vastgehecht te worden, de
zogenaamde ‘sutuurloze kleppen’ (Perceval, Intuity). Deze groep vereist ook minder grote incisies en een kortere klemtijd (XCL) dan de klassieke technieken, wat de postoperatieve morbiditeit ten goede komt4.
Een andere recente ontwikkeling is de TAVI (transcatheter aortic valve implantation). Deze klep wordt meestal ingebracht via de lies, maar dit kan ook suprasternaal of transapicaal. Een groot voordeel van deze techniek is dat men geen gebruik hoeft te maken van een extracorporele circulatie. Een groot nadeel is het feit dat ze heel duur zijn en er strikte restricties bestaan voor terugbetaling. De sutuurloze kleppen en de TAVI hebben beide ook een majeur nadeel, namelijk een hogere postoperatieve incidentie van een totaal atrioventriculair blok. Ondanks de
onmiskenbare voordelen van deze recentere technieken blijft de klassieke SAVR (surgical aortic valve replacement) de meest gebruikte in de medische wereld. De TAVI-techniek wordt echter steeds meer en meer gebruikt in de oudste populatie (80 jaar of meer)4.
Bij aortakleppathologie bij jonge patiënten of kinderen wordt soms de Ross-operatie aangewend. Hierbij wordt de aortaklep vervangen door de eigen pulmonalisklep en vervangt men deze laatste door een homograft4.
3.3.3 Types klepprothesen
Bij de mogelijke chirurgische interventies bij hartkleppathologie kunnen we 2 grote groepen onderscheiden. Enerzijds kan de oorspronkelijke klep vervangen worden door een prothese, zoals vaak uitgevoerd bij aortaklepstenose. Anderzijds kan de oorspronkelijke klep hersteld worden, dit gebeurt vaak bij mitraalkleppathologie of soms bij aortaklepinsufficiëntie. We zullen ons richten op de behandeling door klepvervangingmet de verschillende soorten klepprothesen, aangezien de onderzoeksvraag in dit gebied kadert4.
Er zijn twee grote groepen klepprothesen, namelijk de mechanische en de biologische klepprothesen.
3.3.3.1 Mechanische klepprothesen
De mechanische klepprothesen zijn opgebouwd uit pyrolietcarbon, een heel duurzaam materiaal, waardoor ze de voorkeur krijgen bij jongere personen. De hemodynamiek van deze kleppen is ook gunstig. Het grote nadeel van deze groep is het feit dat de patiënten levenslang vitamine K-antagonisten (VKA) dienen in te nemen. Hierdoor kunnen bij deze patiënten bloedingen, kleptromboses en trombo-embolische fenomenen optreden. Het gebruik van nieuwe orale
anticoagulantia (NOAC) is bij deze soort kleppen niet toegelaten. Vroeger maakten deze kleppen ook veel geluid, maar door de nieuwe technieken is dit duidelijk verminderd4.
3.3.3.2 Biologische klepprothesen
Deze groep van kleppen zijn hetzij van dierlijke (xenografts), hetzij van humane oorsprong (homografts). Ze zijn in tegenstelling tot de mechanische minder aangewezen bij jonge patiënten aangezien ze sneller verkalken, waardoor er nood is aan klepvervanging na een tiental jaar. Hoe ouder de patiënt, hoe minder degeneratie optreedt bij deze kleppen. Het grote voordeel ten opzichte van de mechanische kleppen is het feit dat, indien de patiënt sinusaal is, men na de operatie enkel aspirine dient in te nemen. Deze klepprotheseis bovendien geruisloos. De biologische klepprothesen wordenals ideaal beschouwd voor patiënten boven de 70 jaar. De leeftijdsgroep die zich daar net onder bevindt (60 tot 70 jaar), blijft een discussiegebied. Men moet hierbij in overleg met de arts en de patiënt het risico op heroperatie afwegen tegenover het risico op bloedingen, kleptromboses en trombo-embolische fenomenen4.
Homografts zijn humane kleppen die vooral gebruikt worden bij kinderen met congenitale aandoeningen. In de volwassen populatie worden deze veel minder aangewend. Bij deze homografts wordt vaakook een deel van het aansluitende bloedvat bewaard, bijvoorbeeld een deel van de aorta ascendens bij een aortaklep. Een homograft kan nog altijd verkalken, maar heeft hiertoe iets minder neiging dan de xenografts4.
De laatste jaren is er een duidelijke tendens te zien, waarbij er steeds meer biologische kleppen geplaatst worden. Dit gegeven is wel onlosmakelijk verbonden met de vergrijzing van de
Westerse bevolking4.
3.3.4 Resultaten van aortaklepvervanging
De algemene resultaten voor aortaklepvervangingen (AVR) verschillen naargelang de leeftijd waarop de vervanging gebeurt en van het type prothese dat ingeplant werd. De studie van Glaser et al. concentreerde zich op de leeftijdsgroep van 50-69 jaar. Gedurende de follow-up in deze studie was er in de groep van de mechanische prothesen een mortaliteit van 16% ten opzichte van 20% bij de biologische. De gemiddelde duur van de follow-up betrof hierbij 6,6 jaar, met een
maximum van 17,2 jaar. De overleving was eveneens gunstiger bij de groep van mechanische prothesen. De 5-, 10- en 15-jaars overleving bedroegen respectievelijk 92, 79 en 59% voor de mechanische groep. Voor de biologische prothesen bedroegen die respectievelijk 89, 75 en 50%. De incidentie van neurologische complicaties is vergelijkbaar tussen beide types. Het risico op heroperatie is hoger en het risico op een majeure bloeding lager bij de biologische prothesen8.
Du et al. concentreerden zich meer op de leeftijdscategorie van 65 jaar of ouder, waarbij de gemiddelde leeftijd 76 jaar bedroeg voor de groep van de mechanische prothesen en 77 jaar voor de groep van de biologische. Het risico om te sterven op de dag van de operatie was 60% hoger in de groep van de mechanische prothesen dan van de biologische. In de eerste 30 dagen na de operatiedatum bedroeg het risicoverschil op sterfte 16%, nog altijd in het nadeel van de groep van de mechanische prothesen. Deze verschillen in mortaliteit werden vooral
waargenomen in de groep van de hoog-risico patiënten die eveneens een geassocieerde CABG-procedure (coronary artery bypass grafting) ondergingen. In de patiëntengroep met een geïsoleerde AVR was het risico op vroegtijdige mortaliteit vergelijkbaar tussen de biologische en mechanische prothesen. Er waren echter geen significante verschillen in het risico op sterfte tussen beide groepen binnen de 30 dagen na ontslag en in de periode vanaf 31 dagen tot en met 1 jaar na de operatie9.
Langanay et al. die zich specifiek richtten op patiënten van 80 jaar of ouder, kwamen tot de volgende overlevingscijfers na een aortaklepvervanging: 83%, 62,5% en 25% na respectievelijk 2, 5 en 10 jaar. Er werd hierbij geen onderscheid gemaakt tussen de implantatie van een mechanische of biologische prothese10.
3.4 Trifecta prothese
Onze onderzoeksvraag richt zich specifiek op de klinische en hemodynamische resultaten van de Trifecta aortaklepprothese. Deze prothese behoort tot de biologische klepprothesen en is
samengesteld uit 3 klepblaadjes. Deze prothese is ontworpen voor een supra-annulaire
aanhechting in de aorta. De klep is opgebouwd uit een titanium stent, bedekt met polyester. De stent zelf, exclusief de hechtingsplaats, is bedekt met varkenspericard (xenograft). De 3
klepblaadjes zijn vervaardigd uit rundspericard. Zowel het varkens- als rundspericard zijn bewaard en gecrosslinked in glutaraldehyde. De prothese is beschermd tegen calcificatie door een ethanol-gebaseerde technologie. De beschikbare groottes van de prothese gaan van 19 tot 29 mm, telkens met een diameterinterval van 2 mm11.
De Trifecta klep heeft enkele specifieke eigenschappen in de hoop om enkele fundamentele problemen van oudere biologische aortaklepprothesen op te lossen. Zo moet de concave hechtingsring zorgen voor een adequate vulling van de coronairen. De klepblaadjes uit
rundspericard zijn gemonteerd op de buitenzijde van de titanium stent, en laten zo een maximale cylindrische opening toe gedurende de systole. Deze eigenschap zorgt voor lagere gradiënten en hogere EOA’s (effective orifice area) dan elke andere biologische, gestente aortaklepprothese die beschikbaar was in 2014. Deze resultaten zijn vergelijkbaar met deze van de stentloze
prothesen. Bovendien beschikt de titanium stent nog over een intrinsieke distensibiliteit die een verdere expansie van de prothese mogelijk maakt in situaties met een hogere belasting, bijvoorbeeld bij inspanning. Studies tonen aan dat deze prothese, in vergelijkbare patiëntengroepen, betere hemodynamische resultaten oplevert dan de Sorin Mitroflow
pericardiale aortaprothese, de Medtronic Mosaic porciene aortaprothese en de Edwards Magna Ease. Deze gunstige hemodynamische resultaten weerspiegelen zich ook in een extreem lage incidentie van ernstige PPM (patient-prosthesis mismatch)11.
In de literatuur wijst men op twee belangrijke aandachtspunten bij de implantatie van de Trifecta aortaklepprothese. Het eerste betreft de uitvoering van zowel een hoge als wijde aortotomie, vanwege het hoge profiel van de prothese. De wijde aortotomie is noodzakelijk om de moeilijkheden die gepaard gaan met de hoge aortotomie te compenseren. Het tweede
aandachtspunt betreft het correct schatten van de klepmaat van de in te planten prothese. Een te grote klepmaat bemoeilijkt de implantatie, voornamelijk bij het plaatsen van de prothese in het valvulaire vlak en bij het knopen. Verder leidt een te grote klepmaat tot een toename van de gradiënten wegens een te grote hoeveelheid klepweefsel in de annulus aortae12.
Gedurende meerdere jaren bij de implantatie van de eerste generatie van de Trifecta
aortaklepprothesen maakten verschillende instituten melding van het scheuren van de klep. Dit treedt zelfs op bij patiënten die bij implantatie geen comorbiditeiten vertonen en ook geen postoperatieve complicaties ervaren13.
Om de oorzaak van het scheuren van de klep te vinden, ging men kijken bij de chirurgische implantatie. De chirurg moet bij het plaatsen van de prothese zeer aandachtig zijn om, bij het leggen van knopen, de vrije boord van de klepblaadjes aan de stent niet te beschadigen. Vervorming van de stent kan ook optreden wanneer de prothese eigenlijk iets te groot is. Een vervorming van de stent kan leiden tot verhoogde mechanische stress met bijgevolg een verhoogd risico op scheuren13.
Om deze mogelijke problemen bij het plaatsen van de klep te vermijden, heeft de producent (St. Jude Medical) een nieuwe, tweede generatie aortaklepprothesen in april 2016 op de markt gebracht, de ‘Trifecta with Glide Technology’ (Trifecta GT) (Figuur 3). Het design is aangepast waardoor ze minder gevoelig is voor procedurefouten bij implantatie. De Trifecta GT heeft een nieuwe houder, wat ervoor zorgt dat de klepblaadjes beter beschermd liggen bij implantatie. Een extra titanium band is aanwezig in de stent, wat vervorming tegengaat. Stress ter hoogte van de hechtingsplaatsen op de klepblaadjes wordt door het specifieke design ook verminderd.
Daarnaast heeft men de klepblaadjes bewerkt met een bijzondere collageenvezeltechnologie, die versnelde degeneratie van de klepblaadjes zou tegengaan13.
Sinds het gebruik van de Trifecta GT heeft men bij deze specifieke klep nog geen postoperatieve problemen gehad, wat erop kan wijzen dat de designaanpassingen wel degelijk hun nut
4. Doel van de studie
‘Wat zijn de klinische en hemodynamische resultaten na implantatie van de Trifecta aortaklepprothese?’ is de onderzoeksvraag van deze studie. Dit wordt onderzocht in een retrospectieve klinische studie bij alle patiënten bij wie van 01/01/2012 tot en met 31/12/2017 in het UZ Gent een Trifecta aortaklepprothese werd ingeplant. Concreet wordt gebruik gemaakt van een database waarin zowel het risicoprofiel, als de patiëntenkarakteristieken, als de klinische en echocardiografische gegevens van iedere patiënt aanwezig zijn van bij de implantatie tot bij de laatste follow-up. De resultaten van deze database-analyse zullen eveneens worden afgetoetst aan de reeds bestaande literatuur over dit onderwerp.
5. Methode
5.1 Zoekstrategie
De studie begon met een korte literatuurstudie, enerzijds om onszelf een beter inzicht in de onderzoeksvraag te geven en anderzijds om onze inleiding op te bouwen. Voor het vinden van geschikte artikels voor de literatuurstudie werd gebruik gemaakt van de database PubMed. We maakten eerst enkel gebruik van ‘free-text’, namelijk ‘Trifecta aortic valve’. Met deze zoektermen bekwam men in PubMed 84 artikels. Dit was reeds een vrij beperkte selectie waardoor het mogelijk was deze artikels te overlopen via de titel en abstract om de meest relevante te
selecteren. Daarnaast werdenvia een combinatie met de Booleaanse operator ‘AND’, de MeSH-zoekterm ‘Aortic valve’ en de free-text ‘Trifecta’ 56 artikels gevonden. Dit betrof nog een verdere verenging van de oorspronkelijke 84 artikels waaruit we reeds artikels hadden geselecteerd. Eén artikel werd door de promotor aangebracht. Andere artikels werden via de referentielijst hiervan geselecteerd. Eveneens werden er artikels gevonden bij ‘Similar Articles’ bij dit
aangebrachte artikel. Enkele artikels over het onderwerp ‘TAVI’, één artikel met betrekking tot de risicofactoren en twee artikels over pacemakerimplantaties, werden gevonden via ‘free-text’. Naast het gebruik van PubMed, was de Sobotta anatomieatlas een belangrijke bron van
informatie. De lessen en het lesmateriaal van Prof. dr. François, Prof. dr. D’Herde en Prof. dr. De Pauw bevatten eveneens belangrijke informatie voor onze literatuurstudie.
5.2 Methode en patiënten
Om een aortaklep of een aortaklepprothese te bestuderen, heeft men een aantal parameters gedefinieerd in verschillende studies. Een aantal van deze parameters werden weerhouden en aangevuld met andere na overleg met de promotor.
De database is opgebouwd uit de parameters en gegevens van patiënten die worden bekomen uit het Elektronisch patiëntendossier (EPD). Het is een retrospectieve studie die zich specifiek richt op de klinische en hemodynamische resultaten na de implantatie van een Trifecta
aortaklepprothese. De patiëntenpopulatie bestaat uit patiënten die deze biologische
aortaklepprothese kregen ingeplant tussen 1 januari 2012 en 31 december 2017 in het UZ Gent, geïsoleerd of als onderdeel van een gecombineerde ingreep. In Figuur 4 ziet u het
Figuur 4: Stroomdiagram
5.3 Database
Vooraleer gestart kon worden aan het experimenteel onderzoek en het opstellen van de database op basis van het EPD, was hiervoor toestemming van het Ethisch Comité vereist. De aanvraag werd geplaatst op 27/06/2018 en toestemming werd vervolgens door het Ethisch Comité verleend op 10/07/2018 met Belgische registratienummers B670201836876 (voor Alexander Dereu) en B670201838877 (voor Augustijn Mortelé). Na goedkeuring werd de database opgesteld in een Exceldocument. Er werden hierin enkel patiënten opgenomen die in de bovengenoemde periode een Trifecta aortaklepprothese geïmplanteerd kregen. De lijst van deze patiënten werd verkregen via depromotor, Prof. dr. K. François. Aangezien we een louter retrospectieve studie uitvoeren werd geïnformeerde toestemming bij de patiënten door het
Ethisch Comité van het UZ Gent niet nodig geacht. In het EPD werden vervolgens de parameters gezocht. Deze werden bekomen uit patiëntgerelateerde documenten (operatieverslag, opname- en ontslagbrief, follow-up,…). Uit het EPD genereerden we verslagen die opgesteld werden door zowel artsen verbonden aan het UZ Gent als door artsen verbonden aan perifere ziekenhuizen (vooral de follow-up). Deze laatste verslagen waren vaak beschikbaar via het Collaboratief Zorgplatform (CoZo) dat in het EPD is geïntegreerd. De specifieke gegevens uit het EPD en CoZo werden door Prof. dr. K. François aan ons ter beschikking gesteld.
De opgenomen parameters zijn terug te vinden in Tabel 1 in het Addendum. Een aantal
parameters zijn gelinkt aan bepaalde richtlijnen. Een patiënt dient te voldoen aan die richtlijnen om die parameter als positief te documenteren. Deze richtlijnen worden eveneens in het Addendum opgelijst. Mechanische aortaklepprothese n = 272 Biologische aortaklepprothese n = 653 Trifecta prothese n = 182 Geen Trifecta prothese
n = 470
Aortaklepprothese 2012-2017 (bij volwassenen)
5.4 Statistische analyse
De statistische analyse van de database werd uitgevoerd in IBM SPSS Statistics 25. Een
onderscheid tussen categorische en continue variabelen werd gemaakt. Categorische variabelen zijn uitgedrukt in absolute aantallen en percentages. Normaal verdeelde continue variabelen worden weergegeven als gemiddelde met standaarddeviatie (SD), niet-normaal verdeelde continue variabelen als mediaan en interkwartielafstand (IQR). Veel variabelen werden via het centrale limiet theorema beschouwd als normaal verdeeld. De gradiënten over de aortaklep waren niet normaal verdeeld op elk tijdstip van de follow-up, maar worden toch weergegeven als gemiddelde met SD, aangezien dit toelaat een vergelijking te maken met andere studies. De gemiddelden benaderden hierbij bovendien heel dicht de medianen. Enkel non-parametrische testen werden op de data uitgevoerd aangezien er veel categorische variabelen waren, er een aantal variabelen niet normaal verdeeld waren en bij sommige nulhypothesen de patiëntengroep drastisch verkleind was. Categorische variabelen werden vergeleken via kruistabellen waarop telkens een 𝜒2-test werd uitgevoerd. Indien er van de verwachte frequenties meer dan 20%
kleiner was dan 5 en/of er een verwachte frequentie kleiner was dan 1, was de 𝜒2-test niet geldig
en werd gekeken naar de Fisher’s Exact test. Om continue variabelen tussen groepen te vergelijken, werden de Mann-Whitney U, de Kruskal-Wallis en de Friedman test gebruikt. Vermits er in deze studie pre-operatieve parameters tot en met postoperatieve parameters op 6 jaar onderzocht werden, was het mogelijk om Kaplan Meier overlevingscurves op te stellen. Een algemene Kaplan Meier overlevingscurve werd opgesteld, alsook overlevingscurves die
verschillende groepen vergelijken. Het tijdsverloop werd telkens uitgedrukt in maanden. Om significantie te testen op de Kaplan Meiercurves, werd telkens de Log Rank (Mantel Cox)- en Breslow (Wilcoxon)-test uitgevoerd.
Om te bepalen of een test significant was en de nulhypothese kon worden verworpen, moest er een p-waarde van kleiner dan 0,05 bereikt worden. Hierbij werd telkens gekeken naar de
tweezijdige p-waarde. Bij de Kaplan Meier overlevingcurves is significantie slechts geldig tot het ogenblik dat minder dan 10% van de totale populatie (het aantal patiënten op 0 maanden, bij operatie) nog in de curve kan worden betrokken. De laatst mogelijke datum waarop follow-up geregistreerd kon worden, werd vastgelegd op 30 juni 2019. Logischerwijs hebben niet alle patiënten op elk tijdstip follow-up en is dit afhankelijk van hun operatiedatum.
6. Resultaten
6.1 Klinische resultaten
6.1.1 Patiëntenkarakteristieken en peroperatieve gegevens
Tijdens de studieperiode werden er in totaal 182 Trifecta prothesen geïmplanteerd. Het aantal patiëntenjaren follow-up was 475. De gemiddelde duur van de follow-up bedroeg 36 maanden en de volledigheid van de follow-up 88%. De antropometrische parameters van de studiepopulatie kunnen teruggevonden worden in Tabel 1. Het grootste gedeelte van de patiënten was ouder dan 70 jaar op het moment van de operatie (n = 165). Er was geen enkele patiënt jonger dan 60 jaar. Deze leeftijdsverdeling is terug te vinden in Figuur 5.
Tabel 1. Antropometrische parameters
Variabele (n (%)) Studie populatie
(n = 182) Geslacht Man Vrouw 82 (45,1%) 100 (54,9%) Variabele (Gemiddelde ± SD) Studie populatie (n = 182)
Leeftijd bij operatie (jaren) 77 ± 5,5
Gewicht (kg) 75 ± 13
Lengte (cm) 165 ± 9
BSA (m2) 1,8 ± 0,2
Figuur 5. Leeftijdsgroepen bij operatie
De comorbiditeiten zijn weergegeven in Tabel 2. Arteriële hypertensie (AHT) gevolgd door hypercholesterolemie waren de comorbiditeiten met de hoogste prevalentie. De antihypertensiva en cholesterolremmers waren eveneens de meest frequent gebruikte medicatie pre-operatief (Tabel 3). Bij 9.3% van de patiënten werd vroeger reeds een cardiale operatie uitgevoerd. De meerderheid van de patiënten (79%) was pre-operatief in sinusritme. Urgente operatie (= tijdens dezelfde kliniekopname) was nodig in 11% van de gevallen. In Tabel 4 staan de gegevens met betrekking tot de cardiale status op het moment van de operatie. Hieruit blijkt dat de belangrijkste indicatie tot het overgaan naar chirurgie een aortaklepstenose was. Verder isook het hoge aantal patiënten die zich bevonden in NYHA-klasse (New York Heart Association) III of IV (38%)
17 107 58 0 20 40 60 80 100 120 60-70 70-80 > 80 Aa nt al p at ië nt en Leeftijdsgroep (jaren)
Tabel 2. Comorbiditeiten
Variabele (n (%)) Studie populatie (n = 182)
Arteriële hypertensie 138 (75,8%) Hypercholesterolemie 118 (64,8%) Diabetes Mellitus Roken 46 (25,3%) 15 (8,2%)
Gestopt met roken 53 (29,1%)
Perifeer vaatlijden 65 (35,7%)
Chronisch nierfalen (creatinine > 200) 15 (8,2%)
COPD 24 (13,2%)
Voorafgaand CVA/TIA 24 (13,2%)
Voorafgaand AMI 25 (13,7%)
Tabel 3. Pre-operatieve medicatie
Variabele n (%) Studie populatie (n = 171)
Antihypertensiva 99 (57,9%) Betablokkers 79 (46,2%) Cholesterolremmers 113 (66,1%) Diuretica 74 (43,3%) Anticoagulantia (VKA/NOAC/heparine) 45 (26,3%) Anti-aggregantia (aspirine/clopidogrel) 96 (56,1%)
Tabel 4. Cardiale status
Variabele (n (%)) Studie populatie
(n = 182) Missing values Voorafgaand cardiochirurgie CABG AVR MVR TVP ASD 17 (9,3%) 9 (4,9%) 8 (4,4%) 1 (0,5%) 1 (0,5%) 1 (0,5%) 0
Pre-operatief cardiaal ritme Sinusaal VKF Pacemaker 143 (79%) 32 (17,7%) 6 (3,3%) 1 Electieve operatie 162 (89%) 0 Urgente operatie 20 (11%) 0 NYHA-klasse I II III IV 22 (12,1%) 91 (50%) 50 (27,5%) 19 (10,4%) 0 EUROscore II 5,7 ± 9,8 0
Indicatie voor operatie AoS AI Kunstklependocarditis 174 (95,6%) 7 (3,8%) 1 (0,6%) 0
Figuur 6. Geïmplanteerde klepmaat
Tabel 5. Chirurgische parameters
Variabele Studie
populatie (n = 182)
Gemiddelde ± SD (min)
Extracorporele circulatie (min) Alle patiënten
Met geassocieerde procedure Geïsoleerd 182 108 74 108 ± 40 125 ± 39 83 ± 24 Klemtijd (min) Alle patiënten
Met geassocieerde procedure Geïsoleerd 182 108 74 76 ± 28 87 ± 29 60 ± 17 Studie populatie (n = 182) % Geassocieerde procedures CABG TVP MVP MVR Aorta ascendensvervanging Aorta wortelverbredingsplastie Aorta wortelreconstructie Bentallprocedure MAZE PFO sluiten
Exclusie linker hartoortje Septale myectomie 108 72 17 24 9 5 6 4 1 6 1 6 3 59,34% 39,6% 9,3% 13,2% 4,9% 2,7% 3,3% 2,2% 0,5% 3,3% 0,5% 3,3% 1,6%
6.1.2 Mortaliteit en complicaties
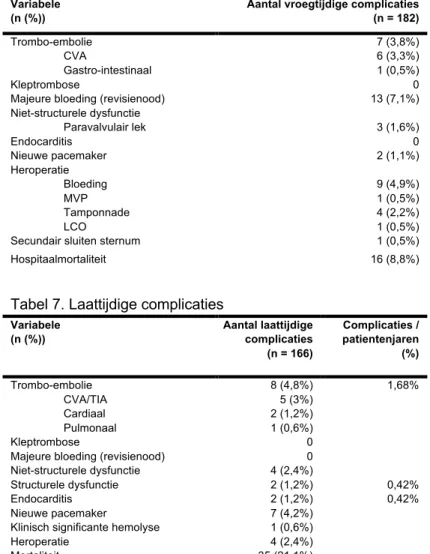
De complicaties zijn onderverdeeld in vroegtijdige (binnen de 30 dagen postoperatief) (Tabel 6) en laattijdige complicaties (Tabel 7). De hospitaalmortaliteit bedroeg 8,8% (16 patiënten), dit verklaart het verschil in de populatiegrootte tussen de vroegtijdige (n = 182) en laattijdige (n = 166)
complicaties. 11 55 73 36 7 0 0 10 20 30 40 50 60 70 80 19 21 23 25 27 29 Aa nt al p at ië nt en Klepmaat (mm)
De trombo-embolische accidenten waren in beide groepen voornamelijk centraal neurologisch. Postoperatieve bloeding met noodzaak tot revisie was de meest genoteerde vroegtijdige
complicatie (7,1%). Niet-structurele dysfunctie kwam vroeg- en laattijdig respectievelijk drie en vier keer voor. Vroegtijdig waren dit uitsluitend kleine paravalvulaire lekken. Laattijdig kwam een paravalvulair lek slechts éénmaal voor. De overige oorzaken van niet-structurele dysfunctie waren een Dressler syndroom, een valvulaire cardiomyopathie en hartfalen. Een klinisch significante hemolyse kwam éénmaal voor als laattijdige complicatie. De desbetreffende patiënt had concomitant met de Trifecta een TVP ondergaan en de hemolyse was gelinkt aan een paravalvulair lek ter hoogte van deze tricuspiedklep. In totaal werden 4 patiënten laattijdig geheropereerd, waarbij structurele dysfunctie de oorzaak was bij twee patiënten. De overige heroperaties waren enerzijds vanwege een endocarditis en anderzijds vanwege een belangrijke aortaklepinsufficiëntie door een paravalvulair lek. In totaal kregen 9 patiënten, waarvan twee vroegtijdig, na de operatie nog een pacemaker geïmplanteerd. De specifieke klepgerelateerde complicaties worden verder besproken in het hoofdstuk ‘6.2.2 Specifieke klepcomplicaties’.
Tabel 6. Vroegtijdige complicaties Variabele
(n (%))
Aantal vroegtijdige complicaties (n = 182) Trombo-embolie CVA Gastro-intestinaal 7 (3,8%) 6 (3,3%) 1 (0,5%) Kleptrombose 0
Majeure bloeding (revisienood) 13 (7,1%) Niet-structurele dysfunctie Paravalvulair lek 3 (1,6%) Endocarditis Nieuwe pacemaker 0 2 (1,1%) Heroperatie Bloeding MVP Tamponnade LCO 9 (4,9%) 1 (0,5%) 4 (2,2%) 1 (0,5%)
Secundair sluiten sternum 1 (0,5%)
Hospitaalmortaliteit 16 (8,8%)
Tabel 7. Laattijdige complicaties Variabele (n (%)) Aantal laattijdige complicaties (n = 166) Complicaties / patientenjaren (%) Trombo-embolie CVA/TIA Cardiaal Pulmonaal 8 (4,8%) 5 (3%) 2 (1,2%) 1 (0,6%) 1,68% Kleptrombose 0
Majeure bloeding (revisienood) 0 Niet-structurele dysfunctie 4 (2,4%)
De oorzaken van de laattijdige mortaliteit waren vaak onbekend, waardoor een verdere opsplitsing hier niet kan toegepast worden. Tabel 8 geeft weer indien er een significante associatie bestaat tussen de laat- en vroegtijdige complicaties, hospitaalmortaliteit, laattijdige mortaliteit en verschillende parameters.
Tabel 8. Associaties met complicaties en mortaliteit Univariabele p-waarde Multivariabele p-waarde Odds ratio (95% BI) Univariabele p-waarde Multivariabele p-waarde Odds ratio (95% BI)
Variabele Vroegtijdige complicaties Hospitaalmortaliteit
Voorafgaande cardiochirurgie 0,007 2,5 (0,3 - 22) 0,001
Urgentie van de operatie 0 4,2 (0,7 - 24,1) 0 0,099 34,1 (0,5 -2262,4)
EUROscore 0,005 0,002 4,1 (0 - 390,4)
Pre-operatieve LV-functie 0,062 0,069 5,2 (0,1 - 285)
Postoperatieve LV-functie 0,048 0,013 0,039 0,01 (0 - 0,8)
Pre-operatieve NYHA-klasse* 0 0,008 16,6 (0
-1078995,7)
Pre-operatief cardiaal ritme** 0,018 0,008 9,4 (0,2 - 390,6)
Geassocieerde TVP 0,047 16,1 (0,4 - 655,6) Geassocieerde MVR 0,016 2,4 (0,3 - 20,7) 0,034 Chronisch nierfalen 0,003 2,7 (0,5 - 16) 0,030 COPD 0,028 0,042 Diabetes mellitus 2,6 (0,8 - 8,2) 0,240 0,094 15,3 (0,6 - 371,2) Voorafgaand AMI 0,023 0,032 4,4 (1,1 - 16,8) 0,036
Variabele Laattijdige complicaties Laattijdige mortaliteit
Urgentie van de operatie 0,004 0,039 6,5 (1,1 - 39,1)
Pre-operatieve LV-functie 4,1 (0,3 - 60,9) 0,005
Pre-operatieve NYHA-klasse* 0,057
Pre-operatief cardiaal ritme** 0,022 4,3 (0,6 - 29,1) 0,002 0,014 4,8 (1,4 - 16,8)
Geassocieerde CABG 0,079 0,055 AHT 0,040 0,049 3,7 (1 - 13,6) Perifeer vaatlijden 0,078 0,034 Chronisch nierfalen 0,075 2,2 (0,2 - 22,6) 0,012 COPD 0,091 0,027 7,1 (1,3 - 40,4) 2,1 (0,5 - 8,5) Diabetes mellitus 0,026 0,088 3,8 (0,8 - 17,8)
*NYHA-klassen in deze test opgedeeld volgens 3 categorieën bij vroegtijdige complicaties en laattijdige mortaliteit: I/II, III en IV. Volgens 2 categorieën bij laattijdige complicaties en hospitaalmortaliteit: I/II en III/IV
De hospitaalmortaliteit wordt gezien als een vroegtijdige complicatie. De oorzaak van de laattijdige mortaliteit was daarentegen immers vaak onbekend en zou leiden tot een
overschatting van de laattijdige complicaties. De relatie tussen de EUROscore en de laattijdige complicaties en mortaliteit is niet relevant, aangezien deze parameter een maat is voor het operatieve risico, en wordt daarom ook niet vermeld.
De resultaten van de univariabele analyse van de risicofactoren zijn in tabel 8 terug te vinden. Een urgente operatie of de aanwezigheid van chronisch nierfalen was significant geassocieerd met vroegtijdige complicaties, hospitaalmortaliteit en laattijdige mortaliteit. Chronisch obstructief longlijden (COPD), een voorafgaand acuut myocardinfarct (AMI) of een slechte linker
ventrikelfunctie postoperatief waren enkel significant geassocieerd met vroegtijdige complicaties en hospitaalmortaliteit. Daarentegen verhoogde een slechte pre-operatieve LV-functie alleen het risico op laattijdige mortaliteit. De relatie met de vroegtijdige complicaties en de
hospitaalmortaliteit was nipt niet significant. De relatie tussen het voorkomen van voorkamerfibrillatie (VKF) pre-operatief was significant verbonden met het optreden van
complicaties en zowel laattijdige als hospitaalmortaliteit. Dit was de enige parameter die alle vier de uitkomsten significant beïnvloedde.
Er werd eveneens een meervoudige logistische regressie uitgevoerd (Tabel 8). Hieruit bleek dat enkel een voorafgaand AMI geassocieerd was met vroegtijdige complicaties, en eveneens enkel de postoperatieve LV-functie met vroegtijdige mortaliteit. Alleen de comorbiditeit COPD
verhoogde significant het risico op laattijdige complicaties. Na deze multivariabele analyse was de laattijdige mortaliteit nog altijd met drie factoren significant geassocieerd, namelijk met de urgentie van de operatie, de aanwezigheid van VKF en arteriële hypertensie. Enkele niet-significante variabelen vertoonden wel hoge odds ratio’s.
6.1.3 Overleving
Een eerste overzicht van de algemene overleving wordt weergegeven op de Kaplan Meiercurve in Figuur 7. Tussen 0 en 20 maanden vonden de meeste dodelijke events plaats, namelijk 37 met slechts 3 patiënten die buiten de follow-up vielen. In de volgende tijdsintervallen werden minder dodelijke events geregistreerd, maar waren er van veel meer patiënten slechts beperkte follow-up gegevens beschikbaar. De overlevingscijfers na 1 en 5 jaar bedroegen respectievelijk 85% en 70%.Op 70 maanden werd minder dan 10% van de totale populatie nog in de curve opgenomen, waardoor de resultaten vanaf dit moment niet meer als relevant te beschouwen waren.
Wanneer een Kaplan Meiercurve werd opgesteld volgens geslacht, werd er geen significant verschil in overleving gevonden. Een vergelijking tussen de verschillende klepmaten gaf
eveneens geen significant overlevingsverschil. Figuur 8 toont de overleving in de tijd per NYHA-klasse (pre-operatief). Een pre-operatieve NYHA-NYHA-klasse IV gaf een significant verschil in
overleving ten opzichte van zowel NYHA-klasse I (p-waarde = 0,012), II (p-waarde = 0,001) als III (p-waarde = 0,032). Tussen NYHA-klasse I, II en III was er onderling geen significant verschil. Wanneer de populatie werd onderverdeeld volgens de pre-operatieve linkerventrikelfunctie (Figuur 9), waren de overlevingscijfers significant beter in de groep met een normale
linkerventrikelfunctie (p-waarde = 0,001).De overlevingscijfers waren eveneens beter bij de patiënten die pre-operatief een sinusaal ritme vertoonden (Figuur 10) ten opzichte van de patiënten die een VKF (p-waarde = 0) of een pacemaker (p-waarde = 0,40) hadden.
.
*Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 7. Kaplan Meier overlevingscurve totale populatie
*p-waarde volgens Log Rank-test. Specifieke p-waarden tussen NYHA-klassen onderling: zie volgende alinea.
**Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 8. Kaplan Meier volgens pre-operatieve NYHA-klasse. Maanden Ov er le v in g * ** Maanden Ov er le v in g p-waarde = 0,001*
De Kaplan Meiercurve volgens de leeftijd bij operatie met een cut-off van 75 jaar gaf een
significant verschil, met een gedaalde overleving voor patiënten ouder dan 75 jaar met p-waarde = 0,011 (Figuur 11). In de eerste twee jaren follow-up was dit verschil reeds duidelijk, wat
gerelateerd kan zijn aan een slechtere operatieve uitkomst van de oudste groep. Nadien zette dit verschil zich voort door de natuurlijke evolutie in mortaliteit. Een geassocieerde procedure bleek de overleving niet significant te beïnvloeden. De Breslow-test vertoonde hierbij echter wel een lagere p-waarde (0,066) dan de Log Rank-test (0,115) (Figuur 12).
. *Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 9. Kaplan Meier volgens pre-operatieve LV-functie.
*Algemene p-waarde.
**Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 10. Kaplan Meier volgens pre-operatief cardiaal ritme.
*p-waarde volgens Log Rank-test.
**Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 11. Kaplan Meier volgens leeftijd bij
*p-waarde volgens Breslow-test. Volgens Log Rank: p-waarde = 0,115.
**Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden. Maanden Ov er le v in g ** p-waarde = 0,011* Maanden Ov er le v in g ** p-waarde = 0,066* Maanden Ov er le v in g p-waarde = 0,001 * ** Maanden Ov er le v in g p-waarde = 0*
6.2 Klepspecifieke resultaten
6.2.1 Hemodynamische resultaten
6.2.1.1 De klepgradiënten
De gradiënten over de klep gedurende de follow-up zijn weergegeven in Figuur 13 en Tabel 9. Er was een significant verschil tussen de gemiddelde en de piekgradiënten pre-operatief en postoperatief (p-waarde = 0). Dit was echter niet het geval tussen de verschillende
piekgradiënten postoperatief (p-waarde = 0,423). De gegevens gedurende de latere follow-up dienen wel genuanceerd te worden vanwege het hoge aantal missing values en de kleinere populatie.
Figuur 13. Gemiddelde gradiënten gedurende follow-up
Tabel 9. Pre- en postoperatieve echoparameters: algemeen
Variabele Pre-operatief (n = 182) Bij ontslag (n = 169) 3m (n = 166) 6m (n = 162) 1j (n = 158) 18m (n = 151) 2j (n = 135) 3j (n = 106) 4j (n = 82) 5j (n = 49) 6j (n = 15) Piekgradiënt Missing values (%) Gemiddelde gradiënt Missing values (%) 68 ± 26 0,5% 42 ± 17 18,7% 15 ± 6 0,6% 8 ± 3 13% 13 ± 5 73,5% 8 ± 3 83,7% 16 ± 7 68,5% 9 ± 7 80,9% 17 ± 8 53,2% 9 ± 7 74% 18 ± 8 68,2% 11 ± 7 84,1% 18 ± 10 48,9% 11 ± 6 68,9% 19 ± 9 40,6% 11 ± 5 58,5% 19 ± 9 48,8% 11 ± 5 62,2% 21 ± 14 36,7% 14 ± 10 59,2% 25 ± 29 53,3% 21 ± 31 80%
Continue variabelen zijn weergeven als gemiddelde ± SD. Gemiddelde gradiënt en piekgradiënt zijn weergeven in mmHg.
68* 15* 13 16 17 18 18 19 19 21 25 42* 8* 8 9 9 11 11 11 11 14 21 0 10 20 30 40 50 60 70 80 Pre-op eratie f Bij on tslag 3m 6m 1j 18m 2j 3j 4j 5j 6j Ge m id de ld e gr ad ië nt (m m Hg ) Tijdstip
De piekgradiënten werden eveneens onderverdeeld afhankelijk van de klepmaat die
geïmplanteerd werd of de leeftijd op het tijdstip van de operatie (Tabel 10 en 11). Een significant verschil tussen de piekgradiënten van de verschillende klepmaten werd enkel gevonden bij ontslag (p-waarde = 0) en na 6 maanden (p-waarde = 0,004). Dit significante verschil op 6 maanden bleek na post-hoc testen klinisch niet relevant te zijn. Bij ontslag daarentegen was er een duidelijk lagere piekgradiënt meetbaar naarmate de klepmaat groter werd (Figuur 14 en Tabel 10).
Tabel 10. Pre- en postoperatieve echoparameters: per klepmaat
Variabele Pre-operatief Bij ontslag 3m 6m 1j 18m 2j 3j 4j 5j 6j Per klepmaat 19mm Piekgradiënt Gemiddelde gradiënt 21mm Piekgradiënt Gemiddelde gradiënt 23mm Piekgradiënt Gemiddelde gradiënt 25mm Piekgradiënt Gemiddelde gradiënt 27mm Piekgradiënt Gemiddelde gradiënt 67 ± 18 39 ± 12 72 ± 31 45 ± 20 65 ± 24 40 ± 16 66 ± 25 41 ± 15 73 ± 37 49 ± 14 18 ± 15 11 ± 3 17 ± 6 9 ± 3 14 ± 5 7 ± 3 13 ± 4 7 ± 2 10 ± 4 6 ± 2 9 ± 7 / 15 ± 4 9 ± 3 14 ± 5 8 ± 3 12 ± 5 6 ± 4 6 ± 2 4 ± 0 17 ± 2 10 ± / 19 ± 8 11 ± 10 16 ± 6 9 ± 3 11 ± 2 6 ± 1 13 ± 1 6 ± / 17 ± 2 10 ± / 19 ± 6 10 ± 3 17 ± 10 11 ± 6 14 ± 4 6 ± 2 15 ± 5 6 ± / 20 ± 5 / 21 ± 11 16 ± 9 17 ± 8 9 ± 4 15 ± 3 8 ± 3 13 ± 1 6 ± / 22 ± 7 13 ± 2 19 ± 12 11 ± 8 19 ± 10 11 ± 6 15 ± 3 8 ± 1 10 ± 5 / 21 ± 5 12 ± 3 20 ± 10 12 ± 7 20 ± 10 11 ± 5 16 ± 3 9 ± 2 / / 18 ± 7 16 ± / 19 ± 8 11 ± 5 18 ± 7 10 ± 3 23 ± 13 15 ± 10 3 ± / / 29 ± / 21 ± / 22 ± 13 12 ± 9 21 ± 12 14 ± 7 20 ± 19 14 ± 15 / / / / 44 ± 57 30 ± 39 27 ± 18 / 13 ± 2 / 8 ± / 5 ± /
Continue variabelen zijn weergeven als gemiddelde ± SD. Gemiddelde gradiënt en piekgradiënt zijn weergeven in mmHg.
epm a at b ij o n ts la g
Tijdens de follow-up tot 6 jaar postoperatief kon geen verschil in klepgradiënten in relatie tot de leeftijd bij implantatie worden teruggevonden (Tabel 11).
Tabel 11. Pre- en postoperatieve echoparameters: per leeftijdsgroep
Variabele Pre-operatief Bij ontslag 3m 6m 1j 18m 2j 3j 4j 5j 6j Per leeftijdsgroep < 70 jaar Piekgradiënt Gemiddelde gradiënt 70 - 80 jaar Piekgradiënt Gemiddelde gradiënt > 80 jaar Piekgradiënt Gemiddelde gradiënt 61 ± 30 38 ± 17 67 ± 25 42 ± 17 71 ± 28 44 ± 18 14 ± 5 7 ± 2 15 ± 5 8 ± 3 14 ± 6 8 ± 3 11 ± 6 7 ± 2 14 ± 5 9 ± 4 12 ± 5 7 ± 3 23 ± 7 12 ± 4 15 ± 5 8 ± 3 18 ± 10 11 ± 13 22 ± 15 10 ± 9 17 ± 6 9 ± 4 13 ± 4 8 ± 2 12 ± 2 6 ± 1 21 ± 9 13 ± 8 14 ± 7 9 ± 2 22 ± 11 10 ± 3 19 ± 11 12 ± 8 16 ± 6 9 ± 4 27 ± 13 15 ± 6 20 ± 8 11 ± 5 16 ± 6 10 ± 4 24 ± 10 12 ± 5 20 ± 9 12 ± 6 16 ± 7 10 ± 4 21 ± 13 11 ± 6 20 ± 15 15 ± 12 24 ± 15 14 ± 11 / / 17 ± 13 5 44 ± 59 30 ± 39
Continue variabelen zijn weergeven als gemiddelde ± SD. Gemiddelde gradiënt en piekgradiënt zijn weergeven in mmHg. Leeftijdsgroep op moment van operatie.
6.2.1.2 De echoparameters van het LV
De LV-parameters, zowel de LV-functie als de LV-wanddikte, vertoonden geen duidelijke veranderingen gedurende de follow-up (Tabel 12). Ook hier dient men eveneens de gegevens gedurende de latere follow-up te nuanceren vanwege het hoge aantal missing values en de kleinere populatie.
Tabel 12. Echoparameters linker ventrikel
Variabele Pre-operatief (n = 182) Bij ontslag (n = 169) 3m (n = 166) 6m (n = 162) 1j (n = 158) 18m (n = 151) 2j (n = 135) 3j (n = 106) 4j (n = 82) 5j (n = 49) 6j (n = 15) LV-functie (n (%)) Normaal Gedaald Missing values (%) LV-wanddikte Missing values (%) 138 (75,8%) 44 (24,2%) 0% 12 ± 3 43,4% 119 (70,4%) 50 (29,6%) 0% 10,8 ± 2,3 28,4% 45 (27,1%) 12 (7,2%) 65,7% 12 ± 2,5 80,1% 53 (32,7%) 10 (6,2%) 61,1% 11 ± 3,1 79% 67 (42,4%) 13 (8,2%) 49,4% 11 ± 2,4 70,3% 41 (27,2%) 12 (7,9%) 64,9% 11 ± 2,3 80,1% 66 (48,9%) 8 (5,9%) 45,2% 11 ± 3 67,4% 59 (55,7%) 10 (9,4%) 34,9% 11 ± 3,2 57,5% 36 (43,9%) 13 (15,9%) 40,2% 10,9 ± 2,5 67,1% 24 (49%) 4 (8,2%) 42,8% 11,6 ± 3,1 63,3% 5 (33,3%) 1 (6,7%) 60% 13 ± 1,5 80% Continue niet-normaal verdeelde variabelen zijn weergeven als mediaan ± IQR.
6.2.2 Specifieke klepcomplicaties
De specifieke klepcomplicaties zijn terug te vinden in Tabel 6 en 7. Zowel vroeg- als laattijdig heeft er zich geen trombose van de prothese voorgedaan. Endocarditis trad tweemaal op, maar enkel als een laattijdige complicatie, na 6 maanden en 5 jaar post-implantatie.Structurele
dysfunctie van de Trifecta prothese trad tweemaal op in de studiepopulatie. Zowel de afwezigheid van structurele dysfunctie als de afwezigheid van heroperatie wegens structurele dysfunctie bedroeg op 1 en 5 jaar respectievelijk 100% en 98% (Figuur 15).
*Waarden boven de X-as geven het aantal personen weer die op het onderstaande corresponderende tijdstip nog in de curve betrokken worden.
Figuur 15. Afwezigheid van structurele dysfunctie
Af w ez ig h ei d v an st ru ct ur el e d ys fun ct ie Maanden 182 142 96 43 5 *
7. Discussie
7.1 Klinisch
7.1.1 Mortaliteit en complicaties
Op klinisch vlak komt deze studie tot vergelijkbare resultaten met andere studies, zowel degene die specifiek de Trifecta evalueren als degene die andere aortaklepprothesen evalueren. De overlevingscijfers in de huidige studiepopulatie (na 1 en 5 jaar respectievelijk 85% en 70%) benaderen de cijfers die recent werden aangetoond in de studie van Kilic et al. over de Trifecta, respectievelijk 90% en 70% op 1 en 5 jaar15. De studie van Goldman et al. had echter
overlevingscijfers na Trifecta implantatie op 1 en 6 jaar die hoger lagen, respectievelijk 96,2% en 87,9%16. Een belangrijke kanttekening die hierbij gemaakt dient te worden, is het feit dat de
gemiddelde leeftijd bij operatie in de huidige patiëntenpopulatie (77 jaar) gevoelig hoger lag dan in de studie van Kilic et al. (72 jaar)15 en Goldman et al. (72 jaar)16. De meerderheid van de
laattijdige sterftes in onze studiepopulatie waren voornamelijk van onbekende origine. Dit gegeven dient meegenomen te worden in de evaluatie en nuanceert de hoge laattijdige mortaliteit.
De meest voorkomende vroegtijdige complicatie was een majeure bloeding met nood tot revisie (7,1%). Dit hoge percentage komt overeen met de percentages in vergelijkbare studies11, 16.
Niet-structurele dysfunctie van de Trifecta prothese kwam zowel vroeg- als laattijdig beperkt voor. De meerderheid van de patiënten met een dergelijke complicatie had een klein paravalvulair lek, waarvoor geen heringreep nodig werd geacht. Een paravalvulair lek leidde echter maar bij 1 patiënt tot een heroperatie. Deze specifieke patiënt heeft opnieuw een Trifecta prothese
geïmplanteerd gekregen. De vroegtijdige resultaten zijn inferieur aan deze die bekomen worden in vergelijkbare studies, vroegtijdig is de prevalentie van een paravalvulair lek namelijk 1,6% in de huidige studie tegenover 0,1% in de literatuur11, 16. Voor laattijdige paravalvulaire lekken is de
prevalentie wel overeenstemmend met de literatuur, 0,6% in de huidige studiepopulatie tegenover 0,7% en 0%11, 16.
De trombo-embolische accidenten waren zowel vroeg- als laattijdig hoofdzakelijk cerebraal van aard en gerelateerd aan VKF, hoge NYHA-klasse en comorbiditeiten zoals AHT,
hypercholesterolemie en diabetes mellitus. In de studies van Goldman et al. en Bavaria et al. waren cerebrale trombo-embolieën eveneens het meest frequent11, 16. Gastro-intestinale, cardiale
en pulmonale trombo-embolische gebeurtenissen waren duidelijk minder frequent in de huidige patiëntenreeks. Het voorkomen van deze trombo-embolieën was dus vermoedelijk onafhankelijk van de al of niet aanwezigheid van de Trifecta. Goldman et al. en Bavaria et al. rapporteerden een vroegtijdige prevalentie van trombo-embolische accidenten van respectievelijk 2,8% en
2,7%. In de huidige studie lag dit percentage hoger, namelijk 3,8%. De prevalentie van laattijdige trombo-embolieën bedroeg respectievelijk 3,6% voor Goldman et al. en 1,90% per patiëntenjaren voor Bavaria et al.11, 16 De prevalentie voor deze laattijdige complicatie in de huidige studiereeks
bedroeg 4,8% en 1,68% per patiëntenjaren. De pre-operatieve prevalentie van VKF lag in de huidige studiereeks echter wel hoger dan bij Goldman et al. en Bavaria et al., respectievelijk 17,7% ten opzichte van 8,5% en 8,8%. De prevalentie van VKF gedurende de follow-up kon niet vergeleken worden, wegens het ontbreken van deze gegevens in de studies van Goldman et al. en Bavaria et al11, 16. Rekening houdend met deze hogere pre-operatieve prevalentie, kan dus
geconcludeerd worden dat de resultaten in verband met deze specifieke complicatie gelijk lopen met de resultaten van andere studies.
De postoperatieve nood aan pacemakerimplantatie was in onze reeks 1,1% vroegtijdig en 4,2% laattijdig tijdens follow-up, wat in de lijn ligt van de resultaten gerapporteerd in de meeste chirurgische reeksen17, 18. Wanneer we dit vergelijken met studies over TAVI werden bij de
Edwards Sapien klep (ESV) en de Medtronic CoreValve (MCV) opmerkelijk meer
pacemakerimplantaties vroeg na klepimplantatie gerapporteerd, van 7-17% 17, 19, 20, 21. Het risico
op postoperatieve pacemakerimplantaties bleek bij de sutuurloze kleppen eveneens hoger te liggen, de literatuur rapporteerde namelijk prevalenties van 3,1 tot 28,6%22.
Endocarditis kwam in deze studie niet voor als vroegtijdige complicatie, enkel als een laattijdige complicatie en had een prevalentie van 1,2%. Het risico op endocarditis per patiëntenjaren was 0,42%. Ter vergelijking rapporteerden Goldman et al. eveneens 0% endocarditis binnen 30 dagen postoperatief en een prevalentie van 0,86% op lange termijn16. Bij Bavaria et al. kwam er
vroegtijdig eveneens geen enkele keer endocarditis voor bij de Trifecta kleppen. Laattijdig was er echter een risico per patiëntenjaren van 1,07%11. De resultaten zijn op korte termijn dus
vergelijkbaar, maar op lange termijn minder uniform. Wanneer de vergelijking gemaakt wordt met een TAVI-procedure, rapporteerden Takeji et al. een prevalentie van 2,4% over 2 jaar follow-up ten opzichte van 1,1% over 6 jaar follow-up in de huidige studie23. Dit suggereert een hoger risico
op endocarditis na TAVI-procedures. Kleptrombose kwam in de huidige studie geen enkele keer voor. Andere Trifecta studies rapporteerden eveneens een percentage van 0% voor
kleptrombose11, 16. Zowel de afwezigheid van structurele dysfunctie als de afwezigheid van een
heroperatie voor structurele dysfunctie van de klep na 1 en 5 jaar was respectievelijk 100% en 98%. Vergelijkbare resultaten worden gevonden in andere studies die de Trifecta bestudeerden,
geen enkele keer scheuren van klepblaadjes vastgesteld. Het risico op structurele dysfunctie van de Trifecta is dus vergelijkbaar met andere biologische aortaklepprothesen.
7.1.2 Risicofactoren
De resultaten toonden aan dat er meerdere factoren zijn die een invloed uitoefenen op de mortaliteit en eventuele complicaties. Er was slechts één pre-operatieve parameter die een invloed uitoefende op zowel de vroegtijdige als laattijdige complicaties en mortaliteit, namelijk het pre-operatieve cardiale ritme. De aanwezigheid van VKF bij een patiënt was dus de belangrijkste risicofactor. De urgentie van de operatie was ook een belangrijke risicofactor voor vroegtijdige complicaties, hospitaalmortaliteit en voor late mortaliteit, maar had geen invloed op het
voorkomen van laattijdige complicaties. De resultaten van Kilic et al. toonden eveneens aan dat een electieve geïsoleerde operatie het risico op het voorkomen van zowel vroeg- als laattijdige complicaties en hospitaalmortaliteit verlaagde15. Opvallend is dat andere cardiale parameters
zoals de pre-operatieve NYHA-klasse of een voorgeschiedenis van cardiochirurgie enkel een invloed uitoefenden op het risico voor vroegtijdige complicaties en hospitaalmortaliteit. Hun invloed verdween dus wanneer de patiënt de onmiddellijke postoperatieve periode verliet. Het verschil tussen de invloed van de pre- en postoperatieve LV-functie verdient ook enige verduidelijking. De postoperatieve LV-functie was enkel een significante risicofactor voor het optreden van vroegtijdige complicaties en hospitaalmortaliteit. De pre-operatieve LV-functie was enkel significant geassocieerd met de laattijdige mortaliteit. Dit uitte zich hoogstwaarschijnlijk door het feit dat het ventrikel al een slechte functie had en de aortaklepvervanging hier nog een weinig duurzaam voordeel kon opleveren. De resultaten van Amano et al. zijn vergelijkbaar. Zij concludeerden eveneens dat een slechte pre-operatieve LV-functie leidde tot een significant hoger risico op mortaliteit. In de studie van Amano et al. werd ook de invloed van de LV-functie, na 1 jaar follow-up, bestudeerd. Deze postoperatieve LV-functie was niet significant geassocieerd met algemene mortaliteit, maar wel met cardiale mortaliteit. Amano et al. bestudeerden wel niet specifiek de Trifecta prothese. Hun patiënten hadden zowel biologische (35%) als mechanische kleppen (65%) ontvangen26.
Indien de patiënten die een geïsoleerde ingreep ondergaan hebben, vergeleken worden met deze met een geassocieerde procedure, ongeacht welke, dan kon er geen significant
overlevingsverschil worden aangetoond. Significantie werd wel bijna bereikt bij de Breslow-test, wat impliceert dat dodelijke events kort na de operatie toch niet helemaal los staan van het uitvoeren van een geassocieerde procedure. Hierover kan echter geen sluitende uitspraak gedaan worden. Een geassocieerde TVP of mitraalklepvervanging (MVR) verhoogde echter wel significant het risico op hospitaalmortaliteit. Algemeen wordt in de literatuur een geassocieerde
CABG als een belangrijke risicofactor beschouwd27. In onze studiepopulatie was een
geassocieerde CABG echter niet significant gerelateerd met een toename van de complicaties of mortaliteit. Formica et al. beschreven vergelijkbare resultaten voor geassocieerde CABG bij AVR wat betreft hospitaalmortaliteit, laattijdige complicaties en laattijdige mortaliteit. Voor het risico op vroegtijdige complicaties bij geassocieerde CABG rapporteerden Formica et al. wel een hoger risico28.
Pre-operatieve comorbiditeiten zijn eveneens verbonden aan een verhoogd risico op complicaties of mortaliteit. De voornaamste risicofactor in deze groep was de aanwezigheid van pre-operatief nierfalen. Dit leidde tot een hogere prevalentie aan vroeg- en laattijdige sterftes en vroegtijdige complicaties, maar had geen effect op de laattijdige complicaties. Diabetes mellitus verhoogde enkel het risico op laattijdige complicaties en perifeer vaatlijden enkel op laattijdige mortaliteit.De andere comorbiditeiten die een invloed uitoefenden, deden het risico op vroegtijdige complicaties en hospitaalmortaliteit toenemen (COPD en voorafgaand AMI). Amano et al. concludeerden eveneens dat een slechte nierfunctie significant het risico op mortaliteit verhoogde. Diabetes mellitus leidde in de studie van Amano et al. echter wel tot een significant hoger risico op mortaliteit26.
Uit de resultaten van de multivariabele analyse bleken de belangrijkste risicofactoren een voorafgaand AMI, de postoperatieve LV-functie of de comorbiditeit COPD te zijn voor
respectievelijk vroegtijdige complicaties, hospitaalmortaliteit en laattijdige complicaties. Er werden drie significante risicofactoren gevonden voor de laattijdige mortaliteit. Het ging hier over de urgentie van de operatie, de aanwezigheid van VKF en arteriële hypertensie, waarvan een VKF de belangrijkste risicofactor bleek te zijn. De belangrijkste risicofactoren voor vroegtijdige mortaliteit uit de multivariabele analyse van Kilic et al. waren echter het voorkomen van geassocieerde procedures en de urgentie van een operatie. Cerebrovasculaire aandoeningen verhoogden ook significant het risico. De geassocieerde procedures die een significante stijging van het risico veroorzaakten waren zowel een CABG, als een MVR/MVP, als overige procedures. De postoperatieve LV-functie werd in Kilic et al. echter niet geëvalueerd als een mogelijke
risicofactor voor vroegtijdige mortaliteit15. Kilic et al. zochten via deze multivariabele analyse
eveneens naar risicofactoren voor mortaliteit na 1 jaar en 5 jaar postoperatief. Zowel de urgentie van de operatie, als een geassocieerde CABG of overige procedures waren significant
opgemerkt te worden dat het pre-operatieve ritme en arteriële hypertensie niet opgenomen waren in het multivariabele model van Kilic et al15. De multivariabele analyse van Amano et al. toonde
aan dat zowel een slechte pre-operatieve LV-functie als een slechte nierfunctie significant het risico op mortaliteit deden stijgen. Dit multivariabele model was maar opgebouwd uit vier mogelijke risicofactoren. Diabetes mellitus en de pre-operatieve LV eind-systolische diameter vertoonden geen significante relatie26.
7.2 Hemodynamisch
7.2.1 Trifecta vs. andere Trifecta studies
De gemiddelde gradiënt bij ontslag in deze patiëntenreeks bedroeg 8 ± 3 mmHg. De gemiddelde gradiënten van andere Trifecta studiereeksen bij ontslag bedroegen 6,8 ± 5,315 en 11,4 ± 4,2
mmHg25. Er dient opgemerkt te worden dat de gradiënten in de studie van Kilic et al. onmiddellijk
postoperatief gemeten werden, terwijl de andere gradiënten bij het ontslag werden gemeten. De gradiënten op 6 maanden en 1 jaar na de operatie bij Kilic et al. lopen echter wel gelijk met de gradiënten in de huidige studie na eenzelfde duur van follow-up, namelijk 9,4 ± 6,1 en 10,1 ± 6,2 mmHg in Kilic et al15, 9 ± 7 en 9 ± 7 mmHg in de huidige patiëntenreeks. Goldman et al.
rapporteerde gemiddelde gradiënten van 7,7 ± 3,3 en 9,1 ± 4,8 mmHg respectievelijk na 1 jaar en 3 jaar follow-up16. Deze waarden zijn iets lager dan de huidige resultaten na eenzelfde periode
van follow-up, respectievelijk 9 ± 7 en 11 ± 5 mmHg. Dit verschil wordt groter indien de
gemiddelde gradiënten na 6 jaar follow-up vergeleken worden, respectievelijk 11 ± 6,3 mmHg in de studie van Goldman et al.16 en 21 ± 31 mmHg in de huidige studiereeks. Deze resultaten
dienen echter sterk genuanceerd te worden, aangezien in de huidige patiëntenreeks de gemiddelde gradiënt na 6 jaar uit een heel beperkte populatiegrootte is berekend (n = 3). Hier kunnen dan ook geen conclusies uit getrokken worden.
Gedurende de follow-up was er in de huidige patiëntenreeks nergens een relevant verschil tussen de piekgradiënten van de verschillende klepmaten, behalve bij ontslag. Deze
piekgradiënten werden namelijk groter naarmate de klepmaat kleiner werd. Indien de gemiddelde gradiënten per klepmaat vergeleken worden met de bestaande literatuur, rapporteerden Modi et al. en Ugur et al. minder gunstige gradiënten25, 29. Kilic et al. beschreven daarentegen lagere
gradiënten15. In de huidige studie werden voor de 19 en 21 mm aortaklep een gemiddelde
gradiënt bij ontslag gevonden van respectievelijk 11 ± 3 en 9 ± 3 mmHg. In de andere Trifecta studies bedroegen de gradiënten bij ontslag voor deze klepmaten respectievelijk 12,7 ± 4,4 en 10,7 ± 3,4 mmHg29, 15,1 ± 5 en 12 ± 4,1 mmHg25 en 9,8 ± 5,5 en 7,9 ± 5,7 mmHg15. Dezelfde
verschillen in transvalvulaire gradiënten zetten zich ook door bij de grotere klepmaten. Er dienen echter enkele kanttekeningen geplaatst te worden bij deze resultaten. Zo lijken de gradiënten in de studie van Kilic et al. op het eerste zicht nog lager te liggen, maar zoals eerder vermeld,