ANTENATALE LONGEMBOLIE IN
BELGIË
RESULTATEN VAN DE BELGIAN OBSTETRIC
SURVEILLANCE SYSTEM
Laura Werquin
Stamnummer: 00705692Promotor 1: Dr. Griet Vandenberghe Promotor 2: Prof. Dr. Kristien Roelens
Masterproef master in de specialistische geneeskunde
Voorwoord
Deze thesis ligt mij nauw aan het hart omdat dit onderwerp aansluit bij mijn interesse in maternale pathologie. Gedurende mijn 5-jarige opleiding tot gynaecoloog heb ik reeds heel snel beseft dat verloskunde een vak is waar ik met heel mijn hart van hou. Het is een zware job, welke moed en opperste concentratie vereist, vaak in het holst van de nacht. Deze job is geen nine to five. Met deze job kan je geen beloftes maken over het uur waarop je thuis zal zijn. Deze job is wel iedere dag opnieuw een
belevenis, een verrassing, soms een rollercoaster van emoties wanneer er iets dreigt mis te lopen met een mama of kind.
Jammer genoeg lopen er nog te vaak dingen mis, en ook in België sterven er nog steeds moeders. Maar nog veel meer moeders zien de dood in de ogen en dit aandeel mogen we als zorgverleners niet onderschatten.
Ik wil graag Griet bedanken voor al haar hulp. Ik was niet de gemakkelijkste thesisstudent, want ze heeft toch enkele keren wat achter mijn veren moeten zitten. Toch wil ik graag zeggen dat we tijdens het voorbije anderhalf jaar een hele goede band hebben opgebouwd. B.OSS is haar geesteskind en ik vind het zo’n ontzettend knap initiatief wat zij op poten heeft gezet. Ik hoop dat ik er in de toekomst deel mag van blijven uitmaken.
Dit is voor alle mama’s in deze wereld.
Inhoudstafel
1. Abstract
2. Inleiding en literatuurstudie
2.1 Ernstige maternale morbiditeit 2.2 Registratiesystemen
2.2.1 UKOSS 2.2.2 B.OSS 2.3 Maternale mortaliteit 2.4 Onderzoeksvraag
2.5 Veneuze trombo-embolie in de zwangerschap 2.5.1 Epidemiologie 2.5.2 Pathogenese 2.5.3 Risicofactoren 2.5.4 Symptomatologie 2.5.5 Diagnostiek 2.5.6 Behandeling 2.5.7 Trombofiliescreening 3. Methodologie 3.1 Casus definitie 3.2 Data verzameling 3.3 Ethisch Comité 3.4 Statistiek 4. Resultaten
4.1 Response rate en incidentie 4.2 Risicofactoren 4.3 Diagnose 4.4 Behandeling 4.5 Uitkomst 4.6 Profylaxe 5. Discussie 5.1 Incidentie 5.2 Risicofactoren 5.3 Diagnostiek 5.4 Behandeling 5.5 Uitkomst 5.6 Profylaxe 5.7 Richtlijnen
5.8 Beperkingen van de studie
5.9 Conclusie en toekomstperspectieven 6. Referentielijst
7. Bijlagen
1. ABSTRACT
Inleiding - Volgens de gegevens van het SPE (Studiecentrum voor Perinatale Epidemiologie) is longembolie de tweede belangrijkste oorzaak van maternale sterfte in Vlaanderen. Er is echter bijzonder weinig geweten over de incidentie van niet-fatale longembolie tijdens de zwangerschap. Dit is een near-miss event en wordt gedefinieerd als een levensbedreigende complicatie waarbij een dringende medische interventie noodzakelijk is om het mogelijke overlijden van de moeder te voorkomen. B.OSS (Belgian Obstetrics Surveillance System) voerde daarom een studie uit die probeerde de incidentie, risicofactoren en behandeling van antenatale longembolie in België in kaart te brengen.
Methodologie - Het onderzoek liep over een periode van 4 jaar: van januari 2015 tot en met december 2018. Maandelijks werden alle Belgische materniteiten via e-mail opgeroepen om casussen te rapporteren. Een uitgebreide vragenlijst werd ingevuld in geval van een casus. Dit gebeurde online via www.b-oss.be. De resultaten werden geanalyseerd met behulp van beschrijvende statistiek.
Resultaten - In totaal werden 29 casussen weerhouden voor analyse. Dit resulteert in een incidentie van 0,65/10.000 bevallingen. De mediane amenorroeduur bij diagnose was 30 weken (range 5 weken 1 dag – 38 weken 2 dagen). 72% van de patiënten hadden minstens één identificeerbare risicofactor voor het ontwikkelen van een veneuze trombo-embolie (VTE). Het merendeel van de patiënten werd initieel behandeld met laag-moleculair gewicht heparines (LMWH) (86%). Er was 1 maternale sterfte, 3 vrouwen werden gereanimeerd en in totaal werden 8 patiënten op Intensieve Zorgen opgenomen. Drie patiënten kregen tromboseprofylaxe antepartum. Twee van deze patiënten kregen echter een te lage dosis. Bovendien waren er 3 patiënten die volgens de bestaande richtlijnen tromboseprofylaxe hadden moeten krijgen.
Conclusie - Met deze studie kunnen we aantonen dat ook in België antenatale longembolie een zeldzame, maar ernstige aandoening is. Er is een zeer grote heterogeniteit in de behandeling, maar voornamelijk in de preventie van VTE. Niet alle patiënten die in aanmerking kwamen, kregen (de correcte) tromboseprofylaxe. Er dient gestreefd te worden naar meer uniforme zorg en daarom is er nood aan evidence-based richtlijnen.
2. INLEIDING EN LITERATUURSTUDIE
2.1 Ernstige maternale morbiditeit
In hoge inkomenslanden is maternale sterfte extreem zeldzaam geworden. Voor elke vrouw die overlijdt aan een ernstige obstetrische complicatie is er een veel groter aantal vrouwen dat zal overleven, maar hier mogelijk ernstige sequelen aan zal overhouden. Daarom is het minstens even belangrijk om gevallen van ernstige maternale morbiditeit en maternale near-miss events te onderzoeken (1).
In de verloskunde zijn er verschillende aandoeningen die kunnen leiden tot zogenaamde near-miss events. Dit zijn potentieel levensbedreigende obstetrische complicaties waarbij een dringende interventie nodig is om het mogelijk overlijden van de moeder te voorkomen. Veel van deze obstetrische complicaties kunnen niet voorspeld worden aan de hand van gekende risicofactoren. Gezien deze events zeldzaam zijn, worden gynaecologen en vroedvrouwen hier slechts enkele keren in hun carrière mee geconfronteerd en is individuele expertise beperkt. Deze zeldzame obstetrische aandoeningen worden maar weinig onderzocht, waardoor er beperkte data zijn over incidentie, risicofactoren en pathofysiologie. Daardoor is er een gebrek aan evidence-based richtlijnen omtrent preventie en behandeling van deze complicaties (2).
2.2 Registratiesystemen 2.2.1 UKOSS
Het Verenigd Koninkrijk (VK) was pionier met het oprichten van het UK Obstetric Surveillance System (UKOSS) in 2006. Hiermee wilden onderzoekers nationaal informatie verzamelen om near-miss events en zeldzame aandoeningen in de zwangerschap te identificeren en bestuderen. Om het mogelijk te maken data te verzamelen over kleine aantallen patiënten was de medewerking vereist van alle kraamafdelingen. Op deze manier konden er beschrijvende epidemiologische studies, case-control studies en cohorte studies uitgevoerd worden. Het verzamelen van kennis over incidentie, risicofactoren, pathofysiologie en aanpak leidt tot een beter inzicht en een betere preventie en behandeling van deze zeldzame aandoeningen. Sinds de oprichting in 2006 heeft de UKOSS reeds verschillende studies uitgevoerd en gepubliceerd, waaronder een studie over antenatale longembolie (3,4). In navolging
van het VK hebben verschillende andere landen een gelijkaardig systeem opgezet, waarbij in 2010 het International Network of Obstetric Survey Systems (INOSS) werd opgericht (5).
2.2.2 B.OSS
In 2011 werd het Belgian Obstetric Surveillance System (B.OSS) opgericht. B.OSS maakt officieel deel uit van INOSS. Het is een nationaal registratiesysteem opgericht met de steun van het College voor Moeder en Pasgeborene, een instantie van de federale overheidsdienst voor volksgezondheid. Er zijn twee teams: een team verantwoordelijk voor de Vlaamse materniteiten (inclusief UZ Brussel) en een team verantwoordelijk voor Brussel en Wallonië.
Reeds uitgevoerde studies door B.OSS zijn: uterusruptuur (2012-2013), peripartum hysterectomie en arteriële embolisatie (2012-2013), eclampsie (2012-2014), spontaan hemoperitoneum tijdens de zwangerschap (09/2015-12/2017) en anafylaxie tijdens de zwangerschap (09/2016 – 01/2018).
2.3 Maternale mortaliteit
Registratie van de maternale sterfte in Vlaanderen gebeurt via het SPE (Studiecentrum voor Perinatale Epidemiologie). Aldaar werden er sinds het begin van de statistieken in 1997 tot en met 2018 102 gevallen van maternale sterfte gerapporteerd. Dit komt overeen met ongeveer 1/20.000 bevallingen. Dertien van deze patiënten zijn overleden aan de gevolgen van een longembolie. Dit is de tweede meest frequente oorzaak van maternale sterfte na vruchtwaterembolie (6). De sterftecijfers van Brussel en Wallonië worden niet geregistreerd.
Longembolie is dus een van de belangrijkste oorzaken van maternale sterfte, maar vermoedelijk nog een veel belangrijkere oorzaak van ernstige maternale morbiditeit. Deze near-miss events worden jammer genoeg nergens geregistreerd, waardoor men geen idee heeft hoeveel ernstige complicaties als gevolg van longembolie er bij aanstaande moeders optraden. Daarom besloot B.OSS een prospectieve studie te starten waarbij gepoogd werd alle casussen van antenatale longembolie in België te registreren over een periode van 4 jaar. De studie liep van januari 2015 tot en met december 2018.
2.4 Onderzoeksvraag
Er zal een antwoord geformuleerd worden op volgende onderzoeksvragen: 1. Wat is de incidentie van antenatale longembolie in België?
2. Hoe wordt antenatale longembolie in België gediagnosticeerd en behandeld? Welke richtlijnen worden er gebruikt?
3. Wat is de outcome van antenatale longembolie in België voor moeder en kind?
4. Kunnen we uit deze studie lessen trekken om de kwaliteit van (obstetrische) zorg in België te verbeteren?
2.5 Veneuze trombo-embolie in de zwangerschap 2.5.1 Epidemiologie
Veneuze trombo-embolie (VTE) is een aandoening die zowel diepe veneuze trombose (DVT) als longembolie (LE) omvat. VTE is verantwoordelijk voor 3% van alle maternale overlijdens wereldwijd en de belangrijkste oorzaak van maternale sterfte in hoge inkomenslanden (7).
Tijdens de zwangerschap heeft een vrouw vijfmaal meer kans om een veneuze trombo-embolie te ontwikkelen in vergelijking met een niet-zwangere vrouw van dezelfde leeftijd. De incidentie van VTE in de zwangerschap en het postpartum wordt geschat op 1-2 per 1000 zwangerschappen (8,9). Ongeveer 75% hiervan presenteert zich met een DVT, 20 à 25% presenteert zich met (bijkomstig) een longembolie. In het postpartum is het risico op VTE tien tot twintig keer verhoogd in vergelijking met niet-zwangere vrouwen van dezelfde leeftijd. Het hoogste risico ziet men in de eerste drie tot zes weken postpartum. Nadien daalt het risico snel, hoewel er een residueel risico kan blijven tot 12 weken na de bevalling. De grootste risicoperiode antenataal is het derde trimester (9,10).
2.5.2 Pathogenese
Algemeen wordt de triade van Virchow aanvaard als basis voor het ontstaan van een DVT: veneuze stase, endotheelschade en hypercoagulabiliteit. De zwangerschap is een protrombogene situatie, waarbij men de drie componenten van deze triade terugvindt.
Veneuze stase wordt veroorzaakt door een hormonaal geïnduceerde vermindering in veneuze tonus en een obstructie van veneuze flow in het bekken door de vergrote uterus (10).
Endotheelschade ter hoogte van pelviene venen kan optreden tijdens de bevalling of door zwangerschapshypertensie. Trombose van de pelviene venen is verantwoordelijk voor een belangrijk deel van de DVT ante- en postnataal en wordt maar zelden gezien buiten de zwangerschap (12).
Vanaf het begin van de zwangerschap zijn er fysiologische veranderingen waarbij het lichaam in een staat van hypercoagulabiliteit gaat. Deze veranderingen dienen om de zwangere vrouw te beschermen tegen eventuele bloeding bij miskraam of bevalling. Niet te vergeten is dat in ontwikkelingslanden de belangrijkste oorzaak van maternale sterfte nog steeds hemorragie is (7). Deze status van hypercoagulabiliteit is de belangrijkste risicofactor. De vorming van fibrinogeen neemt significant toe (stijging tot 50%), fibrinolytische activiteit vermindert, de concentraties van stollingsfactoren II, VII, VIII, IX en X zijn toegenomen. Er is een progressieve daling van endogene anticoagulantia zoals proteïne S en antitrombine (AT) en men ziet een verworven resistentie aan geactiveerd proteïne C (10).
2.5.3 Risicofactoren
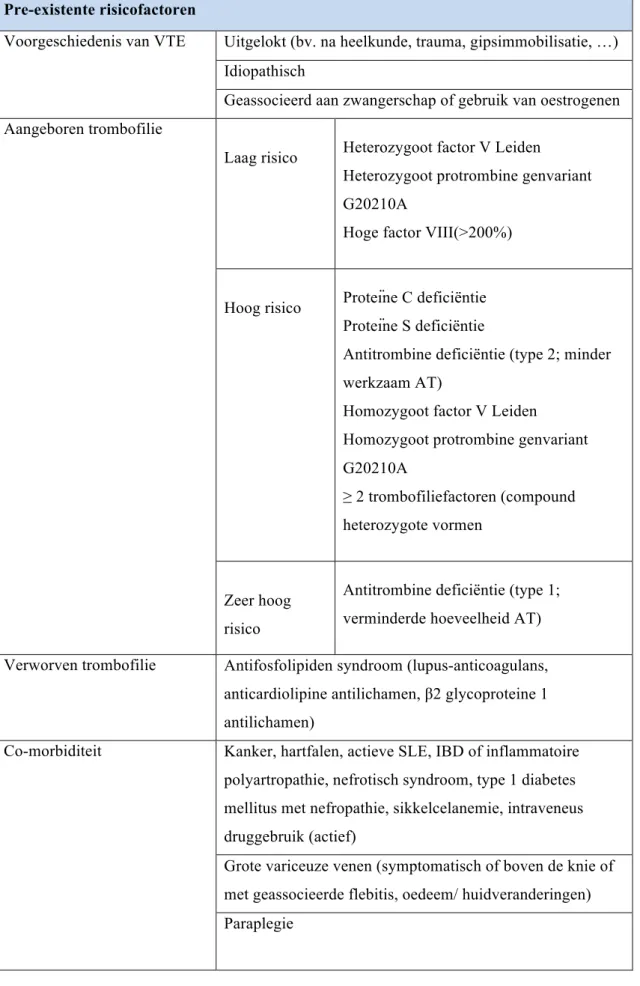
De klassieke gekende risicofactoren voor het ontwikkelen van een VTE blijven gelden in de zwangerschap (tabel 1), zoals persoonlijke voorgeschiedenis van VTE; aangeboren of verworven trombofilie; co-morbiditeiten zoals systemische lupus erythematosus; patiënt-afhankelijke risicofactoren zoals leeftijd, roken en BMI (Body Mass Index). Bovendien kunnen er risicofactoren aanwezig zijn die van voorbijgaande aard zijn zoals tijdelijke immobilisatie, dehydratatie, infectie, heelkunde, … Ten slotte zijn er nog bijkomende obstetrische factoren die een verhoogd risico op VTE met zich kunnen meebrengen zoals bijvoorbeeld pre-eclampsie, meerlingzwangerschap, langdurige arbeid, (secundaire) sectio,… Electieve sectio caesarea verdubbelt het risico in vergelijking met vaginale baring. Een urgente sectio is geassocieerd met een verdere verdubbeling van het risico t.o.v. een geplande sectio.
Tabel 1: Risicofactoren voor VTE (8)
Pre-existente risicofactoren
Voorgeschiedenis van VTE Uitgelokt (bv. na heelkunde, trauma, gipsimmobilisatie, …) Idiopathisch
Geassocieerd aan zwangerschap of gebruik van oestrogenen Aangeboren trombofilie
Laag risico Heterozygoot factor V Leiden
Heterozygoot protrombine genvariant G20210A
Hoge factor VIII(>200%)
Hoog risico Proteïne C deficiëntie Proteïne S deficiëntie
Antitrombine deficiëntie (type 2; minder werkzaam AT)
Homozygoot factor V Leiden
Homozygoot protrombine genvariant G20210A
≥ 2 trombofiliefactoren (compound heterozygote vormen
Zeer hoog risico
Antitrombine deficiëntie (type 1; verminderde hoeveelheid AT)
Verworven trombofilie Antifosfolipiden syndroom (lupus-anticoagulans, anticardiolipine antilichamen, β2 glycoproteine 1 antilichamen)
Co-morbiditeit Kanker, hartfalen, actieve SLE, IBD of inflammatoire polyartropathie, nefrotisch syndroom, type 1 diabetes mellitus met nefropathie, sikkelcelanemie, intraveneus druggebruik (actief)
Grote variceuze venen (symptomatisch of boven de knie of met geassocieerde flebitis, oedeem/ huidveranderingen) Paraplegie
Patiënt-afhankelijke risicofactoren
Leeftijd > 35 jaar Roken
Obesitas : BMI ≥ 30 preconceptioneel of bij intake Pariteit ≥ 3
Familiale voorgeschiedenis Idiopathische of oestrogeen-geassocieerde VTE < 50jaar bij een eerstegraads verwant
Nieuw ontstane / transiënte risicofactoren
Belangrijk om steeds opnieuw de individuele risicofactoren te reëvalueren
Chirurgische ingreep in zwangerschap of postpartum Fractuur
Hyperemesis, dehydratatie Ovariële hyperstimulatie, ART
Hospitalisatie of immobilisatie (>3dagen bedrust)
Systemische infectie (nood aan antibiotica of hospitalisatie) Langdurige reizen (>4u)
Obstetrische risicofactoren
Meerlingzwangerschap Pre-eclampsie
Sectio caesarea (RR secundaire sectio > RR primaire sectio) Langdurige arbeid (>24u)
Kunstverlossing MIU
Partus prematurus
PPH (> 1) en/of transfusienood
SLE= systemische lupus erythematosus , IBD= inflammatoire darmziekte, MIU= mors in utero, PPH= postpartum hemorragie, ART= geassisteerde reproductieve voortplanting
2.5.4 Symptomatologie
Een veneuze trombo-embolie is moeilijker te diagnosticeren in de zwangerschap (7). Het belang van een goede anamnese en klinisch onderzoek mag niet onderschat worden. Een beperkte longembolie kan bij jonge, gezonde vrouwen echter soms een
verschijnselen in de zwangerschap (bijvoorbeeld tachypneu en kortademigheid). Typische klachten van een longembolie zijn dyspneu, thoracale pijn (al dan niet unilateraal) welke vaak ademhalingsgebonden is, hoest, hemoptoe, collaps. In 83% van de gevallen zijn er acute klachten welke in minuten of uren opkomen, maar de symptomen kunnen ook geleidelijk optreden over het verloop van uren tot dagen.
2.5.5 Diagnostiek Klinisch onderzoek
In de meerderheid van de gevallen is er tachypneu en tachycardie. Longauscultatie kan afwijkend zijn met crepitaties, ronchi of verminderd ademgeruis, maar dit is niet obligaat. Hypoxie zien we in een minderheid van de gevallen. Het meten van de saturatie is dus een handige, maar niet erg specifieke test. Een ernstige hypoxie met een saturatie <90% ziet men slechts in 3% van de gevallen (10).
Laboratoriumonderzoeken
D-dimeren zijn beperkt bruikbaar gezien de fysiologische stijging tijdens de zwangerschap en het postpartum. De negatieve predictieve waarde blijft weliswaar hoog: indien D-dimeren laag zijn (<500ng/mL) is een longembolie weinig waarschijnlijk.
Arterieel bloedgas kan een hypoxemie met een hypocapnie en een respiratoire alkalose tonen. Arterieel bloedgas kan echter bij zwangeren vaak nog normaal zijn en bovendien kan hypocapnie een normaal fysiologisch verschijnsel zijn in de zwangerschap (10).
Beeldvorming
RX thorax is vaak normaal, maar is een essentieel onderdeel van de onderzoeken om andere belangrijke oorzaken van dyspneu, thoracale pijn of hypoxie uit te sluiten zoals bijvoorbeeld pneumonie of pneumothorax.
Bij concomitant vermoeden van DVT dient eerst een compressie-echografie met duplex van de onderste ledematen worden uitgevoerd. Indien deze de aanwezigheid van een DVT bevestigt, kan er gestart worden met anticoagulantia zonder verdere onderzoeken (13).
Bij sterk vermoeden van longembolie zonder tekenen van DVT of negatieve echo-duplex van de onderste ledematen kan er een ventilatie/perfusie scan (V/Q-scan) of
een CT-angiografie worden uitgevoerd. Beide onderzoeken zijn veilig in de zwangerschap. Bij een V/Q-scan verkiest men om bij een zwangere vrouw initieel enkel een perfusiescan te verrichten ter reductie van de stralenbelasting. Deze kan slecht doorbloede zones in de long aantonen. Indien nodig kan een bijkomende ventilatiescan een eventuele ventilatie/perfusie mismatch aantonen. Dit onderzoek heeft vermoedelijk een iets grotere negatieve predictieve waarde dan een CT -angiografie. Het nadeel van een V/Q-scan is dat deze niet steeds beschikbaar is en dus niet in urgente setting kan gebruikt worden. De totale straling voor de foetus bij een V/Q-scan is minimaal. CT-angiografie is een evenwaardig onderzoek en kan eveneens veilig gebruikt worden in de zwangerschap. De straling voor de foetus is bij het gebruik van een loodschort minimaal en minder dan bij een V/Q-scan, maar er is een significante radiatie van het maternale zwangere borstklierweefsel. De stralingsdosis kan met 20-40% verminderd worden door het gebruik van bismuth shields t.h.v. de maternale borst. Het voordeel is dat een CT-angiografie steeds beschikbaar is en dus nuttig indien een urgente diagnose noodzakelijk is. Ook bij vooraf bestaande longpathologie is CT-angiografie superieur aan V/Q-scan en bovendien kan een CT-scan ook andere pathologie identificeren (10, 13).
Bijkomende technische onderzoeken
Echo cor kan worden uitgevoerd bij een bewezen longembolie. Rechter ventrikel overbelasting geeft een indicatie omtrent de ernst en kan implicaties hebben naar beleid toe, zoals bijvoorbeeld opname op hartbewaking, noodzaak tot trombolyse, … ECG kan normaal zijn behoudens een sinus tachycardie. Bij een grote longembolie kan het ECG afwijkend zijn. Bovendien kunnen hier andere oorzaken van thoracale pijn mee worden uitgesloten (10).
2.5.6 Behandeling Anticoagulantia
Bij klinisch sterke verdenking op DVT of longembolie dient behandeling met anticoagulantia onmiddellijk gestart te worden totdat de diagnose uitgesloten is d.m.v. technische onderzoeken, tenzij behandeling gecontra-indiceerd is (10, 13). De
standaardbehandeling van een VTE bestaat uit de subcutane toediening van laag-moleculair gewicht heparines (LMWH). De dosis is gebaseerd op het gewicht van de
gebruikt worden in de zwangerschap: Enoxaparine (Clexane®), Nadroparine (Fraxiparine/Fraxodi®), Dalteparine (Fragmin®), Tinzaparine (Innohep®).
In geselecteerde gevallen kan het geïndiceerd zijn om ongefractioneerde heparine (UFH) te gebruiken. Dit kan intraveneus of subcutaan. De voordelen van LMWH t.o.v. ongefractioneerde heparine (UFH) zijn talrijk: minder risico op bloeding, lagere prevalentie van geïnduceerde trombocytopenie (HIT) en heparine-geïnduceerde osteoporose. Bovendien ziet men bij UFH een onvoorspelbare dosis-respons relatie, met de noodzaak tot frequente monitoring van aPTT (geactiveerde partiële tromboplastinetijd). Voordelen zijn de kortere halfwaardetijd, de beschikbaarheid van een antidotum (protamine) en het feit dat UFH niet via de nier uitgescheiden worden. Allergische huidreacties kunnen bij beide geneesmiddelen voorkomen.
Bij een massieve longembolie met hemodynamische repercussies is intraveneus UFH de eerste keuze behandeling. Enkel bij levensbedreigende situaties zijn trombolyse of chirurgische trombectomie van toepassing (9, 10,13).
Indien heparine gecontra-indiceerd is (bijvoorbeeld bij HIT of ernstige huidallergie), kan er eventueel gebruik gemaakt worden van Fondaparinux, een synthetische factor Xa inhibitor welke volgens preliminaire data veilig zou zijn in de zwangerschap (14). Wat betreft de directe orale anticoagulantia (DOAC’s) zijn er onvoldoende gegevens over de veiligheid en deze zijn daarom gecontra-indiceerd tijdens de zwangerschap en de borstvoeding. Vitamine K-antagonisten (VKA) gaan transplacentair en zijn dan ook gecontra-indiceerd in de zwangerschap. Ze kunnen congenitale afwijkingen geven bij gebruik in het eerste trimester. VKA kunnen wel veilig gebruikt worden tijdens de borstvoeding en kunnen opgestart worden vanaf dag 5 postpartum. De meeste ervaring is er met Warfarine (14).
2.5.7 Trombofiliescreening
Vrouwen die tijdens de zwangerschap een VTE hebben doorgemaakt moeten postpartum worden aangemeld voor een hematologisch consult. Hier kan besproken worden wat de persoonlijke risico’s voor deze patiënte zijn in een volgende zwangerschap of tijdens bepaalde risicoperiodes. Bovendien moet er gesproken worden over de contraceptieve opties. Trombofiliescreening dient uitgevoerd te worden wanneer de anticoagulantia gestopt zijn en alleen indien men denkt dat de resultaten de toekomstige aanpak voor deze vrouw zullen beïnvloeden (13).
3. METHODOLOGIE
3.1 Casus definitie
B.OSS heeft dezelfde definitie van antenatale longembolie gehanteerd als UKOSS, dit om eventuele internationale studies mogelijk te maken in de toekomst.
- Bevestiging door middel van geschikte beeldvorming (angiografie, CT scan, MRI scan of ventilatie/perfusiescan) die met grote waarschijnlijkheid longembolie aantoont
OF
- Bevestiging tijdens chirurgie of post-mortem onderzoek OF
- Klinische diagnose aan de hand van symptomen en klinische tekenen, behandeling met anticoagulantia > 1 week
3.2 Data verzameling
Data werden verzameld gedurende 4 jaar: van januari 2015 t.e.m. december 2018 via het bestaande systeem van B.OSS. Rapportering gebeurt op vrijwillige basis. Elk ziekenhuis heeft zelf een contactpersoon aangesteld die hiervoor verantwoordelijk is. Meestal is dit een gynaecoloog, maar dit kan ook bijvoorbeeld een vroedvrouw of een andere medewerker zijn. De contactpersoon krijgt maandelijks een e-mail toegestuurd met de vraag of er die maand zich een bepaalde complicatie heeft voorgedaan in het betreffende ziekenhuis. Via een link naar de website (www.b-oss.be) kan het rapporteringsformulier en aansluitend een uitgebreide vragenlijst worden ingevuld. De vragenlijst (bijlage 1) werd opgesteld aan de hand van de vragenlijst van UKOSS en behandelt volgende variabelen:
- Eigenschappen van de moeder (leeftijd, BMI, etniciteit, burgerlijke staat, beroep, nicotine abusus).
- Medische, obstetrische en familiale voorgeschiedenis. - Het verloop van de huidige zwangerschap.
- Symptomatologie van de LE, uitgevoerde onderzoeken ter diagnostiek. - Behandeling: welke, duur van de behandeling.
- Uitkomst van de moeder. - Uitkomst van de neonaat.
Alle gegevens zijn gecodeerd en dus anoniem. Indien er achterstand is bij de registratie of bijkomende informatie gewenst is over een aangemelde casus, kan een lid van het B.OSS team ter herinnering de contactpersonen telefonisch of via email contacteren.
3.3 Ethisch comité
Het B.OSS project algemeen en deze studie werd goedgekeurd door het centrale Ethisch Comité van het UZ Gent (Belgisch registratienummer B6780201526875, EC UZG 2015/1470), vervolgens werden de Ethische comités van de deelnemende ziekenhuizen op de hoogte gebracht. De patiënte werd geïnformeerd over de studie door haar behandelende arts middels een informatiebrief ( https://www.b-oss.be/patient-information-letter). Na ingaan van de nieuwe Europese GDPR-wetgeving in mei 2018 werden patiënten gevraagd om een informed consent te ondertekenen.
3.4 Statistiek
Gezien de beperkte sample-size en het ontbreken van een controlegroep, worden de gegevens enkel via beschrijvende statistiek geanalyseerd. De resultaten worden vergeleken met de resultaten van de UKOSS studie (4) en met bestaande richtlijnen in verband met profylaxe, diagnose en management van longembolie in de zwangerschap van de RCOG (8,13). Belgische richtlijnen zijn schaars en de laatste update dateert van 2009 (15).
4. RESULTATEN
4.1 Response rate en incidentie
Er werden 32 casussen van antenatale longembolie aangemeld. Eén casus werd dubbel aangemeld, van 1 casus werden geen data ontvangen en 1 casus werd niet weerhouden omdat deze niet aan de definitie voldeed, het ging namelijk om een vruchtwaterembool. Na exclusie van deze 3 casussen werden er 29 casussen weerhouden.
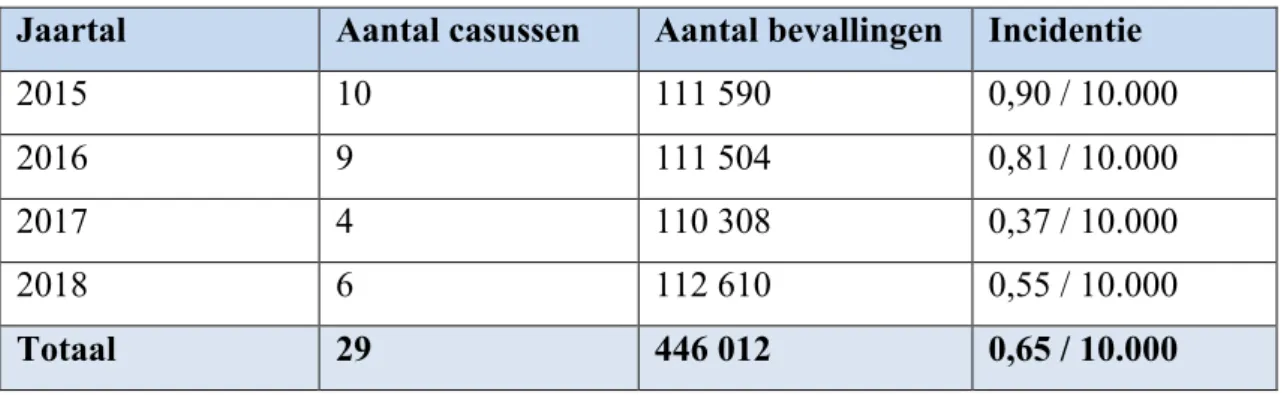
De response rate is de ratio van het aantal ingevulde op het aantal uitgestuurde rapporteringsformulieren. In 2015 was dit 92%, in 2016 92,9%, in 2017 94,4% en in 2018 96,3%. Eén groot ziekenhuis weigert deelname aan de B.OSS registratie. Bovendien zijn er zes andere ziekenhuizen die slechts enkele maanden tot een jaar lang gerapporteerd hebben. Indien men alle bevallingen die plaatsvinden in deze ziekenhuizen optelt, zijn zij samen verantwoordelijk voor jaarlijks meer dan 9000 bevallingen. De noemer voor de berekende incidentie werd hieraan aangepast, wat deze op 446 012 bevallingen brengt over 4 jaar tijd (tabel 2). Het aantal bevallingen is gebaseerd op de cijfers afkomstig van de jaarrapporten van het SPE en CepiP (6, 16, 17). Dit resulteert in een geschatte incidentie van 0,65/10.000 bevallingen.
Tabel 2: Berekening incidentie longembolie
Jaartal Aantal casussen Aantal bevallingen Incidentie
2015 10 111 590 0,90 / 10.000 2016 9 111 504 0,81 / 10.000 2017 4 110 308 0,37 / 10.000 2018 6 112 610 0,55 / 10.000 Totaal 29 446 012 0,65 / 10.000 4.2 Risicofactoren
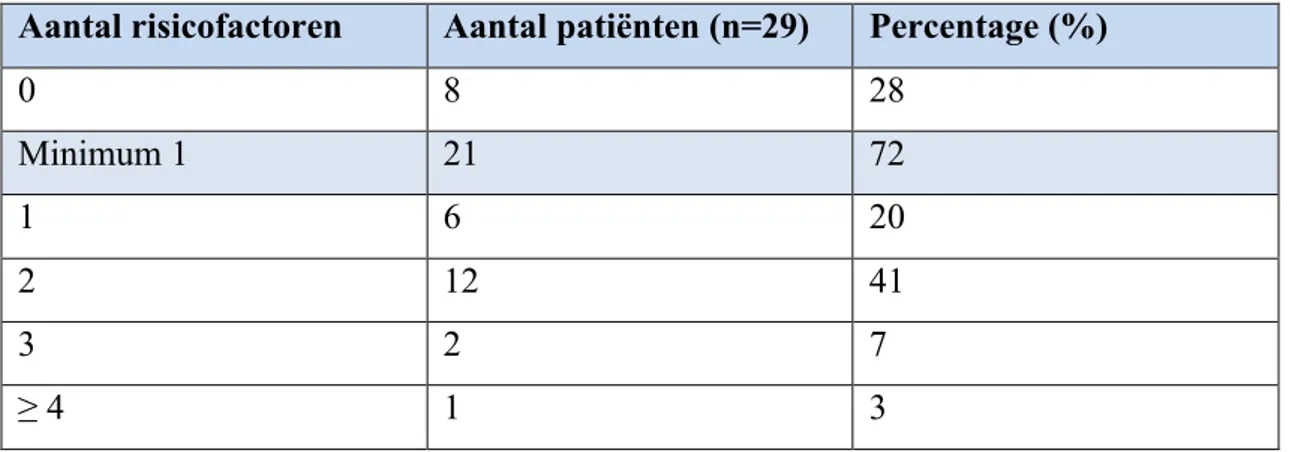
Acht patiënten hadden geen enkele identificeerbare risicofactor en 21 patiënten (72%) hadden minstens één klassieke risicofactor voor het ontwikkelen van een VTE (tabel 3, tabel 4).
Tabel 3: Aantal aanwezige risicofactoren bij patiënten
Aantal risicofactoren Aantal patiënten (n=29) Percentage (%)
0 8 28 Minimum 1 21 72 1 6 20 2 12 41 3 2 7 ≥ 4 1 3
Tabel 4: Risicofactoren geïdentificeerd bij de patiënten met longembolie
Risicofactor Aantal Percentage (%)
Persoonlijke voorgeschiedenis DVT 3 10
Gekende trombofilie - laag risico - hoog risico
Nieuwe diagnose trombofilie Totaal trombofilie 5 4 1 2 7 17 14 3 7 24 Familiale voorgeschiedenis DVT 3 10 Leeftijd ≥ 35 jaar 8 28 BMI 25-30kg/m2 BMI ≥ 30kg/m2 17 1 59 3 Pariteit ≥ 3 5 17
Actief roken of gestopt tijdens zwangerschap 7 24 Meerlingzwangerschap 2 7 (Relatieve) immobilisatie - hospitalisatie - dehydratatie
- langdurige reis (> 10u)
8 5 2 1 28 17 7 3
Voorgeschiedenis van VTE
Drie patiënten hadden een persoonlijke voorgeschiedenis van een VTE. Eén patiënte had een DVT doorgemaakt tijdens een vorige zwangerschap en bovendien een
longembolie onder OAC (orale anticonceptie). De tweede patiënte had reeds 7 keer een DVT doorgemaakt, die eenmalig gecompliceerd werd door een longembolie. De derde patiënte had een eenmalige DVT in de voorgeschiedenis. Al deze patiënten waren gekend met een trombofilie. Er waren 3 patiënten met een positieve familiale anamnese voor VTE. Er werd niet gespecifieerd of dit een eerstegraadsverwant betrof.
Trombofilie
Er was een gekende trombofilie bij 5 patiënten: 4 patiënten met een laag risico trombofilie (2 met heterozygoot factor V Leiden en 2 met een verhoogde factor VIII) en 1 patiënt met een hoog risico trombofilie (homozygoot factor V Leiden).
Bij 11 patiënten werd een postpartum trombofiliescreening uitgevoerd. Bij 9 patiënten was deze normaal, bij 2 patiënten was deze afwijkend: 1 patiënt die factor V Leiden heterozygoot bleek te zijn en 1 patiënt die drager was van een protrombine genmutatie G20210A. Bij de resterende 11 patiënten werd geen trombofiliescreening uitgevoerd of werd dit niet gerapporteerd. In totaal waren er dus 7 patiënten met een trombofilie, dit komt overeen met 24% van de studiepopulatie.
Leeftijd ≥ 35 jaar
Acht patiënten (28%) waren 35 jaar of ouder.
BMI > 30
Er was 1 patiënte met obesitas (BMI > 30kg/m2), namelijk 32,5kg/m2. Bij 1 patiënt werd obesitas vermeld in de voorgeschiedenis, maar werd lengte noch gewicht gerapporteerd. Er waren echter ook 17 patiënten te weerhouden met overgewicht (BMI 25-30kg/m2), wat overeenkomt met bijna 59%. Bij 2 patiënten werd het BMI niet vermeld.
Pariteit
Er waren 8 primiparae en 21 multiparae, waarvan 5 patiënten met een pariteit ≥ 3.
Roken
Vier patiënten waren actieve rooksters en 3 patiënten waren gestopt met roken tijdens de zwangerschap.
Immobilisatie
Vijf patiënten ontwikkelden een longembolie tijdens of kort na een hospitalisatie. Het betroffen 3 opnames in kader van dreigende vroeggeboorte of PPROM (preterm prelabour rupture of membranes) en 2 opnames naar aanleiding van braken en dehydratatie. Drie patiënten werden omwille van premature contracties relatieve rust voorgeschreven, maar waren niet opgenomen in het ziekenhuis. Eén patiënte had recent een lange vliegtuigreis van meer dan 10 uur ondernomen. Twee patiënten kregen tromboseprofylaxe onder de vorm van TED-kousen (Trombo Embolism Deterrent), maar geen enkele patiënte kreeg LMWH toegediend.
4.3 Diagnose Amenorroeduur
De mediane amenorroeduur bij diagnose was 30 weken (range 5 weken 1dag – 38 weken 2 dagen), wat bevestigt dat het merendeel van de antenatale longembolieën voorkomen in het derde trimester.
Symptomatologie
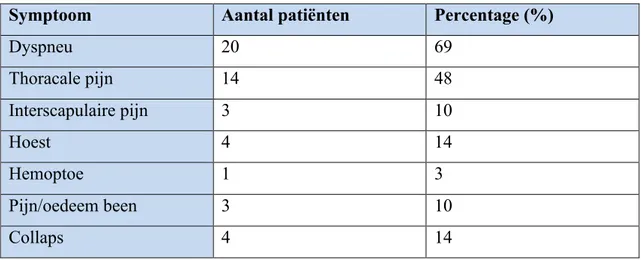
Het frequentst gerapporteerde symptoom was dyspneu, dit kwam voor bij bijna 70% van de patiënten. Ongeveer de helft van de patiënten klaagde van thoracale pijn. Vier patiënten presenteerden zich met collaps en bewustzijnsverlies, drie van deze patiënten hadden een hartstilstand en moesten gereanimeerd worden (tabel 5).
Tabel 5: Symptomatologie
Symptoom Aantal patiënten Percentage (%)
Dyspneu 20 69 Thoracale pijn 14 48 Interscapulaire pijn 3 10 Hoest 4 14 Hemoptoe 1 3 Pijn/oedeem been 3 10 Collaps 4 14
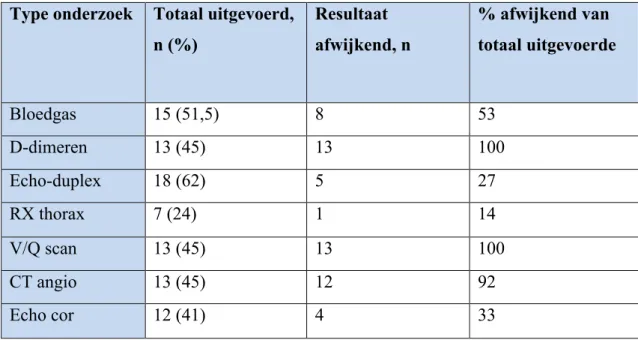
Diagnostische technieken
Er werden verschillende technieken gebruikt om tot de diagnose te komen, met vaak meerdere onderzoeken bij dezelfde patiënt (tabel 6). Bloedgasanalyse werd bij de helft van de patiënten uitgevoerd en was bij 53% afwijkend. D-dimeren werden bij 45% van de patiënten bepaald en waren bij iedereen gestegen (> 500ng/mL) (range 733ng/mL – 126 187ng/mL). Duplexechografie werd gebruikt bij 62% van de patiënten, maar kon slechts bij 1 op 4 van deze patiënten een DVT aantonen. Zeven patiënten kregen een RX-thorax, deze was slechts bij 1 patiënt afwijkend. Dertien patiënten ondergingen een V/Q-scan, deze kon bij iedereen een longembolie aantonen. Eveneens 13 patiënten kregen een CT-angiografie, welke bij 12 op 13 afwijkend was. Dit wil zeggen dat in totaal 26 van de 29 patiënten beeldvorming van de thorax kregen onder de vorm van een V/Q-scan of een CT-angiografie. Bij de overige 3 patiënten werd reeds een diagnose van DVT gesteld bij duplex echografie met bij 1 patiënt eveneens een afwijkende echo cor.
Tabel 6: Gebruikte diagnostische middelen Type onderzoek Totaal uitgevoerd,
n (%) Resultaat afwijkend, n % afwijkend van totaal uitgevoerde Bloedgas 15 (51,5) 8 53 D-dimeren 13 (45) 13 100 Echo-duplex 18 (62) 5 27 RX thorax 7 (24) 1 14 V/Q scan 13 (45) 13 100 CT angio 13 (45) 12 92 Echo cor 12 (41) 4 33 4.4 Behandeling
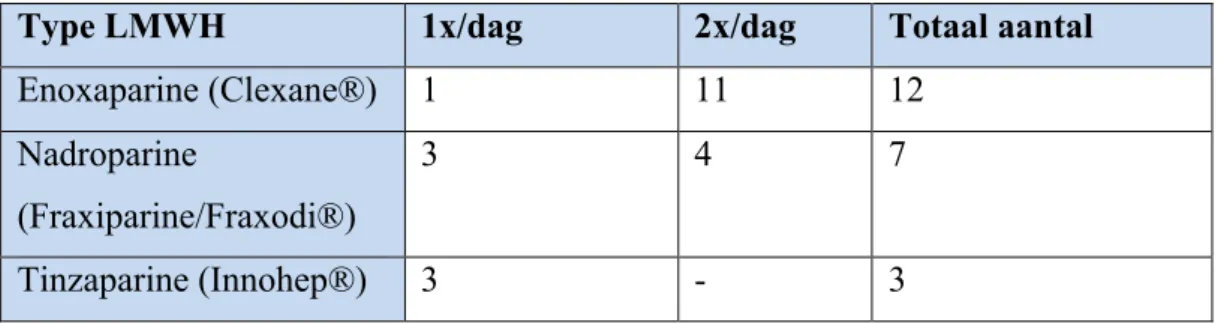
Er werden 25 patiënten initieel behandeld met LMWH (86%). De gebruikte types LMWH waren Enoxaparine (Clexane®), Nadroparine (Fraxiparine/Fraxodi®) en Tinzaparine (Innohep®) (tabel 7). Het meest gebruikte regime was Enoxaparine 2 maal daags. Er waren 3 patiënten bij wie na een bepaalde periode werd
overgeschakeld op een ander type LMWH. Er werd niet gespecifieerd waarom deze beslissing werd gemaakt.
Tabel 7: Behandeling met laag-moleculair gewicht heparines (LMWH)
Type LMWH 1x/dag 2x/dag Totaal aantal
Enoxaparine (Clexane®) 1 11 12
Nadroparine
(Fraxiparine/Fraxodi®)
3 4 7
Tinzaparine (Innohep®) 3 - 3
Drie patiënten werden behandeld met heparine IV. De eerste patiënte werd al therapeutisch ontstold met LMWH na een doorgemaakte DVT eerder die zwangerschap. De tweede patiënte werd initieel behandeld met een suboptimale dosis Nadroparine en werd daags nadien opgenomen op intensieve zorgen omwille van pulmonale hypertensie waarbij heparine IV werd gestart. Nadien werd er opnieuw overgegaan naar LMWH. De derde patiënte had een hartstilstand, werd gereanimeerd en overleefde. Eén patiënte kreeg trombolyse na hartstilstand en reanimatie. Eén patiënte werd chirurgisch behandeld middels trombectomie na reanimatie. Deze patiënte overleed 2 dagen later.
De duur van de behandeling verschilde enorm; gaande van 2 weken, 3 à 6 maand, tot levenslang. Bij 5 patiënten werd de duur van de behandeling niet gespecifieerd. Bij 5 patiënten werd postpartum gekozen voor DOAC’s zoals Rivaroxaban (Xarelto®) of Edoxaban (Lixiana®). Bij 2 patiënten werd overgegaan op VKA zoals Warfarine (Marevan®) of Acenocoumarol (Sintrom®).
4.5 Uitkomst Maternale uitkomst
Er werd 1 maternale sterfte gerapporteerd. Deze patiënte had geen enkele identificeerbare risicofactor voor het ontwikkelen van een VTE. Het event deed zich voor op 20 weken zwangerschap. De patiënte werd opgenomen via de spoedgevallendienst met een hartstilstand. Zij werd gereanimeerd en er werd nog chirurgisch ingegrepen, maar omwille van vegetatieve toestand werden na 2 dagen de
intensieve zorgen gestaakt. In totaal werden er 3 patiënten gereanimeerd. Ernstige maternale morbiditeit trad op bij 8 patiënten (27%) en al deze patiënten werden opgenomen op de dienst Intensieve Zorgen, met een gemiddelde ligduur van 5 dagen. Drie van deze patiënten hadden nood aan kunstmatige ventilatie. Redenen voor opname op Intensieve Zorgen waren pulmonale hypertensie, peripartum cardiomyopathie, collaps en ernstige postpartum bloeding.
Zwangerschapsuitkomst
De mediane amenorroeduur bij partus was 38 weken 2 dagen (range 33 weken 2 dagen – 41 weken 2 dagen).
Twee patiënten hadden een miskraam: één patiënte na reanimatie rond 10 weken zwangerschap en één rond 16 weken. Er was 1 patiënte die een abortus provocatus onderging, de reden hiervoor is niet gekend. Bij de patiënte die gereanimeerd werd en uiteindelijk overleed bij 20 weken zwangerschap, werd reeds op intensieve zorgen het overlijden van de foetus vastgesteld.
Er werden 11 patiënten geïnduceerd, allen (gedeeltelijk) omwille van LMWH-gebruik, 8 van deze patiënten bevielen vaginaal, 3 patiënten kregen alsnog een sectio. Spontane arbeid trad op bij 4 patiënten, van 1 vrouw is de wijze van arbeid niet gekend. Twaalf patiënten bevielen middels sectio caesarea; 6 waren geplande sectio’s, 6 waren spoedsectio’s.
Neonatale uitkomst
Bij één neonaat (amenorroeduur 38 weken 3 dagen) was er een ernstige asfyxie na zowel maternale als neonatale reanimatie, met intubatie en kunstmatige ventilatie op de dienst Neonatale Intensieve Zorgen (NICU). De baby overleefde, maar er waren wel ernstige complicaties. De lange termijn sequelen zijn niet gekend. Zeven baby’s werden opgenomen op de NICU, omwille van prematuriteit, laag geboortegewicht of niet nader gespecifieerde reden.
4.6 Profylaxe
Drie patiënten kregen tromboseprofylaxe antepartum. Dit waren drie patiënten met een gekende trombofilie en nog minstens één bijkomende risicofactor. Twee van deze patiënten kregen echter een te lage dosis. De eerste patiënte nam preconceptioneel
V Leiden homozygoot), bovendien rookte zij nog aan het begin van de zwangerschap en was zij ouder dan 35jaar. Zij kreeg tijdens de zwangerschap een profylactische dosis Enoxaparine, hoewel zij eigenlijk een therapeutische dosis had moeten krijgen. De tweede patiënte was gekend met laag risico trombofilie (verhoogde factor VIII) en een DVT in de voorgeschiedenis en kreeg profylaxe middels Enoxaparine 20mg. Zij woog 50kg en had volgens haar gewicht Enoxaparine 40mg moeten krijgen.
5. DISCUSSIE
Dit is de eerste studie uitgevoerd in België die longembolieën in de zwangerschap geregistreerd en in detail bevraagd heeft. In wat volgt worden de belangrijkste bevindingen beschreven en vergeleken met een gelijkaardig onderzoek uitgevoerd door de UKOSS in het Verenigd Koninktrijk. Dit was een nationale case-control studie waarbij tussen februari 2005 en augustus 2006 alle gevallen van antenatale longembolieën in het Verenigd Koninkrijk werden geregistreerd (4).
Verder wordt een vergelijking gemaakt met de gegevens van alle bevallingen in België geregistreerd in het Studiecentrum voor Perinatale Epidemiologie (SPE) voor Vlaanderen en door het Centre d’Epidemiologie Perinatale (CEpiP) voor Brussel en Wallonië.
5.1 Incidentie
In België werden 29 gevallen van antenatale longembolieën geregistreerd op 446 012 bevallingen op 4 jaar tijd. Dit komt overeen met een incidentie van 0,65 per 10.000 zwangerschappen. UKOSS daarentegen zag een incidentie van 1,3 per 10.000 zwangerschappen.
Hoe kunnen deze verschillen in incidentie verklaard worden?
Enerzijds is er zeker en vast een onderrapportering van het aantal casussen in België. Omdat B.OSS beroep doet op de vrijwillige deelname van meestal drukbezette clinici, is dit systeem sowieso onderhevig aan onderrapportering. Eén groot ziekenhuis weigert deelname aan de B.OSS registratie. Bovendien waren er zes andere ziekenhuizen die slechts enkele maanden tot een jaar lang gerapporteerd hebben. De
noemer voor de berekende incidentie werd hier weliswaar aan aangepast, maar dit kan wel deels een verklaring zijn voor de lagere incidentie van longembolie in België. Het is immers niet geweten hoeveel casussen er zich in deze ziekenhuizen hebben voorgedaan. In het VK daarentegen hebben 100% van de materniteiten hun resultaten gerapporteerd. Zo kon UKOSS met een goede betrouwbaarheid de incidentie berekenen.
Bovendien lijkt het plausibel dat er casussen gemist werden doordat er enkel gynaecologen of hoofdvroedvrouwen in de ziekenhuizen bevraagd werden. Vermoedelijk zijn er enkele diagnoses van longembolie die gesteld werden door een huisarts, op een spoeddienst of door een internist die niet werden opgenomen in de statistieken. Waarschijnlijk gaat het dan voornamelijk om longembolieën in het eerste trimester van de zwangerschap. In het VK werden ook radiologische afdelingen bevraagd waarbij er nog 3 extra casussen aan het licht kwamen en bovendien werden er via het perinatale audit systeem CEMACH (The Confidential Enquiry into Maternal and Child Health) nog 2 bijkomende diagnoses geïdentificeerd.
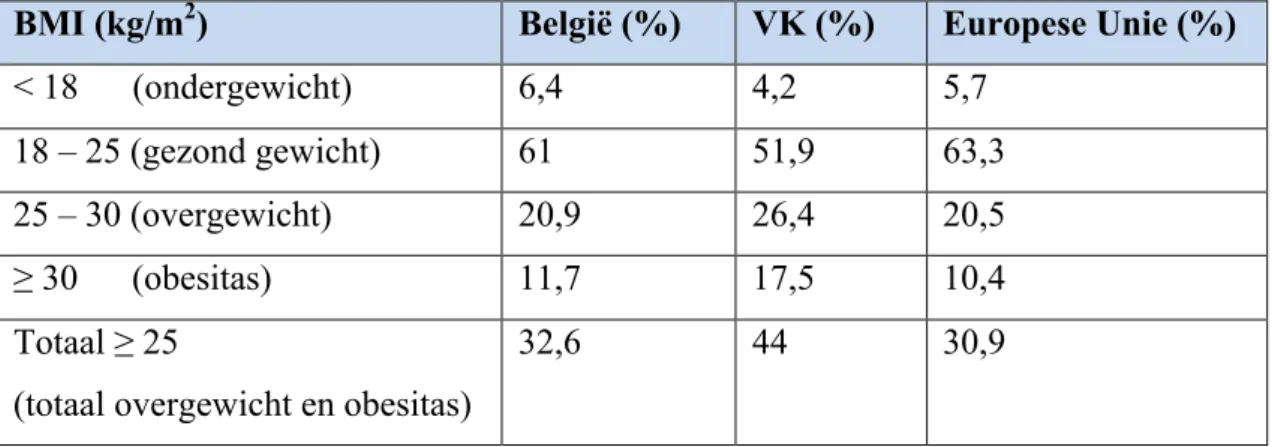
Ten slotte lijkt er toch een verschil te zijn in risicofactoren tussen de twee landen. Het belangrijkste verschil is de prevalentie van obesitas. Deze verschillen zijn te verklaren door de andere levensstijl en eetgewoonten. De prevalentie van obesitas bij vrouwen in de vruchtbare leeftijd (leeftijdscategorie 18-44jaar) in het VK is 17,5% tegenover 11,7% in België (tabel 8). Dit kan één van de redenen zijn waarom de incidentie van longembolie in het VK hoger is dan in België.
Tabel 8: BMI België, VK en Europese Unie volgens gegevens Eurostat, vrouwen tussen 18-44 jaar, jaartal 2014 (18)
BMI (kg/m2) België (%) VK (%) Europese Unie (%)
< 18 (ondergewicht) 6,4 4,2 5,7
18 – 25 (gezond gewicht) 61 51,9 63,3
25 – 30 (overgewicht) 20,9 26,4 20,5
≥ 30 (obesitas) 11,7 17,5 10,4
Totaal ≥ 25
(totaal overgewicht en obesitas)
Om te controleren op onderrapportering werden andere administratieve bronnen geraadpleegd, waar antenatale longembolieën geregistreerd worden. De Federale overheidsdienst Volksgezondheid verzamelt Minimale Ziekenhuisgegevens (MZG) aan hand van ICD-10-cm-codes. Zij identificeerden 9 hospitalisaties met deze code in 2016 en 2017 samen, in tegenstelling tot 13 gerapporteerde casussen via B.OSS. Er waren geen gegevens beschikbaar voor 2015 (gezien overgangsjaar van de codering van ICD9-CM naar ICD-10-BE) en gegevens van 2018 waren nog niet beschikbaar. Bij het InterMutualistisch Agentschap (IMA) loopt momenteel een analyse gebaseerd op de facturatiegegevens van LMWH, beeldvorming middels VQ-scan of CT-angiografie, en bepaling van anti-Xa-activiteit. Resultaten hiervan volgen nog.
5.2 Risicofactoren
In onze studiepopulatie had 72% van de vrouwen minstens 1 identificeerbare risicofactor voor veneuze trombo-embolie. Bij UKOSS was dit 70%. In de controlegroep bij UKOSS had 49% van de vrouwen een risicofactor, waarbij leeftijd > 35jaar en obesitas de meest frequente waren. De enige risicofactoren die bij UKOSS geassocieerd waren met een statistisch significante stijging van de adjusted odds ratio (aOR) waren multipariteit (aOR 4.03, 95% CI 1.60-9.84) en BMI ≥ 30kg/m2 (aOR 2.65, 95% CI 1,09-6,45).
De meest frequente risicofactoren bij de B.OSS studie waren immobilisatie, roken en leeftijd ≥ 35 jaar. Indien men de resultaten van de achteraf uitgevoerde trombofilie testen mee in rekening brengt, wordt ook trombofilie een vaak voorkomende risicofactor in onze populatie.
BMI
In onze database was er 1 patiënte met obesitas (BMI > 30mg/kg2) en had 59% van de onderzochte patiënten overgewicht (BMI 25 – 30mg/kg2). Bij UKOSS had 28% van
de cases en 21% van de controles een BMI tussen 25-30mg/kg2. In de UKOSS studie werden er statistisch significante verschillen gezien wat betreft obesitas. Er werd bovendien gezien dat er een gradiënt is van stijgend risico met toenemend BMI waarbij er een aOR van respectievelijk 2,51 en 2,65 bij BMI 25-30mg/kg2en BMI > 30kg/m2 (tabel 9).
Tabel 9: UKOSS: BMI adjusted odds ratio (aOR)
BMI (kg/m2) Odds ratio
< 20 0,69
20 - 25 1
25 - 30 2,51
≥ 30 2,65
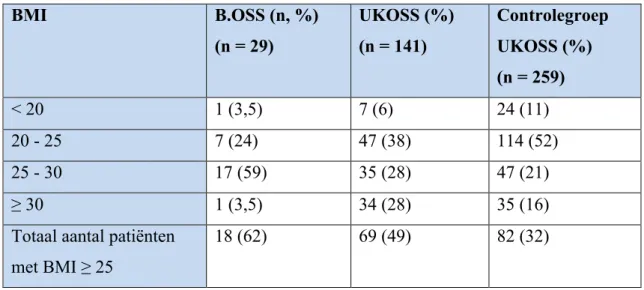
De verdeling van BMI in beide studiepopulaties wordt hieronder weergegeven. Bij B.OSS zijn er duidelijk minder patiënten met obesitas, maar indien men de patiënten met overgewicht en obesitas optelt, ziet men bij B.OSS zelfs een iets hoger percentage dan bij UKOSS: respectievelijk 62% vs. 49% (tabel 10).
Tabel 10: Verdeling BMI B.OSS vs. UKOSS
BMI B.OSS (n, %) (n = 29) UKOSS (%) (n = 141) Controlegroep UKOSS (%) (n = 259) < 20 1 (3,5) 7 (6) 24 (11) 20 - 25 7 (24) 47 (38) 114 (52) 25 - 30 17 (59) 35 (28) 47 (21) ≥ 30 1 (3,5) 34 (28) 35 (16)
Totaal aantal patiënten met BMI ≥ 25
18 (62) 69 (49) 82 (32)
Pariteit
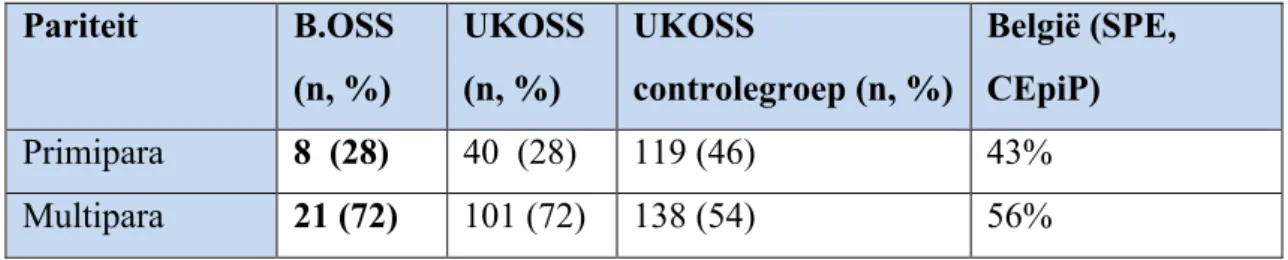
Bij de gerapporteerde gevallen van B.OSS zag men 28% primipara en 72% multipara. UKOSS kon multipariteit weerhouden als een statistisch significante risicofactor voor het ontwikkelen van een longembolie. Dit verschil was reeds significant vanaf een pariteit ≥ 1 (aOR 4.03, 95% CI 1.60-9.84). De percentages van B.OSS en UKOSS komen exact overeen wat betreft pariteit bij de patiënten met antenatale longembolie. Ook de verdeling van de pariteit bij de UKOSS controlegroep en de percentages bij de bevallingen in België tussen 2015 en 2018 komen relatief goed overeen (tabel 11).
Tabel 11: Pariteit: B.OSS vs. UKOSS
Pariteit B.OSS (n, %) UKOSS (n, %) UKOSS controlegroep (n, %) België (SPE, CEpiP) Primipara 8 (28) 40 (28) 119 (46) 43% Multipara 21 (72) 101 (72) 138 (54) 56% Leeftijd
In de studiepopulatie was 28% van de patiënten 35 jaar of ouder. Hier ziet men een klein verschil met de leeftijdsverdeling van alle bevallen patiënten in België gedurende de studieperiode (2015-2018). Uit de gegevens van de jaarrapporten van het SPE en CepiP kon men berekenen dat er gemiddeld 20% van de patiënten 35 jaar of ouder was op het moment van de bevalling (tabel 12).
In de UKOSS studie kon leeftijd ≥ 35 jaar niet weerhouden worden als onafhankelijke risicofactor. De resultaten in de literatuur spreken elkaar tegen. Enkele case-control studies toonden een beperkte toename van het relatieve risico met toenemende leeftijd (19-21). Maar een andere Britse grote cohortestudie kon geen significante verschillen aantonen in de incidentie van VTE antenataal op basis van leeftijd (22). Deze studie zag echter wel een duidelijk verschil in incidentie in het postpartum tussen de beide leeftijdsgroepen.
Tabel 12: Maternale leeftijdsverdeling B.OSS vs UKOSS (2015 – 2018) o.b.v. gegevens van SPE en CepiP jaarrapporten
Leeftijd B.OSS (n, %) UKOSS (n, %) UKOSS controlegroep (n, %) België (SPE, CEpiP) < 35 jaar 8 (72) 98 (70) 190 (74) 80% ≥ 35 jaar 21 (28) 43 (31) 67 (26) 20% Trombofilie
Er werden in de B.OSS studie 7 patiënten met een erfelijke trombofilie geïdentificeerd (24%). Vijf hiervan waren reeds gekend met deze trombofilie, twee patiënten kregen de diagnose pas naar aanleiding van de trombofiliescreening die werd uitgevoerd na de zwangerschap.
In de UKOSS database waren er slechts 4 patiënten met een gekende trombofilie en 7 patiënten met een nieuwe diagnose, wat het totaal op 10 brengt (7%).
Volgens de RCOG zijn erfelijke trombofilieën verantwoordelijk voor 20-50% van de zwangerschapsgerelateerde VTE (8). Vermoedelijk is er toch nog een belangrijke mate van onderrapportering bij de UKOSS data. Ook bij B.OSS gebeurde bij 45% van de casussen (n = 11) geen trombofiliescreening of werd deze niet duidelijk vermeld in de rapportering. Een verklaring hiervoor is dat de trombofiliescreening niet kan plaatsvinden tijdens de zwangerschap (op het moment van diagnose), noch in het onmiddellijke postpartum gezien de fysiologische veranderingen van de stollingsmechanismen nog enkele weken aanhouden. Trombofiliescreening gebeurt bovendien idealiter pas na staken van de anticoagulantia en op dat moment zijn de patiënten al lang niet meer bij de gynaecoloog in opvolging.
Immobilisatie en hospitalisatie
(Relatieve) immobilisatie was één van de meest frequente risicofactoren bij B.OSS. Hierbij zijn zowel patiënten geteld die gehospitaliseerd waren, die thuis bedrust werden voorgeschreven omwille van preterme contracties en een laatste patiënt die een langdurige vliegtuigreis had ondernomen.
Er zijn weinig data over immobilisatie als risicofactor tijdens de zwangerschap, daarom worden data geëxtrapoleerd uit studies bij niet zwangere patiënten (23). Volgens richtlijnen van NICE (24) en RCOG (25) verhoogt elke reis > 4 uur het risico op een VTE bij de zwangere vrouw, dit onafhankelijk van het feit of deze via auto of vliegtuig plaatsvindt. Aanbevelingen zijn dan ook dat elke zwangere vrouw bij een reis > 4 uur TED-kousen gebruikt. Indien er bijkomende risicofactoren aanwezig zijn, kan bovendien profylaxe met LMWH worden overwogen de dag van de reis en enkele dagen nadien (24).Ziekenhuisopname tijdens de zwangerschap verhoogt het risico op VTE met factor 18 en is bovendien afhankelijk van de duur van de opname (26). Het risico is het hoogste tijdens het derde trimester en bij de aanwezigheid van bijkomende risicofactoren. De RCOG raadt in haar richtlijn dan ook aan dat bij elke gehospitaliseerde zwangere patiënt tromboseprofylaxe dient overwogen te worden. TED-kousen zijn bij opgenomen zwangere patiënten geïndiceerd. Bovendien raden zij aan om laagdrempelig ook LMWH’s te starten, onafhankelijk van bijkomende risicofactoren (8). Geen enkele van de gehospitaliseerde patiënten in onze studie
kreeg LMWH tijdens de hospitalisatie. Er zijn in België geen nationale richtlijnen die het gebruik van LMWH tijdens de zwangerschap voorschrijven.
5.3 Diagnostiek
De diagnose werd bij 25 van de 29 patiënten gesteld op basis van V/Q-scan of CT-angiografie. Zoals reeds eerder vermeld zijn beide onderzoeken evenwaardig en veilig in de zwangerschap. Bij 3 patiënten werd er geen beeldvorming van de thorax uitgevoerd, maar werd reeds een DVT vastgesteld op duplexechografie. In combinatie met klachten suggestief voor longembolie (dyspneu) werd opgestart met LMWH. Dit is een correcte manier van handelen en op deze manier vermindert men de stralenbelasting voor patiënte en foetus (10, 13).
5.4 Behandeling
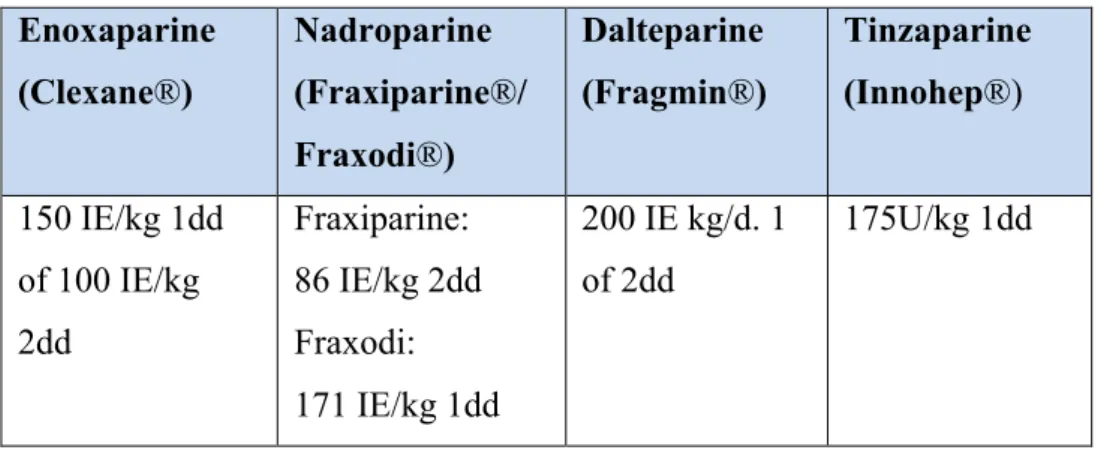
De meest gebruikte behandeling was Enoxaparine (Clexane®) 2 keer per dag. De dosis is gebaseerd op het gewicht van de vrouw in het begin van de zwangerschap (tabel 13). Tijdens de zwangerschap verandert het distributievolume en de snelheid van de renale klaring. Dit resulteert in veranderingen in de farmacokinetica van LMWH’s (27). Er is echter geen enkele studie die een voordeel kon aantonen van één of tweemaal daags toedienen van LMWH’s.
Tabel 13: LMWH therapeutische dosis Enoxaparine (Clexane®) Nadroparine (Fraxiparine®/ Fraxodi®) Dalteparine (Fragmin®) Tinzaparine (Innohep®) 150 IE/kg 1dd of 100 IE/kg 2dd Fraxiparine: 86 IE/kg 2dd Fraxodi: 171 IE/kg 1dd 200 IE kg/d. 1 of 2dd 175U/kg 1dd Duur behandeling
Behandeling met therapeutische doses anticoagulantia dienen gecontinueerd te worden gedurende het vervolg van de zwangerschap minstens tot en met 6 weken postpartum. De totale duur van de behandeling dient minimaal 3 maanden te zijn (13).
Bij 5 patiënten werd de duur van de behandeling niet gespecifieerd. Eén patiënt werd niet lang genoeg behandeld. De andere patiënten (n = 22) werden minimaal 3 maanden en minstens 6 weken postpartum behandeld met anticoagulantia.
5.5 Uitkomst
In de B.OSS studie werden er 3 patiënten gereanimeerd, waarvan 1 patiënt het niet overleefde. Dit komt overeen met een maternale sterfte van 3,5%. Ook bij UKOSS was de case fatality 3,5%; daar stierven namelijk 5 van de 143 vrouwen. Bovendien is er een groot percentage patiënten met ernstige maternale morbiditeit. Bij B.OSS werden er 8 van de 29 patiënten opgenomen op Intensieve Zorgen.
5.6 Profylaxe
Het VK had reeds nationale richtlijnen betreffende preventie en behandeling van veneuze trombo-embolie in de zwangerschap ook toen de UKOSS studie liep. Sommige casussen waren het gevolg van suboptimale implementatie van deze richtlijnen. Uit deze studie bleek dan ook dat niet alle risicopatiënten (de correcte) tromboseprofylaxe kregen ondanks bestaande nationale richtlijnen.
Indien we de resultaten van B.OSS toetsen aan de Britse richtlijnen (8) kunnen we concluderen dat ook in België enkele patiënten onvoldoende profylaxe kregen. Eén patiënt kreeg een te lage dosis Enoxaparine volgens haar gewicht (tabel 14). Een tweede patiënt werd prenataal therapeutisch ontstold met Warfarine, maar werd tijdens de zwangerschap op een profylactische dosis Enoxaparine gezet. Bovendien hadden 3 patiënten volgens de Britse richtlijn tijdens opname in het ziekenhuis LMWH’s moeten krijgen. Zij hadden namelijk bovenop de risicofactor van ziekenhuisopname tijdens de zwangerschap nog 1 of 2 bijkomende risicofactoren. Twee patiënten kwamen in aanmerking voor tromboseprofylaxe, maar bij hen was het volgens de richtlijnen niet obligaat. Beide patiënten kregen ook geen TED-kousen ter profylaxe.
Twee patiënten met een laag risico trombofilie (factor V Leiden heterozygoot) kregen Aspirine 100mg toegediend. Eén patiënte kreeg deze profylaxe correct ter preventie van pre-eclampsie gezien haar obstetrische voorgeschiedenis. Aspirine is echter geen profylaxe voor het ontwikkelen van een VTE. De enige trombofilie waarbij aspirine tijdens de zwangerschap geïndiceerd is, is het antifosfolipidensyndroom. Dit dient
echter ter preventie van obstetrische complicaties zoals herhaald miskraam en pre-eclampsie.
Tabel 14: LMWH profylactische dosis (8)
Gewicht Enoxaparine (Clexane®) Dalteparine (Fragmin®) Tinzaparine (75U/kg/dag) (Innohep®) <50kg 20mg/d 2500IU/d 3500U/d 50-90kg 40mg/d 5000IU/d 4500U/d 91-130kg 60mg/d 7500IU/d 7000U/d 131-170kg 80mg/d 10.000IU/d 9000U/d >170kg 0,6mg/kg/d 75U/kg/d 75U/kg/d 5.7 Richtlijnen
Gezien het absolute risico op het ontwikkelen van een VTE tijdens de zwangerschap laag is, dient er een risicostratificatie te gebeuren om te bepalen welke vrouwen er al dan niet in aanmerking komen voor tromboseprofylaxe. In 2015 reviseerde de RCOG de laatste keer zijn uitgebreide guideline (8). Een Belgische richtlijn dateert echter van 2009 en is sindsdien niet meer herzien (15). In België wordt door gynaecologen dan ook voornamelijk beroep gedaan op beschikbare richtlijnen van andere landen en worden er bovendien ziekenhuisbrede richtlijnen opgesteld. Het ontbreken van nationale richtlijnen leidt dus tot willekeur en de heterogeniteit geobserveerd in deze studie.
De RCOG raadt aan om bij iedere vrouw preconceptioneel en/of aan het begin van de zwangerschap eventuele risicofactoren voor het ontwikkelen van een VTE te identificeren. Deze risk assessment dient herhaald te worden wanneer de patiënte bijvoorbeeld wordt opgenomen in het ziekenhuis (figuur 1).
Figuur 1: Antenatale tromboseprofylaxe volgens RCOG (8)
SLE = systemische lupus erythematosus, IBD = inflammatoire darmziekte, DM = diabetes mellitus, OHSS = ovarieel hyperstimulatiesyndroom, IVF = in vitro fertilisatie, ARG = geassisteerde reproductieve geneeskunde
* BMI ≥ 30 en 2 risicofactoren
5.8 Beperkingen van de studie
Als tekortkomingen van deze studie noteren we het gebrek aan een controlegroep. Enkele variabelen konden wel beschrijvend vergeleken worden met een controlepopulatie uit statistieken van de jaarverslagen van het SPE en CepiP, maar er waren te weinig variabelen om deze correct als controlegroep te gebruiken. Door het beperkt aantal casussen en het ontbreken van deze controlegroep, hebben we ons in deze studie beperkt tot een beschrijvende statistiek en kunnen er geen statische significante conclusies worden gemaakt. Verder doet B.OSS beroep op de vrijwillige deelname van de Belgische materniteiten, waardoor zeker en vast een deel van de gevallen gemist werd.
5.9 Conclusie en toekomstperspectieven
Met deze studie kunnen we aantonen dat antenatale longembolie ook in België een zeldzame, maar zeer ernstige aandoening is. De diagnose is soms moeilijk te stellen aangezien de symptomen kunnen lijken op fysiologische verschijnselen tijdens de zwangerschap. Daarom moet iedere zwangere patiënte die zich aanmeldt met thoracale pijn of dyspneu grondig worden onderzocht en indien nodig dienen er laagdrempelig bijkomende onderzoeken te gebeuren. Bovendien is er vastgesteld dat er een zeer grote heterogeniteit is in de behandeling, maar voornamelijk in de preventie van VTE. Er dient gestreefd te worden naar meer uniforme zorg en daarom is er nood aan evidence-based richtlijnen. De Belgische richtlijnen dateren van 2009 en zijn te beperkt. Een revisie van deze richtlijnen dringt zich dan ook op.
De maternale sterftecijfers representeren slechts het topje van de ijsberg. De andere patiënten worden niet in de statistieken opgenomen. Daardoor is er een onderschatting van de morbiditeit die veroorzaakt wordt door longembolie. Laattijdige diagnose, laattijdige of inadequate behandeling en suboptimale tromboseprofylaxe lijken verantwoordelijk voor veel van deze gevallen. Dankzij registratiesystemen als B.OSS en UKOSS kan men tekortkomingen in de aanpak van deze ernstige complicaties blootleggen en kan het aandeel worden ingeschat van dit deel van de ijsberg dat anders nooit zichtbaar was geworden. Dit toont aan hoe belangrijk het is door te gaan met de registratie van zeldzame en ernstige aandoeningen in de zwangerschap. Op deze manier kunnen landen hun richtlijnen aanpassen en de kwaliteit van zorg verbeteren. Alleen zo kunnen deze near-miss events en maternale overlijdens in de toekomst vermeden worden.
6. REFERENTIES
1. Vandenberghe G. The point of surveying severe maternal morbidity: the Belgian Obstetric Surveillance System. Scriptie voorgedragen in het kader van de opleiging tot doctor in de Gezondheidswetenschappen, Universiteit Gent 2017-2018; 19.
2. Vandenberghe G, Roelens K, Van Leeuw V et al. The Belgian Obstetric Surveillance System to monitor severe maternal morbidity.
3. Knight M, Lewis G, Acosta CD et al. Maternal near-miss case reviews: the UK approach. BJOG. 2014;121 Suppl 4:112-6.
4. Knight M, UKOSS. Antenatal pulmonary embolism: risk factors, management and outcomes. BJOG 2008;115(4): 453-61.
5. Knight M. The International Network of Obstetric Survey Systems (INOSS): benefits of multicountry studies of severe and uncommon maternal
morbidities. Acta Obstet Gynecol Scand. 2014;93:127-31.
6. Devlieger R, Goemas R, Laubach M. Perinatale activiteiten in Vlaanderen 2018. SPE, Brussel, 2018. Opgehaald op 15/03/2020, van https://www.zorg-
en-gezondheid.be/sites/default/files/atoms/files/EMBARGO_SPE_Perinatale%20 activiteiten%20in%20Vlaanderen%202018.pdf
7. Devis P, Knuttinen MG. Deep venous thrombosis in pregnancy: incidence, pathogenesis and endovascular management. Cardiovasc Diagn Ther 2017;7(Suppl 3):S309-2319.
8. Royal College of Obstetricians and Gynaecologists. Green-top Guideline No. 37a: Reducing the Risk of Venous Thromboembolism during Pregnancy and the Puerperium. Update 2015. Available from:
https://www.rcog.org.uk/globalassets/documents/guidelines/gtg-37a.pdf 9. Bates SM, Middeldorp S, Rodger M, James AH, Greer I. Guidance for the
treatment and prevention of obstetric-associated venous thromboembolism. J Thromb Thrombolysis 2016;41(1):92-128.
10. Nelson-Piercy C. Handbook of Obstetric Medicine. Fifth edition. CRC Press, 2015; 45-62.
11. Macklon NS, Greer IA. The deep venous system in the puerperium: an ultrasound study. Br J Obstet Gynaecol 1997;104:198-200.
12. James AH, Tapson VF, Goldberg SZ. Thrombosis during pregnancy and the postpartum period. Am J Obstet Gynecol 2005;193:216-9.
13. Royal College of Obstetricians and Gynaecologists. Green-top Guideline No. 37b: Thromboembolic Disease in Pregnancy and the Puerperium: Acute Management. Update 2015. Available from:
https://www.rcog.org.uk/globalassets/documents/guidelines/gtg-37b.pdf 14. Duhl AJ , Paidas MJ, Ural SH et al. Pregnancy and Thrombosis Working
Group. Antithrombotic therapy and pregnancy: consensus report and recommendations for prevention and adverse pregnancy outcomes. Am J Obstet Gynecol 2007; 197:457.e1-21.
15. ‘Preventie van veneuze trombo-embolie bij zwangere vrouwen ’ en ‘Treatment of VTE’ van de Thrombosis Guidelines Group of the Belgian Society on Thrombosis and Haemostasis and the Balgian Working Group on Angiology.
16. Van Leeuw V, Moreau N, Leroy C.
Santé périnatale en Région bruxelloise Année 2018. Opgehaald op 10/04/2020, van
https://www.cepip.be/pdf/rapport_CEPIP_Bxl2018_FR_2tma.pdf
17. Leroy C, Moreau N, Van Leeuw V. Santé périnatale en Wallonie Année 2018. Opgehaald op 10/04/2020, van
https://www.cepip.be/pdf/rapport_CEPIP_Wal2018_2tma.pdf 18. Eurostat, BMI. Afgehaald op 15/4/2020, van
https://ec.europa.eu/eurostat/data/browse-statistics-by-theme
19. Lindqvist P, Dahlbäck B, Marsal K. Thrombotic risk during pregnancy: a population study. Obstet Gynecol 1999;94:595-9.
20. Liu S, Rouleau J, Joseph KS, et al. Maternal Health Study Group of the Canadian Perinatal Surveillance System. Epidemiology of
pregnancy-associated venous thromboembolism: a population study in Canada. J Obstet Gynaecol Can 2009; 31:611-20.
21. Simpson EL, Lawrenson RA, Nightingale AL, Farmer RD. Venous
thromboembolism in pregnancy and the puerperium: incidence and additional risk factors from a London perinatal database. BJOG 2001;108:56-60.
22. Sultan AA, West J , Tata LJ et al. Risk of first venous tromboembolism in and around pregnancy: a population-based cohort study. Br J Haematol
2012;156:366-73.
23. Anderson FA Jr, Spencer FA. Risk factors for venous trhromboembolism. Circulation 2003;107 Suppl 1:I9-16.
24. National Collaborating Centre for Women’s and Children’s Health. Antenatal care: routine care for the healthy pregnant woman. London: RCOG Press; 2008.
25. Royal College of Obstetricians and Gynaecologists. Air Travel and Pregnancy. Scientific Impact Paper No. 1. London: RCOG;2013.
26. Abdul Sultan A, West J, Tata LJ et al. Risk of venous thromboembolism in pregnant women in hospital: population based cohort study from England. BMJ 2013; 347:f6099.
27. Patel JP, Green B, Patel RK, et al. Population pharmacokinetics of enoxaparine during the antenatal period. Circulation 2013;128:1462-9.
7. BIJLAGEN: VRAGENLIJST B.OSS
Antenatal Pulmonary
Embolism
DATA COLLECTION FORM
Hospital name
Hospital case number
(gelieve hier een dossiernummer of andere code in te vullen, waardoor u in staat bent het dossier van deze casus makkelijk te traceren op een later tijdstip)
BACKGROUND INFORMATION
Pulmonary embolism (PE) is a leading cause of maternal death,
demonstrated in the 7th report of Confidential Enquiries into
maternal deaths in the United Kingdom (2007), and other
comparable reports of Norway, Australia, United States. An overview
of maternal deaths in SPE (Studiecentrum voor Perinatale
Epidemiologie) reported 92 maternal deaths since onset of SPE-registration, of which 12 cases were caused by pulmonary embolism,
being the second most frequent cause.
UKOSS has studied Antenatal Pulmonary Embolism in a case-control
study: between February 2005 and August 2006 they identified 143
cases, representing an incidence of 1.3 per 10.000 maternities (95%
1.1-1.5). UK has comprehensive guidelines on both prevention and
management of venous thromboembolism in pregnancy (RCOG green
top guideline No 37 a and No 37 b). Some of the cases identified were
the consequence of suboptimal implementation of the national
guidelines for the prevention of thrombosis during pregnancy.
However, the majority of the cases (94%) were not eligible for
thromboprophylaxis according to the current guidelines. Multiparity
and obesity were the main riskfactors, but even this large cohort
study had insufficient power to show statistically significant
associations with other riskfactors. This highlights the need for very
large, multinational studies of rare conditions to accurately identify
and quantify significant risks. Antenatal pulmonary embolism is or
has been studied by other Obstetric Surveillance Systems: AMOSS
(Australia – New Zealand), AuOSS (Austria), France (EPIMOMS),
GerOSS (Germany).
In Belgium we are currently unaware of the incidence of antenatal
pulmonary embolism, how antenatal PE is diagnosed, how we
manage antenatal PE and what the outcomes are for both mother and
child.
A nationwide study of antenatal PE during 4 years by B.OSS can
provide more insight in this rare but possible life-threatening
disorder of pregnancy in Belgium. Furthermore this study can
contribute to an international study as part of the INOSS (the
International Network of Obstetric Survey Systems).
Research questions:
1.What is the incidence of antenatal pulmonary embolism in
Belgium?
2.
How is antenatal pulmonary embolism managed in Belgium? (What
guidelines do we use?)
3.What is the outcome of antenatal pulmonary embolism in Belgium
for mother and child?
Definition pulmonary embolism
B.OSS will use the same definition as used by UKOSS, to enable
comparison and participation in international studies.
–
EITHER
PE is confirmed using suitable imaging (angiography,
computed tomography, echocardiography, magnetic
resonance imaging or ventilation-perfusion scan showing
a high probability of PE)
–
OR PE is confirmed at surgery or postmortem
–
OR a clinician has made a diagnosis of PE with signs
and symptoms consistent with PE present, and the
patient has received a course of anticoagulation therapy
(>1 week duration)